Knochenwachstum und Knochenverlust
Knochenaufbau- und Knochenumbauvorgänge werden durch das Zusammenspiel von 4 Zelltypen (Osteoblasten, Osteoklasten, Osteozyten und Saumzellen) reguliert. Führen diese Aktivitäten in Summe zu einer zunehmenden Knochenmasse und/oder -größe wird dieser Prozess als „Bone Modeling“ bezeichnet. Der Ersatz alten Knochens durch neuen im Erwachsenenalter erfolgt vorwiegend durch das Bone Remodeling, welches jeweils durch einen lokalen Knochenabbau eingeleitet und durch die vollständige Mineralisation neu gebildeten Knochens vollendet wird. Auf diese Art und Weise wird das gesamte knöcherne Skelett etwa alle 10 Jahre einmal vollständig erneuert.
Physiologischer Knochenmasseverlust
Das knöcherne Skelett des Erwachsenen weist über viele Jahre eine sehr konstante Knochenmasse auf, wobei ein physiologischer Knochenmasseverlust von zumeist unter 1 % jährlich keine wesentlichen Auswirkungen auf die Bruchfestigkeit hat. Während beim männlichen Geschlecht dieser eher geringgradige jährliche Verlust im Wesentlichen bis in das Senium erhalten bleibt, zeigen Untersuchungen beim weiblichen Geschlecht, dass während der menopausalen Transition innerhalb eines Zeitraums von etwa 3 Jahren der Knochenmasseverlust besonders stark beschleunigt ist. Bemerkenswert ist hierbei, dass dieser beschleunigte Abbau bereits rund ein Jahr vor dem letzten Menstruationszyklus beginnt, und zwar ohne messbar verringerte Östrogenspiegel. In diesen Jahren des „unbalancierten Remodelings“ kann der jährliche Knochenmasseverlust durchaus 10 % und mehr betragen.
Bemerkenswert ist, dass bei beiden Geschlechtern mit zunehmendem Alter sowohl der innere als auch der äußere Knochendurchmesser zunimmt, wobei die Zunahme des äußeren Durchmessers beim männlichen Geschlecht ausgeprägter ist. Dies erklärt zumindest teilweise, warum der männliche Röhrenknochen auch im Alter weniger bruchgefährdet ist als der weibliche.
Diagnose der Osteoporose
Die operationale Definition der Osteoporose orientiert sich seit 1994 an der Knochenmineraldichte (KMD), bestimmt mittels Zwei-Spektren-Röntgenabsorptiometrie (Dual X-Ray Absorptiometry, DXA). Bei einem KMD-Wert (ausgedrückt als T-Score) von 2,5 Standardabweichungen oder mehr unter dem mittleren Normwert knochengesunder junger Erwachsener darf laut WHO eine Osteoporose diagnostiziert werden. Allerdings sollte mit diesem Begriff insbesondere bei jüngeren Erwachsenen behutsam umgegangen werden. Während z. B. ein T-Score von –2,5 bei einer 80-jährigen Frau ein vielfach erhöhtes Knochenbruchrisiko bedeutet, so ist derselbe Wert bei einer 40-jährigen gebärfähigen Frau nahezu bedeutungslos, da ihr Frakturrisiko nur unwesentlich über jenem Knochengesunder liegt. Ein weiteres für die tägliche Praxis wesentliches Faktum ist, dass die Mehrheit aller Frakturen bei Erwachsenen nicht im osteoporotischen, sondern im osteopenischen KMD-Bereich auftritt, also bei einem T-Score von –1,0 bis –2,5. Die Diagnose einer (manifesten) Osteoporose ist in jedem Fall auch dann zu stellen, wenn eine Fraktur nach niedrigem oder inadäquatem Trauma bei osteopenischer oder sogar normaler KMD auftritt.
Erfassung des individuellen Knochenbruchrisikos
Anders als noch vor zwei Jahrzehnten liegt der Fokus in der Beurteilung des individuellen Knochenbruchrisikos heute auf der Erfassung von Risikofaktoren, welche weitgehend unabhängig von der KMD sind. Beispiele sind neben dem Geschlecht und dem Alter Faktoren wie Rauchen oder eine längerfristige systemische Behandlung mit Glukokortikoiden. Diese und andere Risikofaktoren sind die Grundlage von Algorithmen, welche in Frakturrisiko-Assessment-Werkzeugen Anwendung finden. Das weltweit bedeutendste Werkzeug ist FRAX®, welches bereits für mehr als 85 % der Weltpopulation, einschließlich einer Österreich-Version, webbasiert zur Verfügung steht.
Behandlungsindikation und Behandlungsschwellen
Die (erste) osteoporotische Fraktur bedeutet eine Vervielfachung des Risikos für weitere Frakturen. Aus diesem Grund besteht bei prävalenter niedrig traumatischer Fraktur ein „hohes Frakturrisiko“ – und somit unabhängig von der KMD eine absolute Indikation für eine osteoporosespezifische Behandlung. Die „Arznei & Vernunft“-Leitlinie in der geltenden Version (2017) sieht daher auch vor, dass alle Personen im Alter 50+ eine osteoporosespezifische Behandlung erhalten, wenn sie bereits eine niedrig traumatische Fraktur erlitten haben oder ein 10-Jahres-Frakturrisiko laut FRAX®-Berechnung von 20 % für die wichtigsten osteoporotischen Frakturen oder 5 % für die Schenkelhalsfrakturen aufweisen. Zusätzlich hat nun eine rezente Studie gezeigt, dass innerhalb der ersten 1 bis 2 Jahre das Risiko einer Folgefraktur am höchsten ist. Für diesen Zeitraum wird daher auch ein „sehr hohes“ Risiko angenommen.
Medikamentöse Therapieoptionen
Zu den klassischen osteoporosespezifischen Pharmaka zählen die Antiresorptiva, welche in erster Linie die Knochenresorption hemmen und zu einer verstärkten Mineralisation bestehenden Knochens führen. Antiresorptiva sollten gemäß aktuellen Empfehlungen der International Osteoporosis Foundation (IOF) sowie mehrerer europäischer Leitlinien (z. B. NOGG) primär bei „hohem“ Frakturrisiko zum Einsatz kommen.
Für die kürzlich etablierte Kategorie des „sehr hohen“ Frakturrisikos wird hingegen der primäre Einsatz knochenanabol wirksamer Substanzen empfohlen, weil deren positiver Effekt auf das Knochenbruchrisiko rascher eintritt und ausgeprägter ist als jener unter antiresorptiv wirksamen Substanzen. Im Gegensatz zu Letzteren kommt es unter knochenanabol wirksamen Substanzen zu einem echten „Modeling“, also einem echten Zuwachs an Knochen. Dies drückt sich unter anderem in einer Zunahme der Knochentrabekelzahl, aber auch der Knochentrabekeldicke aus. Die Mineralisation des neu gebildeten Knochens folgt mit zeitlicher Verzögerung, weswegen im Anschluss an eine knochenanabole Behandlung auch immer eine Konsolidierung mit einem Antiresorptivum erfolgen muss. Die kürzlich seitens der Europäischen Arzneimittelbehörde zugelassene Substanz Romosozumab nimmt hier insofern auch nochmals eine Sonderstellung ein, als ihr knochenanaboler Effekt in den ersten Anwendungsmonaten zum Tragen kommt und danach von einer vorwiegend antiresorptiv wirksamen Phase abgelöst wird. Der Wirkmechanismus wird daher auch häufig als „dual“ bezeichnet.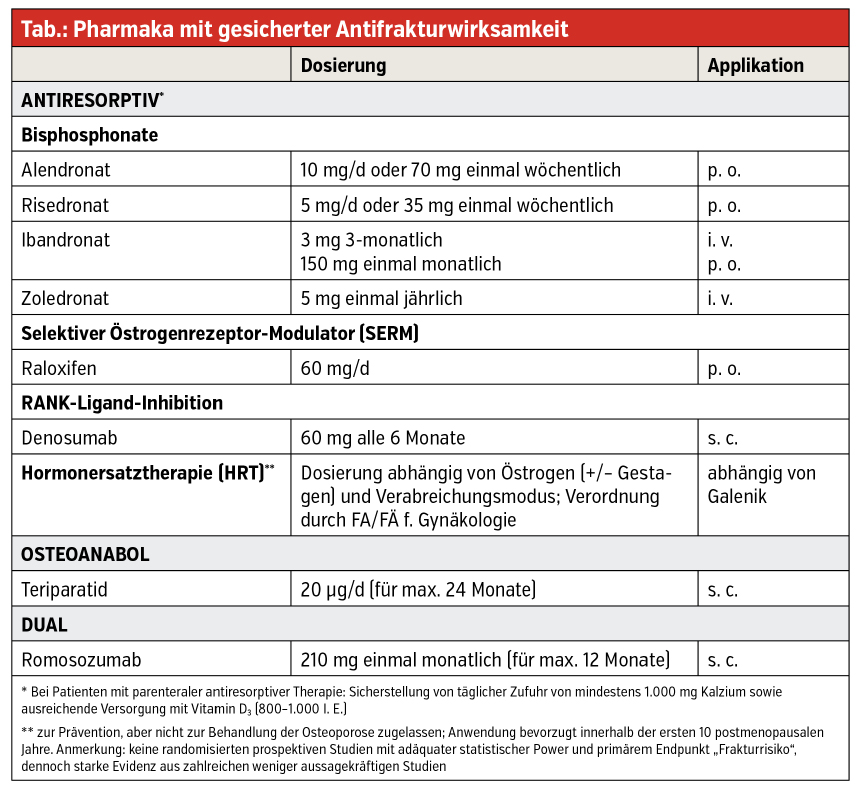
- Etwa ein Jahr vor dem letzten Menstruationszyklus beginnt ein stark beschleunigter Knochenabbau, und zwar ohne messbar verringerte Östrogenspiegel.
- Der männliche Röhrenknochen weist im Vergleich zum weiblichen einen durchschnittlich größeren Gesamtdurchmesser auf, was sich positiv auf die Bruchfestigkeit auswirkt.
- Unter einer osteoanabolen Therapie kommt es vor allem durch eine Zunahme der Trabekelzahl und der Trabekeldicke zu einem realen Zuwachs an Knochenmasse.























































































