Aspirin-(In-)Toleranz bei N-ERD
NSAID-Exacerbated Respiratory Disease (N-ERD), auch bekannt als Morbus Widal, Samter’s Triad, aspirinsensitives Asthma oder Aspirin-Exacerbated Respiratory Disease (AERD), umfasst die Symptomtrias aus allergischem Asthma, chronischer Rhinosinusitis mit nasaler Polyposis (CRSwNP) sowie einer Unverträglichkeit gegenüber nichtsteroidalen Antirheumatika (NSAID), die zu einer starken Beeinträchtigung der Lebensqualität führen kann. Die Prävalenz der N-ERD ist derzeit nicht genau bekannt. In der Literatur wird berichtet, dass unter den Patienten mit CRSwNP etwa 30 % ein allergisches Asthma und davon ca. 15 % eine NSAID-Intoleranz haben (Abb. 1).1, 2
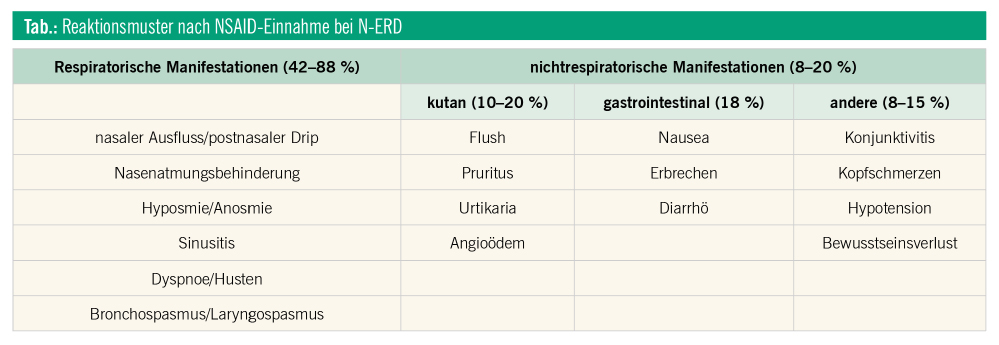
Das durchschnittliche Erkrankungsalter liegt bei 35 Jahren, wobei zu diesem Zeitpunkt die klassische Trias noch nicht vorliegen muss und sich erst im Laufe der Zeit manifestieren kann. Anfänglich bestehen oft unspezifische Beschwerden im Bereich der Nase, Nasennebenhöhlen und/oder Bronchien, die den charakteristischen Symptomen einer Schmerzmittel-Intoleranz vorausgehen. Dazu zählen verstopfte oder „laufende“ Nase, Störungen des Geruchssinnes oder Kopfschmerzen. Auch Symptome einer Sinusitis oder Nasenpolypen können sich bereits Jahre zuvor bemerkbar machen. Unter Exposition mit einem Schmerzmittel vom NSAID-Typ entwickeln N-ERD-Patienten vorwiegend Symptome der oberen und unteren Atemwege, wie beispielsweise Rhinorrhö, Rhinitis, Husten, Bronchialkrämpfe, Asthmaanfälle, aber auch Reaktionen im Gastrointestinaltrakt oder schwere anaphylaktische Reaktionen (Tab.).
Patienten sollten ASS und alle anderen nichtselektiven Cyclooxygenase-(COX-)Inhibitoren konsequent meiden. Grundsätzlich gibt es kein Analgetikum, das von allen N-ERD-Patienten gleich gut toleriert wird. Eine Alternative stellt Paracetamol (Acetaminophen) dar, das vorwiegend ein COX-3-Hemmer ist und nur schwach COX-1 und COX-2 inhibiert (COX-1 wird hierbei nur in hohen Konzentrationen gehemmt). Weitere Analgetika, die nur selten Unverträglichkeitsreaktionen hervorrufen und präferiert als Ausweichpräparate empfohlen werden, sind Lornoxicam bzw. weitere Wirkstoffe aus der Gruppe der selektiven COX-2-Hemmer (Celecoxib, Etoricoxib, Parecoxib). ASS-intolerante Patienten können entsprechende Symptome auch durch Verwendung von Zahnpasta entwickeln: Minze, Menthol oder minzartige Aromen, die für den erfrischenden Geschmack in einigen Zahnpasten sorgen, sind häufig salicylathaltig.
Pathogenese
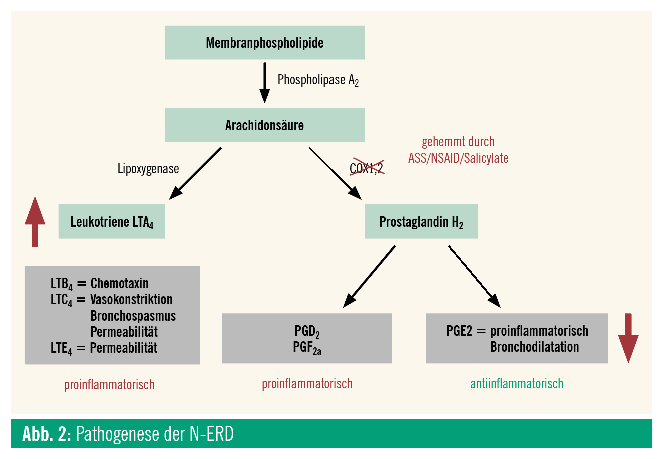
Die N-ERD wird durch ein Ungleichgewicht bei der Umbildung des Vorläuferhormons Prostaglandin H2 im Arachidonsäurestoffwechsel verursacht, wobei der entzündungshemmende Mediator Prostaglandin E2 vermindert produziert wird und der COX-2-abhängige proentzündliche Mediator Prostaglandin D2 und seine Metaboliten überwiegen. Wodurch dieses primäre Ungleichgewicht entsteht, ist derzeit noch nicht endgültig geklärt. Die Exposition mit einem NSAID führt zu einer weiteren Reduktion von Prostaglandin E2 und zur Akkumulation von Leukotrienen, wodurch proinflammatorische Wege weiter verstärkt werden (Abb. 2) und es unter Beteiligung von T-Helferzellen der Typ-2-Immunität (Th2) zu einer ausgedehnten eosinophilen Schleimhautentzündung in den unteren und oberen Atemwegen kommt.3, 4
Mastzellen sind eine wichtige Quelle für proinflammatorische Mediatoren, wie Leukotriene oder Prostaglandin D2, wodurch die eosinophile Entzündung auch bei stabiler N-ERD vorangetrieben wird. Es konnte gezeigt werden, dass auch Immunglobulin E (IgE) bei N-ERD-Patienten in der Nasenschleimhaut stark erhöht ist und eine zentrale Rolle in der Entstehung von nasalen Polypen spielt, indem es Mastzellen aktiviert und die Typ-2-Immunität weiter verstärkt.5 Tomassen et al. führten eine Studie zur Beschreibung der Entzündungsmuster bei Patienten mit chronischer Rhinosinusitis durch und korrelierten die Cluster der immunologischen Endotypen mit den entsprechenden Phänotypen. Es konnte gezeigt werden, dass bei Patienten mit CRSwNP und Asthma die Zytokinprofile ähnlich sind und ein durch IL-5 und IgE dominiertes Typ-2-Entzündungsprofil vorliegt.6
Therapieoptionen der N-ERD
Adaptive Desaktivierung
Eine große Bedeutung in der Therapie NSAID-sensitiver Patienten hatte bisher die adaptive ASS-Desaktivierung. Ziel ist es, eine Toleranzinduktion durch die wiederholte Verabreichung von ASS in aufsteigender Dosierung zu erreichen. Die adaptive Desaktivierung kann oral oder kombiniert inhalativ/oral erfolgen, wobei sich die orale Applikation als Standardverfahren etabliert hat. Die Desaktivierungsschemata variieren stark, meist wird mit einer Dosierung von 30 mg begonnen und alle 30 Minuten die Dosis verdoppelt bis zum Erreichen der Erhaltungsdosis, die zwischen 300 mg und 1.200 mg liegt.7, 8 Nach dem Erreichen der individuellen Schwellendosis muss diese als dauerhafte ASS-Erhaltungsdosis eingenommen werden, um die Toleranz aufrechtzuerhalten. Die adaptive Desaktivierung wurde bereits in einigen Studien untersucht, in denen sich eine signifikante Reduktion der Polypengröße, der nasalen Beschwerden und eine Verbesserung der Asthmasymptomatik sowie eine Verminderung von Exazerbationen und Hospitalisierungen nachweisen ließen.10 Eine hohe Compliance des Patienten muss jedoch gewährleistet sein. Kommt es zur Unterbrechung der täglichen ASS-Einnahme, tritt nach Überschreiten der Refraktärzeit, die nur 24 h betragen kann, ein Verlust der Toleranz gegenüber ASS auf. Wird dann die Therapie unkontrolliert wieder fortgesetzt, ist erneut mit schweren anaphylaktischen Reaktionen zu rechnen. Zusätzlich kann eine dauerhafte NSAID-Einnahme mit schweren Nebenwirkungen einhergehen, wie z. B. der Gefahr gastrointestinaler Ulzera und Blutungen.
Biologika
Zielgerichtete Biologika sind moderne und vielversprechende Therapieansätze für Patienten mit Erkrankungen der Typ-2-Immunität. Derzeit sind zwei Biologika, Omalizumab und Dupilumab, für die Indikationen Asthma und CRSwNP zugelassen. Auch für Patienten mit N-ERD stellen diese Behandlungen eine vielversprechende Therapieoption zur deutlichen Verbesserung der Lebensqualität dar.
Bisher gibt es noch keine direkte Vergleichsstudie zur Wirksamkeit von Biologika und adaptiver Desaktivierung. Eine rezente Metaanalyse aus dem Jahr 2021 analysierte 29 randomisiert kontrollierte Studien bei Patienten mit CRSwNP, die den Effekt der Biologika Dupilumab, Omalizumab, Mepolizumab, Benralizumab, Etokimab und AK001 mit dem der adaptiven Desaktivierung verglichen. Der größte Benefit hinsichtlich Wirksamkeit (Reduktion der Polypengröße, Verbesserung des Riechvermögens und der Lebensqualität) konnte unter Dupilumab erreicht werden, gefolgt von Omalizumab, Mepolizumab und der adaptiven Desaktivierung. Eine Verbesserung der ASS-Intoleranz konnte bisher nur mit der adaptiven Desaktivierung und dem Biologikum Omalizumab erzielt werden.8, 9 Hinsichtlich des Nebenwirkungsprofils sind moderne Biologika der adaptiven Desaktivierung deutlich überlegen.9
Omalizumab: Der humanisierte monoklonale Anti-IgE-Antikörper Omalizumab ist seit 2005 für die Behandlung von allergischem IgE-vermitteltem Asthma und seit 2020 für die Behandlung der CRSwNP zugelassen. In zwei Phase-III-Studien (POLYP-1 und POLYP-2) konnte eine klinisch relevante Reduktion der Polypengröße sowie eine signifikante Verbesserung der subjektiven nasalen Obstruktion und des Riechvermögens festgestellt werden.10 Omalizumab bindet freies IgE und blockiert dadurch die Fortleitung der Typ-2-Entzündungskaskade an Mastzellen und basophilen Granulozyten. Das Nebenwirkungsspektrum ist gering und umfasst vor allem Kopfschmerzen, Reaktionen an der Injektionsstelle und Arthralgien.10 In einer kürzlich von uns durchgeführten Studie mit 33 N-ERD-Patienten konnten wir zeigen, dass Omalizumab neben einer Verbesserung des Asthmas und einer Reduktion der Polypengröße zusätzlich eine ASS-Toleranz induzieren kann.11, 12 Die Hemmung von IgE kann daher in Zukunft eine vielversprechende Behandlungsoption zur Verhinderung von NSAID-Überempfindlichkeitsreaktionen bei Patienten mit N-ERD sein.
Dupilumab – Dermatologen vor allem aus der Therapie der atopischen Dermatitis bekannt – ist ein monoklonaler IL-4a-Rezeptor-Antikörper gegen die gemeinsame Rezeptoruntereinheit der Th2-Zytokine IL-4 und IL-13. Dupilumab erhielt 2019 neben der Zulassung für eosinophiles Asthma auch als erster Antikörper in Europa die Zulassung zur Therapie der CRSwNP. In zwei Phase-III-Zulassungsstudien (LIBERTY NP SINUS-24 und LIBERTY NP SINUS-52) konnte eine signifikante Reduktion der Ausdehnung der nasalen Polypen sowie eine deutliche Verbesserung der subjektiven nasalen Verstopfung, des Riechvermögens und der krankheitsspezifischen Lebensqualität gezeigt werden.13 Bei Patienten mit komorbidem Asthma kam es analog zur nasalen Verbesserung auch zur Reduktion der Asthmasymptomatik. Die Notwendigkeit von systemischen Steroidtherapien oder einer Operation konnte um 74 % bzw. 84 % reduziert werden. Dupilumab zeigt zudem ein günstiges Sicherheitsprofil, das Auftreten von Arthralgien war die häufigste Nebenwirkung.13 Kleine Fallserien speziell bei Patienten mit N-ERD zeigen nicht nur Effizienz in Bezug auf nasale Polyposis und Asthma, sondern auch eine mögliche Toleranzinduktion von ASS unter Dupilumab.14, 15 Die Bestätigung dieser Daten anhand größerer Studien ist derzeit noch ausständig.