Krebsimmuntherapie: Der Schlüssel zur personalisierten Behandlung?
Das Immunsystem fungiert als körpereigene Alarmanlage – mit der Aufgabe, diesen vor eindringenden Pathogenen, Allergenen und Viren zu schützen. Durch die kontinuierliche Überwachung von Immunzellen werden auch geschädigte Zellen, einschließlich Krebszellen, aufgrund von tumorassoziierten Antigenen (TAAs) als fremd identifiziert und eliminiert. Krebszellen können jedoch Mechanismen entwickeln, um der Immunantwort zu entkommen, wobei vier Hauptwege unterschieden werden: die Reduzierung der immunogenen Aktivität durch verringerte Expression von Oberflächenantigenen, die Hochregulierung von Immuncheckpoints zur Unterdrückung der T-Zell-Aktivität, die Schaffung einer immunsuppressiven Krebsumgebung und die Freisetzung von sauren/toxischen Metaboliten, welche die Immunzellen in der Krebsmikroumgebung inaktivieren.1
Konzept und Arten der Krebsimmuntherapie
Die Krebsimmuntherapie zielt darauf ab, das Immunsystem zu stärken oder künstlich hergestellte Immunzellen einzusetzen, um Krebszellen gezielt zu bekämpfen und zu zerstören. Dadurch soll das Wachstum der entarteten Zellen verlangsamt oder gestoppt und die Ausbreitung der Krebszellen auf andere Körperregionen verhindert werden.1, 2
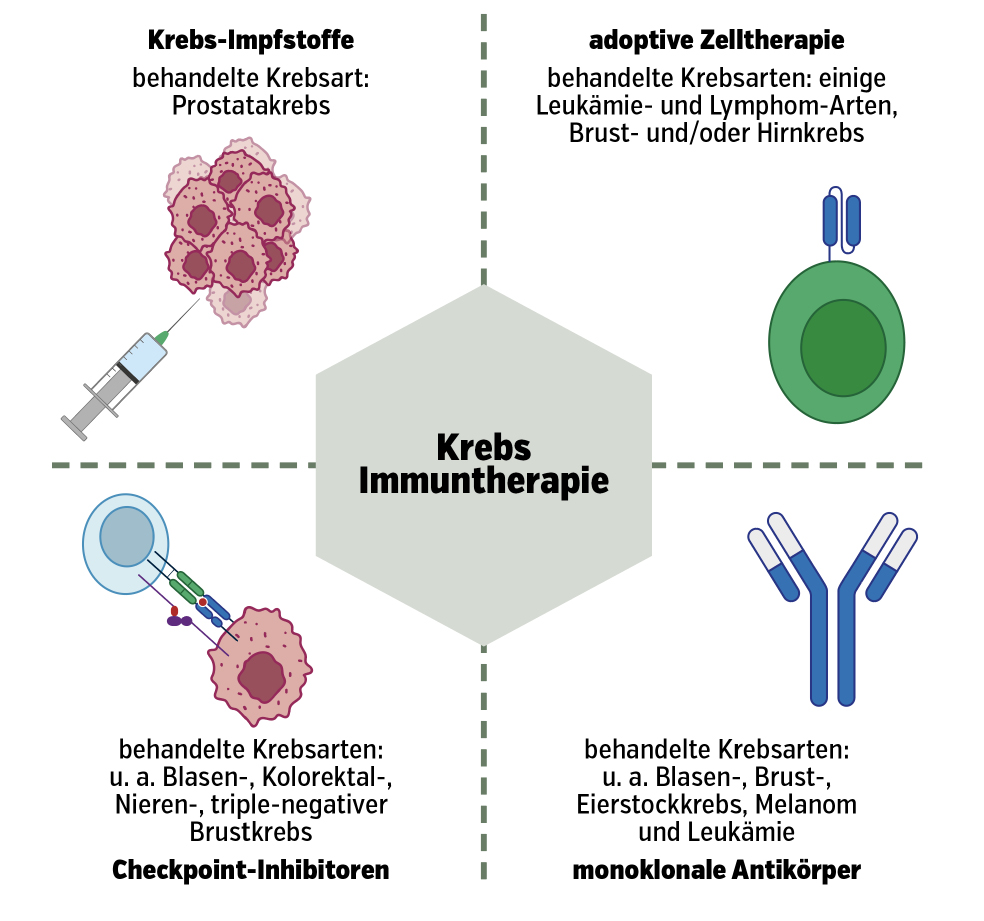
Es gibt 4 Arten der Immuntherapie:
- Checkpoint-Inhibitoren: Checkpoints sind Schlüsselkomponenten des Immunsystems, welche die Aktivierung von T-Zellen regulieren. Im Krebsmikroumfeld sind diese Checkpoints hoch aktiv, was zur Unterdrückung der Immunantwort und damit zur Nichterkennung von Krebszellen durch das körpereigene Immunsystem führt. Checkpoint-Inhibitoren wie beispielsweise Pembrolizumab, Nivolumab (Anti-PD-1) oder Ipilimumab (Anti-CTLA-4) werden eingesetzt, um die Immunantwort zu reaktivieren.1, 3
- adoptive Zelltherapie (ACT): Zur ACT gehören die Therapie mit tumorinfiltrie-renden Lymphozyten sowie die chimäre Antigenrezeptor-CAR-T-Zell-Therapie. Bei dieser Behandlung werden dem/der Patient:in genetisch modifizierte T-Zellen reinfundiert, die einen chimären Antigenrezeptor enthalten. Der Rezeptor erkennt wiederum spezifische Proteine auf Krebszellen, wodurch T-Zellen aktiviert werden. Im Jahr 2018 wurden in Europa erstmals mit Tisagenlecleucel und Axicabtagen-Ciloleucel zwei CAR-T-Zell-Therapien zur Behandlung von Blutkrebsarten wie Leukämie, Lymphom oder multiples Myelom zugelassen.1, 3
- monoklonale Antikörper (mAK): mAKs sind gegen spezifische Antigene auf Krebszellen gerichtet und können entweder nichtkonjugiert oder mit Medikamenten konjugiert sein, die einen zytotoxischen Effekt auf die geschädigten Zellen ausüben. Dazu zählen unter anderem Cetuximab, Panitumumab oder Pertuzumab.1
- Krebsimpfstoffe: Impfstoffe gegen Krebs sollen das Immunsystem anregen, Krebszellen zu erkennen und anzugreifen. Der Impfstoff Sipuleucel-T ist beispielsweise zur Behandlung von Prostatakrebs zugelassen.4
Herausforderungen
Obwohl die Immuntherapie bereits erfolgreich zur Behandlung verschiedener Krebsarten eingesetzt wird, sind damit zahlreiche Herausforderungen verbunden: So bringt die Therapie beispielsweise häufig immunassoziierte Nebenwirkungen mit sich, die sämtliche Organe des Körpers betreffen können. Zudem können Krebszellen durch die Hochregulierung alternativer Kontrollpunkte oder die Aktivierung immunsuppressiver Signalwege Resistenzen gegenüber der Immuntherapie entwickeln. Darüber hinaus ist die Immuntherapie eine kostspielige Behandlungsmethode, was den Zugang für Patient:innen zum Teil erschwert.5, 6
Fazit
Der Hauptvorteil der Immuntherapie ist ihr Potenzial zur Personalisierung. Da das Immunsystem stark individualisiert ist, kann die Wirksamkeit der Immuntherapie von Person zu Person variieren. Fortschritte im Verständnis des Immunsystems, der Tumorbiologie sowie die Identifikation von spezifischen Tumormarkern und Antigenen haben den Weg in Richtung personalisierte Immuntherapie mit geebnet.7 Die Identifikation weiterer Biomarker (analog zu PD-L1), die Indikatoren für das Ansprechen auf die Therapie darstellen, ist jedenfalls von entscheidender Bedeutung, um eine personalisierte Behandlung zu ermöglichen. Außerdem stellt die Komplexität von personalisierten Ansätzen aktuell eine Herausforderung dar. Insgesamt kann die Immunkrebstherapie aber durch ihre Fähigkeit, individuell auf Patient:innen abgestimmt zu werden, als ein zentraler Bestandteil von personalisierter Medizin betrachtet werden.