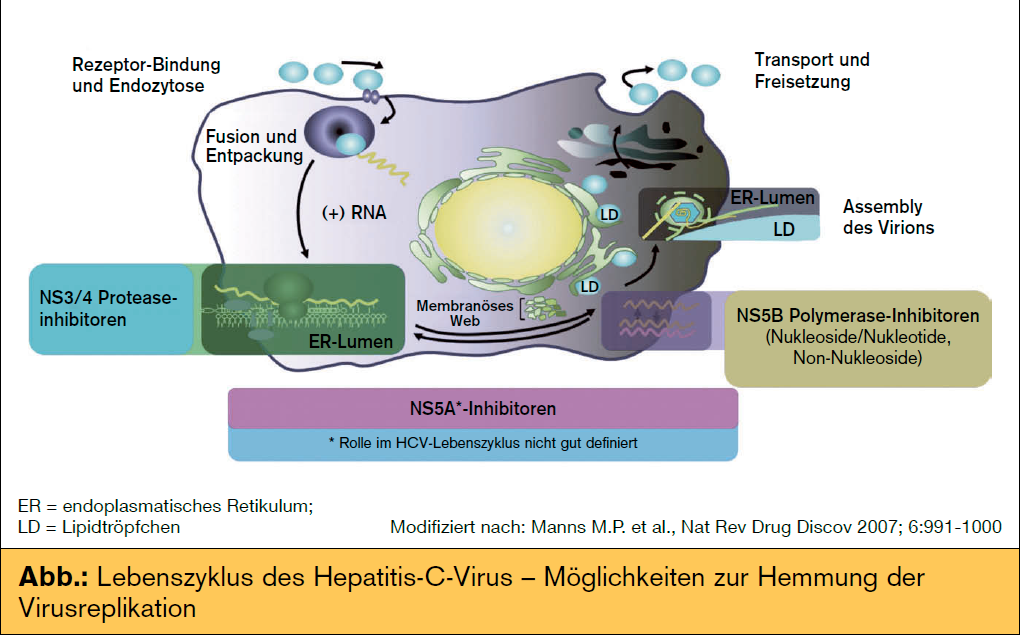
Interferonfreie Therapie der chronischen Hepatitis C – Gesucht wird: einfach, kurz und nebenwirkungsarm
Ein weiteres Problem der Tripeltherapie sind die komplexen Therapiealgorithmen und die engmaschigen Kontrollen während der Therapie. Außerdem ist die Tripeltherapie nur für Patienten, die mit dem Genotyp 1 infiziert sind, zugelassen. Daher besteht der Wunsch nach einer simplen, für alle Genotypen wirksamen, möglichst kurzen und nebenwirkungsarmen Therapie.
INFORM-1: Die erste „Proof of Concept“-Studie (INFORM-1) wurde vor 3 Jahren erstmals vorgestellt. Tatsächlich gelang es, mit zwei DAA (dem Proteasehemmer Danoprevir und dem RnA-Polymerasehemmer Mericitabine) innerhalb von 14 Tagen fast bei allen Patienten die HCV-RnA unter die nachweisgrenze zu bringen. Während dieser 2 Wochen wurden keine Virusmutationen beobachtet. In einer Phase- IIb-Studie mit diesem Therapiekonzept konnte nach einer 24-wöchigen Behandlung nur bei einer bescheidenen Zahl der Patienten eine Dauerheilung erzielt werden. Das große Problem war bei den Patienten mit Genotyp 1a die hohe Zahl von Virusmutationen.
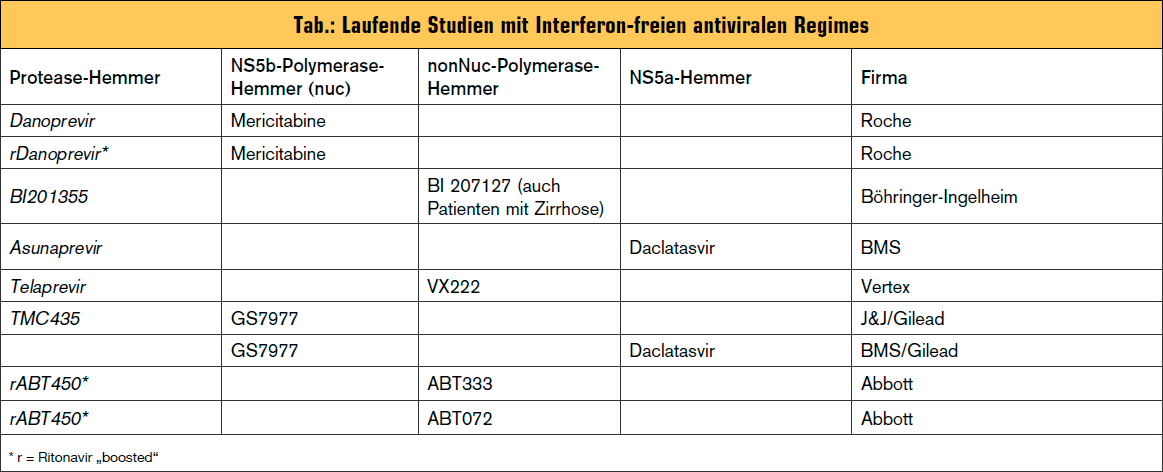
Seit dieser Studie sind mehrere Konzerne in diesen Wettbewerb eingestiegen und momentan geht es mehr um die Aktienkurse als um das Wohl der Patienten. Gemeinsam für alle bisher präsentierten Studiendaten ist die extrem kleine Fallzahl, eine Therapiedauer von 12–24 Wochen, SVR-Raten von > 90 %, das Fehlen signifikanter Nebenwirkungen und die Bedeutung der Therapieadhärenz. Eine – keineswegs vollständige – Liste der derzeit beforschten Medikamentenkombinationen wird in der Tab. präsentiert.
GS7977: Dieses Medikament hemmt die RnAPolymerase (nS5b). Es wurde von der Fa. Pharmaset entwickelt. Beim US-Leberkongress im November 2011 wurden die ersten Daten bei Patienten mit dem Genotyp 2 und 3 vorgestellt. 10/10 der Patienten, die GS7977 (1 Tablette zu 400 mg tgl.) und RBV erhielten, erreichten eine SVR (= Heilung) nach 12-wöchiger Therapie. Diese Daten haben die Firma Gilead bewogen, Pharmaset um 11,6 Milliarden Dollar zu kaufen.
Etwas weniger günstig waren die Daten bei GT1-Nullrespondern, aber immerhin konnten fast 90 % Heilungsraten erzielt werden. Die Therapie war praktisch frei von Nebenwirkungen. Abgesehen von der guten Verträglichkeit hat das Medikament eine hohe genetische Barriere, das heißt, es führt zu keinen Virusmutationen. Weiters ist GS7977 gegen alle Virusgenotypen wirksam. Derzeit wird GS7977in allen möglichen Kombinationen untersucht. Am weitesten fortgeschritten ist die Phase-III-Studie bei Genotyp-3-Patienten. Für diese Subgruppen könnte bereits nächstes Jahr eine Zulassung erfolgen.
Daclatasvir: Dieses Medikament ist ein nS5a- Hemmer. Die genetische Barriere ist niedrig. In einer kleinen Studie aus Japan wurden 10 Nullresponder mit Genotyp 1b mit einer Kombination von Daclatasvir und Asunaprevir (ein Proteaseinhibitor) behandelt. 9/10 Patienten konnten mit einer 24-wöchigen Therapie geheilt werden. Der 10. Patient beendete nach 2 Wochen die Therapie wegen nebenwirkungen, blieb aber HCV-RnA negativ. Patienten mit Genotyp 1a hatten eine hohe Virus- Mutationsrate, die jedoch durch Zugabe von pegIFn/RBV kompensiert wurde.
Bi 207127: Diese Medikament ist ein nichtnukleosidischer Polymerasehemmer und wird mit dem Proteasehemmer BI210355 kombiniert (SOUnD-2 Studie). Dies ist die einzige Studie mit einer großen Fallzahl und es wurden auch Patienten mit Leberzirrhose eingeschlossen. Wiederum schnitten Patienten mit Genotyp 1b (70–80 % SVR) besser als jene mit Genotyp 1a (35–45 % SVR) ab.
ZUSAMMENFASSUNG: Der Wunsch nach einer einfachen, kurzen, nebenwirkungsarmen Therapie der chronischen Hepatitis C rückt in die nähe. Wann diese Therapien verfügbar sein werden, lässt sich heute noch nicht voraussagen. Ebenso nicht, ob Interferon und/oder Ribavirin in der Zukunft noch nötig sein werden. Auf Grund der sehr kleinen Fallzahlen ist eine medizinische Bewertung noch nicht möglich. Man hat den Eindruck, dass Berichte eher für Investoren als für Ärzte abgefasst werden.