Hormontherapie, Adipositas und Brustkrebsrisiko
Zwar können Pflanzenextrakte leichtere klimakterische Beschwerden bessern – die meisten der Extrakte enthalten Phytoöstrogene, also östrogenwirksame Substanzen –, allerdings ist bei Vorliegen von gravierenden Östrogenmangelsymptomen eine Hormonsubstitution aus therapeutischen Gründen indiziert. In jedem Fall sind die Patientinnen im Rahmen des ärztlichen Gespräches einerseits ausführlich über die Auswirkungen eines Östrogenmangels und über die verschiedenen therapeutischen Möglichkeiten aufzuklären, andererseits aber auch über die Risiken einer Hormonersatztherapie (HRT).
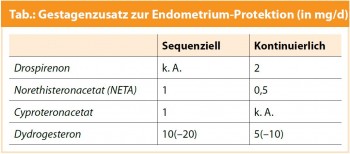
Welche Hormone, welche Schemata? In der Prämenopause sind – bei unzureichender oder fehlender Corpus-luteum- Funktion – die Östrogenspiegel relativ erhöht. Somit empfiehlt sich eine zyklische Gestagengabe zur Verhinderung einer Endometriumhyperplasie, wobei diese Substitution in adäquater Dosierung über mindestens 12 Tage pro Monat durchgeführt werden sollte. Im Allgemeinen reicht bei niedrigen Östrogendosen ein geringer Gestagenzusatz zur Protektion des Endometriums (Tab.).
Zur Östrogentherapie sind 17β-Östradiol (E2) bzw. dessen Ester sowie konjugierte equine Östrogene (CEE) geeignet, wobei die HRT mit einer möglichst niedrigen Östrogendosis begonnen und bei Bedarf angepasst werden sollte. In diesem Zusammenhang ist anzumerken, dass Östriol (E3) in üblicher Dosierung keine (bzw. nur eine geringe) proliferative Wirkung auf das Endometrium hat, womit bei E3-Medikation keine zusätzliche Gestagenmedikation notwendig ist. Da keine systemische Wirkung gegeben ist, bestehen naturgemäß auch keine positiven Effekte auf Knochen- und Fettstoffwechsel.
Ethinylestradiol (EE) als Inhaltsstoff fast aller hormonellen Kontrazeptiva ist wegen seiner starken hepatischen Wirkung und der damit verbundenen ungünstigen Nebenwirkungen zur HRT nicht zu empfehlen. Bezogen auf Hitzewallungen ist EE außerdem weniger wirksam als E2, deshalb können in der Perimenopause auch unter der Einnahme von Ovulationshemmern durchaus klimakterische Beschwerden auftreten.
Übergewicht, metabolisches Syndrom, Hyperinsulinämie und Mammakarzinomrisiko: Im Hinblick auf die Bewertung der modifizierbaren Risikofaktoren für das Mammakarzinom sind die folgenden Ergebnisse epidemiologischer und endokrinologischer Untersuchungen von Bedeutung:
- Die große Collaborative Re-Analyse von 1997 sowie die Nurses’ Health Study und eine Studie der amerikanischen Krebsgesellschaft stellten übereinstimmend fest, dass Übergewicht bei postmenopausalen Frauen das Brustkrebsrisiko erhöht.
- Eine Querschnittstudie der WHI (mit 86.000 Frauen) ergab, dass bei adipösen Frauen ohne HRT das Brustkrebsrisiko um 150 % erhöht ist, in der Altersgruppe von 50–69 Jahren sogar um mehr als 350 %. Die Studie ergab keine weitere Erhöhung durch Vornahme einer HRT, sondern tendenziell sogar eine Abnahme.
- Eine HRT steigerte das Risiko für Mammakarzinom nur bei postmenopausalen Frauen mit Normalgewicht (BMI < 25 kg/m2). Entsprechend der Datenlage hängt das Ergebnis von wissenschaftlichen Studien über den Einfluss einer HRT auf das Brustkrebsrisiko vom Prozentsatz übergewichtiger Frauen in der Studienpopulation ab. Je mehr Frauen übergewichtig oder adipös sind, umso niedriger ist das relative Gesamtrisiko bei den mit Hormonen behandelten Frauen. Bei unbehandelten adipösen Frauen ist das Risiko gleich hoch bzw. sogar höher als bei adipösen Frauen mit HRT.
- In der randomisierten, placebokontrollierten WHI-Studie reduzierte die Monotherapie mit konjugierten Östrogenen bei Frauen, die mindestens 80 % der Medikation eingenommen hatten, das Brustkrebsrisiko signifikant um 33 %. Die Ursache dieses überraschenden Ergebnisses hängt mit großer Wahrscheinlichkeit damit zusammen, dass 34,8 % der teilnehmenden Frauen übergewichtig und weitere 44,6 % adipös waren.
- Im Gegensatz zu postmenopausalen Frauen ist bei übergewichtigen Frauen in der Prämenopause das Brustkrebsrisi ko nicht erhöht, es steigt erst nach der Menopause an. Dies ist ein Hinweis darauf, dass die endogenen Östrogene einen protektiven Effekt gegenüber den Auswirkungen einer zentralen Adipositas haben.
- Eine prospektive Studie der amerikanischen National Institutes of Health (NIH) ergab, dass eine Gewichtszunahme ab dem 18. Lebensjahr das Brustkrebsrisiko in der Postmenopause erhöht, wobei diese Risikozunahme mit dem Ausmaß der Gewichtszunahme korreliert. Bei diesen Frauen verhinderte eine Hormonsubstitution den Anstieg des Mammakarzinomrisikos.
- In der WHI-Studie erhöhte die Östrogen-Gestagen-Therapie (CEE/Medroxyprogesteronacetat) das Brustkrebsrisiko nur bei Frauen, die vor Studienbeginn mit einer HRT behandelt worden waren. Allerdings beruhte diese Risikozunahme auf dem Umstand, dass in der HRT-vorbehandelten Placebogruppe der normale altersabhängige Anstieg des Brustkrebsrisikos ausblieb. Im Gegensatz dazu beobachtete man bei den nicht-vorbehandelten Frauen in der Placebogruppe über die Beobachtungszeit von 7 Jahren einen Anstieg, der mit jenem in der Hormongruppe vergleichbar war.
- Eine zentrale Adipositas ist ein wichtiges Kriterium für das metabolische Syndrom, das u. a. mit einem hohen Risiko für Insulinresistenz und chronischer Hyperinsulinämie verbunden ist. Die chronische Hyperinsulinämie bedeutet ein erhebliches Krebsrisiko, da Insulin direkt die Karzinogenese stimuliert.
Bei postmenopausalen Frauen mit therapiertem Mammakarzinom erhöht ein metabolisches Syndrom das Rezidivrisiko auf das Dreifache. Bei den Patientinnen mit den höchsten Insulinspiegeln ist das Risiko für Fernmetastasen verdoppelt und die Mortalität verdreifacht. - Bei gesunden postmenopausalen Frauen reduziert eine Monotherapie mit E2 (ERT) den Insulinspiegel und den HOMA-Index um 30–40 %. Eine ERT hat einen günstigen Einfluss auf den Kohlenhydratstoffwechsel und reduziert das Risiko für Diabetes Typ 2. Bei postmenopausalen Frauen mit Hyperinsulinämie ist das Brustkrebsrisiko erhöht, wird aber durch Östrogen-Monotherapie reduziert.
- Körperliche Aktivität reduziert das Brustkrebsrisiko in der Postmenopause um 20–40 % und verbessert bei Brustkrebspatientinnen die Prognose.
- Eine Metformintherapie reduziert bei Frauen mit Brustkrebs im Frühstadium einen erhöhten Insulinspiegel und den HOMA-Index um 22–25 %. Eine 5-jährige Metformintherapie reduziert bei Frauen mit Diabetes Typ 2 das Krebsrisiko um 44 %.
ZUSAMMENFASSEND ist der Schluss zulässig, dass Östrogenmangel zur Insulinresistenz mit chronischer Hyperinsulinämie führen kann, die sich durch Östrogentherapie reduzieren bzw. oder beseitigen lässt. Alle Maßnahmen, die zu einer Besserung der Insulinresistenz führen, bedeuten eine Möglichkeit, das Risiko für Malignome und insbesondere für Mammakarzinome bei postmenopausalen Frauen zu reduzieren. Dazu zählen eine niedrig dosierte Östrogentherapie sowie die Reduktion des Gewichts bzw. der zentralen Fettmasse durch körperliche Aktivität, Verringerung der Kalorienaufnahme bzw. durch Metformintherapie.
Quellen: auszugsweise Wiedergabe von Ergebnissen des 45. Arbeitstreffens des „Zürcher Gesprächskreises“/Dezember 2010 bzw. Präsentationen im Rahmen des Menopause-Kongresses, Wien/Dezember 2011