Sympathikusblockade als zentrale Therapieoption bei Hypertonie und Endorganschäden
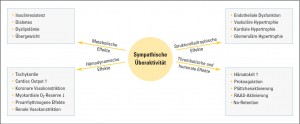
Die Bedeutung der Sympathikusaktivierung in der kurzfristigen Kontrolle des arteriellen Blutdrucks, aber auch für die Entstehung und den Fortbestand einer essenziellen Hypertonie, ist unbestritten.1 Ebenso spielt sie bei kardiovaskulären (z. B. Herzinsuffizienz, Arrhythmien, Myokardinfarkt und ischämischen Schlaganfällen) und renalen Erkrankungen eine besondere Rolle. Auch bei metabolischen Veränderungen (z. B. metabolisches Syndrom, Adipositas und Diabetes mellitus) ist das adrenerge System aktiviert (Abb.). Bei Patienten mit Nierenerkrankungen aggraviert die sympathische Überaktivität die Progression der renalen Schädigung und das kardiovaskuläre Risiko.
Hypertonie
Bei vielen jungen Hypertonikern kommt es früh im Erkrankungsverlauf zu einem Anstieg des Cardiac Outputs und der Herzfrequenz, begleitet von erhöhten Noradrenalinplasmaspiegeln sowie einer Steigerung der sympathischen Aktivität an periphereren Nerven. 2, 3 Auch bei „Weißkittelhypertonie und maskierter Hypertonie“ sowie bei Patienten mit „reverse dipping“ in der 24-Stunden-Blutdruckmessung ist eine Sympathikusaktivierung nachweisbar. Dies erlaubt den Schluss, dass der sympathischen Überaktivität als Mechanismus für die Entstehung und Aufrechterhaltung einer Hypertonie eine bedeutende Rolle zukommt und dass die Beeinflussung des Sympathikus eine vernünftige Therapieoption in der Behandlung von hypertensiven Patienten mit oder ohne Endorganschäden darstellt. 4
Renale Erkrankungen
Das sympathische Nervensystem stimuliert vaskuläre α 1-adrenerge Rezeptoren und renale β 1-Rezeptoren in juxtaglomerulären Zellen in afferenten Arteriolen, die für eine Steigerung der Reninfreisetzung und Produktion von Angiotensin II verantwortlich sind. Auch eine Aktivierung des Renin-Angiotensin- Aldosteron-Systems (RAAS) steigert die sympathische Aktivität sowohl peripher über eine gesteigerte Noradrenalinfreisetzung in peripheren Nervenendigungen als auch zentral über Stimulation vasomotorischer Zentren des Sympathikus im Hypothalamus.
Die Bedeutung der sympathischen Überaktivität bei renalen Erkrankungen blieb lange Zeit wenig beachtet. Neuere Studien zeigen, dass die sympathische Überaktivität an der Pathogenese der arteriellen Hypertonie bei Nierenpatienten (85% der niereninsuffizienten Patienten sind hyperton) wesentlich beteiligt ist. Die Niere, die von efferenten sympathischen und afferenten sensorischen Fasern innerviert wird, kann auch Ursprung der sympathischen Überaktivität sein (reviewed in [9]) und afferente Signale aussenden, welche Zentren im Hypothalamus stimulieren, die wiederum efferente sympathische Nervenimpulse aussenden. Die Normalisierung der adrenergen Stimuli nach bilateraler Nephrektomie bei Hämodialysepatienten und bei Patienten nach Nierentransplantation macht deutlich, dass die Überaktivität aus den geschädigten Nieren resultiert. Sie ist bereits in der Frühphase einer chronischen Niereninsuffizienz nachweisbar und durch mikroneurographische Studien auch in fortgeschrittenen Stadien belegt.
Unterschiedliche Mechanismen (z. B. akute renale Schädigung, nephrotisches Syndrom oder polyzystische Nierenerkrankung) können zu einer Aktivierung des sympathischen Nervensystems führen. Weitere Faktoren, die bei Nierenpatienten die Überaktivität begünstigen, sind die Aktivierung renaler Chemorezeptoren, die RAAS-Stimulierung oder erhöhte Spiegel von zirkulierendem asymmetrischem Dimethylarginin als Inhibitor der Nitric-Oxide-Synthetase.
Der sympathischen Überaktivität wird eine bedeutende Rolle als Progressionsfaktor der Niereninsuffizienz zugeschrieben. In tierexperimentellen Studien führte sie blutdruckunabhängig zur Progression einer Niereninsuffizienz. Weiters ist die adrenerge Stimulation für das exzessiv erhöhte kardiovaskuläre Risiko renaler Patienten mitverantwortlich.
Kardiovaskuläre Erkrankungen
Die sympathische Überaktivität spielt auch bei kardialen Erkrankungen eine bedeutende Rolle.2
Herzinsuffizienz
Die hohen Norepinephrinplasmaspiegel bei Patienten mit Herzinsuffizienz sind durch eine verminderte Gewebeclearance, aber auch durch ein „Spill-over“ aus sympathischen Nervenendigungen bedingt. Der Grad der Sympathikusaktivität korreliert eng mit dem klinischen Grad der Herzinsuffizienz und einer erhöhten Mortalität.6 Die gesteigerte Sympathikusaktivität führt zu einem Anstieg des intrazellulären Kalziums sowie zur Hypertrophie und Apoptose von Kardiomyozyten.5
Myokardinfarkt
Eine Vielzahl von Studien bestätigt, dass eine sympathische Überaktivität das Auftreten von Myokardinfarkten begünstigt. (reviewed in [7]) Neben hämodynamischen Veränderungen, wie z. B. akuten Blutdruckanstiegen, Steigerung der Herzfrequenz oder Vasokonstriktion besonders in bereits arteriosklerotisch vorgeschädigten Gefäßen, spielen auch prothrombotische Faktoren mit einer erhöhten Thrombozytenaggregation und einer verminderten Fibrinolyse eine kausale Rolle in der Entstehung von myokardialen Ischämien. Gleichzeitig trägt das ischämische Myokard durch zusätzliche Aktivierung des Sympathikotonus und eine Erhöhung des linksventrikulären Füllungsdruckes zu einer Verschlechterung der kardialen Situation bei. Als zusätzliches Problem bestehen die unter Sympathikuseinfluss gesteigerte elektrische Instabilität und die Gefahr von Arrhythmien. Als externe Auslöser einer Aktivierung des Sympathikus gelten unter anderen exzessive körperliche Belastungen, emotionaler Stress, Kälteexposition sowie die Konsumation großer Mengen von Alkohol oder Rauchen.
Metabolische Störungen
Die bei der viszeralen Form der Adipositas nachweisbare sympathische Überaktivität (reviewed in [8]) führt zu Veränderungen der Insulinsensitivität sowie des Blutdrucks. Als Ursachen für die verstärkte adrenerge Aktivität werden das oft mit Adipositas vergesellschaftete Schlaf-Apnoe-Syndrom, eine Hyperinsulinämie (resultierend aus gestörter muskulärer Durchblutung, verminderter peripherer Glukosebereitstellung und Insulinresistenz), erhöhte Spiegel von Leptin (ein aus Fettgewebe freigesetztes Protein) bzw. Störungen des Baroreflex- Mechanismus diskutiert.
Beeinflussung der sympathischen Überaktivität
Lifestyle-Modifikationen
Unter den nicht pharmakologischen Maßnahmen zur Reduktion der sympathischen Überaktivität kommt der Gewichtsreduktion und der regelmäßigen körperlichen Aktivität die größte Bedeutung zu. Die Reduktion des Körpergewichts bewirkt eine Normalisierung der oft gleichzeitig bestehenden metabolischen Veränderungen (Hyperlipidämie, Hyperinsulinämie) und ist mit einem Absinken erhöhter Plasma-Noradrenalin-Werte vergesellschaftet. Unbestritten sind auch die positiven Effekte eines regelmäßigen körperlichen Trainings auf die Reduktion der sympathischen Aktivität.
Medikamentöse Therapie
In den vergangenen Jahren wurden die Effekte unterschiedlicher Klassen von Medikamenten auf die sympathische Nervenaktivität untersucht.10,11
Betarezeptorenblocker: Betablocker senken die Herzfrequenz, den Cardiac Output und den arteriellen Blutdruck und hemmen die intrarenale Reninausschüttung aus juxtaglomerulären Zellen der Macula densa: Vor allem durch Hemmung der Katecholaminwirkung auf kardiale betaadrenerge Rezeptoren wirken sie blutdrucksenkend.
Große kontrollierte Hypertoniestudien, wie z. B. STOP-II, UKPDS-HDS, AASK oder NORDIL, wiesen signifikante Verringerungen der Inzidenz von Myokardinfarkten und Schlaganfällen durch Betablocker nach. Betarezeptorenblocker sind bei Patienten mit tachykarder Herzaktion, Angina pectoris, nach Myokardinfarkt und Herzinsuffizienz indiziert. Weitere Einsatzgebiet der Betablocker sind die Hypertonie in der Schwangerschaft, Vorhofflimmern und rekurrierende Migräne.
Zentral wirksame Sympathikolytika: Die periphere Aktivität des Sympathikus kann auch durch zentral wirksame Sympathikolytika verringert werden. Substanzen, welche die Stimulierung von Alpha-2a-Rezeptoren im zentralen Nervensystem bewirken (z. B. Clonidin), werden wegen der häufig auftretenden Nebenwirkungen (Mundtrockenheit, Müdigkeit, Depression) nur mehr selten eingesetzt und wurden im klinischen Einsatz durch selektive I1-Imidazolin-Rezeptoragonisten (z. B. Rilmenidin, Moxonidin) mit einer ebenso effektiven Blutdrucksenkung abgelöst. Zentral wirksame Sympathikolytika stellen wichtige Kombinationspartner in der Hypertoniebehandlung dar.
Alpha-1-Rezeptorenblocker: Alphablocker blockieren die postsynaptischen Alpha-1-Rezeptoren im postganglionären sympathischen Neuron. Weiters hemmen sie die durch endogene Katecholamine induzierte Vasokonstriktion der arteriellen Widerstandsgefäße (Arteriolen) und Venen und senken den peripheren Widerstand. Aufgrund des Fehlens von Endpunktstudien für die Verhinderung kardiovaskulärer Ereignisse werden Alphablocker nicht als Mittel der ersten Wahl in der Hypertonietherapie gesehen. Sie eignen sich für den Einsatz bei älteren hypertensiven Männern aufgrund ihrer positiven Wirkungen bei Prostatahypertrophie (Alpha-1-Rezeptoren befinden sich auch an der glatten Muskulatur des Blasenhalses) bzw. als Kombinationspartner in der Therapie schwerer Hypertonieformen.
ACE-Hemmer: ACE-Hemmer reduzieren wie andere RAAS-Hemmer eine sympathische Überaktivität. Ihre Wirkungen wurden in vielen kontrollierten Studien (z. B. STOP II, SOLVD, CAPPP, HOPE, ALLHAT, PROGRESS, QUIET, AASK, ANBP2, ABCD, ONTARGET, ACCOMPLISH) untersucht. Sie sind Mittel der ersten Wahl für die Behandlung von Patienten mit chronischer Herzinsuffizienz, für Patienten mit eingeschränkter Ventrikelfunktion nach Myokardinfarkt, Patienten mit hohem kardiovaskulärem Risiko und/oder eingeschränkter Nierenfunktion bzw. Proteinurie.
Angiotensin-Rezeptorblocker: Die Wirkweise der AT1-Rezeptorblocker beruht auf der Hemmung der über den AT1-Rezeptor vermittelten Wirkungen von Angiotensin II. Bei Patienten mit Herzinsuffizienz, bei Hypertonikern mit erhöhtem kardiovaskulärem Risiko (z. B. linksventrikuläre Hypertrophie), bei Patienten mit akutem Schlaganfall oder mit renalen Erkrankungen weisen sie eine gute Effektivität auf, wie in großen Studien (z. B. OPTIMAAL, RESOLVD, ELITE II, Val-HeFt, SCOPE, CHARM, ACCESS, VALUE, LIFE, IDNT, RENAAL, ONTARGET) gezeigt wurde.
Renininhibitoren: In Analogie zu ACE-Hemmern und AT1- Rezeptorblockern ist auch für Renininhibitoren ein positiver Effekt auf die Verringerung der sympathischen Aktivität anzunehmen. Endpunktstudien für diese Substanzklasse werden derzeit durchgeführt.
Nicht medikamentöse Therapiemöglichkeiten: Durch neue technische Entwicklungen und interventionelle Therapiestrategien, wie z. B. die renale Sympathikusdenervierung oder Barorezeptorstimulation, ist es nun auch mit nicht medikamentösen Interventionen möglich, die Sympathikusaktivität zu beeinflussen. Über diese Therapieverfahren wird an anderer Stelle in diesem Heft berichtet.
1 Corti R et al., News Physiol Sci 2000; 15:125–129
2 Grassi G et al., J Nephrol 2009; 22:190–195
3 Grassi G et al., J Hypertens 1999; 17:719–734
4 Grassi G, Curr Hypertens Rep 2003; 5:277–280
5 Adams KF Jr, Am J Health Syst Pharm 2004; 61(Suppl 2):S4–13
6 Brunner-La Rocca HP et al., Eur Heart J 2001; 22:1136–1143
7 Culic V, Int J Cardiol 2007; 117:260–269
8 Esler M et al., Hypertension 2006; 48:787–796
9 Habicht A et al., Wien Klin Wochenschr 2003; in press
10 de Champlain J, Curr Hypertens Rep 2001; 3:305–313 11Wenzel RR et al., J Cardiovasc Pharmacol 2000; 35:S43–52
NEPHRO Spot
Der sympathischen Überaktivität kommt für die Entwicklung und das Fortbestehen einer Hypertonie sowie bei kardiovaskulären und renalen Erkrankungen und bei metabolischen Veränderungen eine wichtige Rolle zu. Eine Sympathikusblockade durch medikamentöse oder mittlerweise auch interventionelle Therapieformen stellt für eine Vielzahl von Patienten mit Hypertonie, metabolischen, kardialen oder renalen Problemen eine sinnvolle Therapieoption dar.