Alpha-1-Antitrypsin-Mangel – Risiko für Lunge und Leber
Pathophysiologie
Alpha-1-Antitrypsin (AAT) ist ein Akute-Phase-Protein, das im Rahmen von Infektionen vermehrt gebildet wird und als Proteinase-Inhibitor eine gewebeschützende Funktion einnimmt: Es neutralisiert die bei einer Inflammation freigesetzten proteolytischen Enzyme, allen voran die von neutrophilen Granulozyten ausgeschüttete Elastase. Diese übernimmt im Rahmen einer Entzündungsreaktion im Bereich der Atemwege die Aufgabe, bakterielle Proteine durch einen proteolytischen Abbau zu zersetzen. Bei einem Mangel an AAT kommt es zu einer Dysbalance im Zusammenspiel von Proteinasen und Antiproteinasen, und es wird gesundes Lungengewebe geschädigt. Als langfristige Folge entsteht ein (meist panazinäres) Emphysem.
Klinik
Die klinische Ausprägung der Erkrankung ist vom Genotyp und vom Serumspiegel abhängig. Sie reicht von Symptomfreiheit bis zu schweren Lungen- und Lebererkrankungen. Eine pulmonale Symptomatik beginnt meist unspezifisch mit Dyspnoe, Husten und Auswurf und kann bis zur Entwicklung eines schweren Lungenemphysems fortschreiten. Wegen der geringen Spezifität der Beschwerden wird die Diagnose erst nach 4 bis 8 Jahren gestellt. In einer retrospektiven Analyse der Daten aus dem österreichischen Register betrug der durchschnittliche Delay 5,3 Jahre.
Bei hepatischer Beteiligung können bereits im Neugeborenenalter ein prolongierter Ikterus oder eine Erhöhung der Lebertransaminasen bis hin zum klinischen Bild einer Hepatitis auftreten. Im Verlauf sind sowohl eine vollständige Ausheilung als auch die frühe Entstehung einer Leberzirrhose möglich. In der Literatur beschrieben wird auch, dass Patient:innen, die in der Kindheit keine Leberauffälligkeiten zeigten, mit einem AAT-Mangel-Genotyp PiZZ im Erwachsenenalter ein erhöhtes Risiko für die Entwicklung einer Leberzirrhose und eines hepatozellulären Karzinoms haben.
Prinzipiell kann bei AAT-Mangel gleichzeitig eine Leber- und Lungenbeteiligung auftreten, das Vollbild der Erkrankung sowohl mit schwerem Lungenemphysem als auch mit einer Leberzirrhose ist allerdings selten.
Assoziiert mit einem AAT-Mangel kann in seltenen Fällen auch eine nekrotisierende Pannikulitis und sekundäre Vaskulitis sein.
Diagnostik
Der AAT-Mangel wird bei weitem zu selten diagnostiziert. Grund ist die hohe Variabilität in der Symptomausprägung: Diese reicht von respiratorischen Symptomen einer obstruktiven Lungenerkrankung bis zu gänzlich asymptomatischen Verläufen. Jede:r Pa-tient:in mit COPD sollte daher – ungeachtet des Alters – auf einen AAT-Mangel getestet werden. Dies gilt ebenso für Patient:innen mit einer kryptogenen Lebererkrankung, nekrotisierenden Pannikulitis und c-ANCA-positiver Vaskulitis.
Bei gesicherter Diagnose wird ein Screening der Familienmitglieder empfohlen.
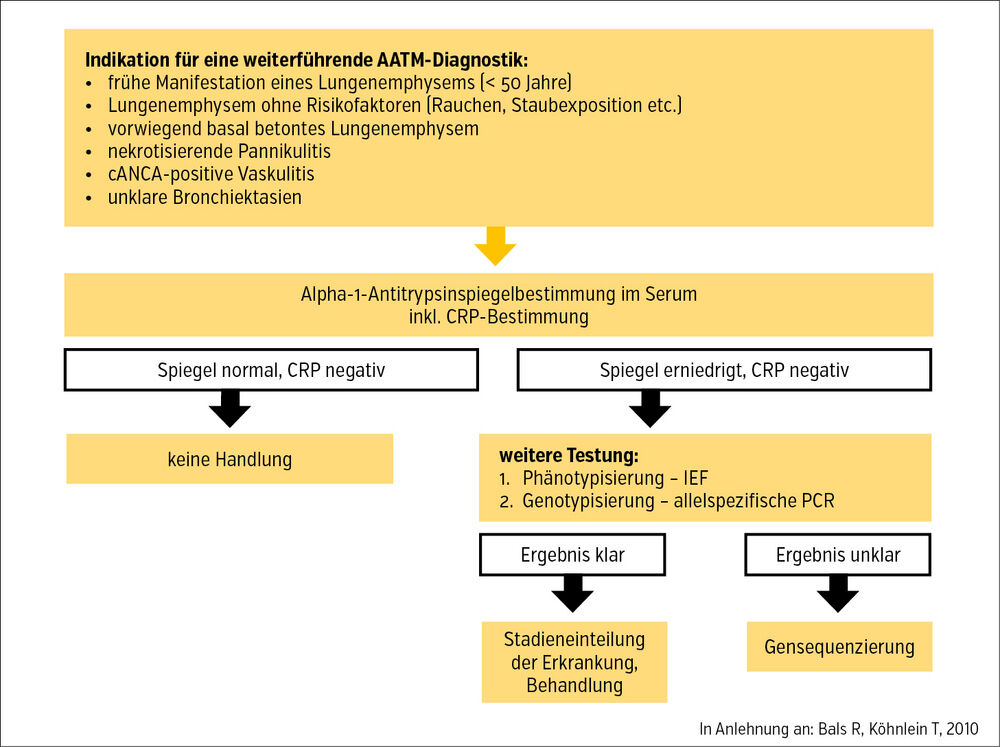
Zur Testung gehört initial die Bestimmung des Serumspiegels. Da es sich bei AAT um ein Akute-Phase-Protein handelt, kann der Serumspiegel bei Entzündungen erhöht sein. Es soll daher gleichzeitig eine Bestimmung des CRP erfolgen. Bei erniedrigtem oder im unteren Normbereich liegendem Serumspiegel (<100 mg/dl) von AAT müssen weitere genetische Untersuchungen eingeleitet werden: die Phänotypisierung mittels isoelektrischer Fokussierung (IEF) und Genotypisierung mittels PCR. Bei Verdacht auf eine seltene Mutation, d. h. bei unschlüssigen Befundkonstellationen, ist eine Gensequenzierung notwendig (Abb.).
Nach Diagnosesicherung erfolgt eine umfassende erste klinische, funktionelle und radiologische Evaluierung.
Therapie
Die Behandlung des AAT-Mangels mit Lungenbeteiligung folgt einem multimodalen Konzept, das sich im Wesentlichen nicht von den Empfehlungen für COPD unterscheidet. Unumgänglich ist der komplette Rauchstopp bzw. das Schaffen einer rauch- und staubfreien Umgebung. Dazu gehört ggf. auch eine berufliche Umorientierung.
Ist eine Lungenfunktionseinschränkung bereits manifestiert, kann bei klinisch relevanten Mangelvarianten (PiZZ, PiSZ, PiZ0, Pi00) eine Augmentationstherapie eingeleitet werden. Diese besteht in einer einmal wöchentlichen intravenösen Gabe von hochgereinigtem AAT. Ziel dabei ist es, den Serumspiegel über die „protektive Schwelle“ (> 80 mg/dl) anzuheben, um eine fortschreitende Lungenzerstörung hintanzustellen.
Die Indikation zur Therapie muss durch ein Kompetenzzentrum für AAT gestellt werden. Hier erfolgt auch die Aufnahme der Patient:innen in das nationale und europäische Register.
Sind alle Therapiemöglichkeiten ausgeschöpft, wird bei geeigneten Patient:innen eine Lungentransplantation angestrebt.