COPD: Neues zur Klassifikation und Therapie
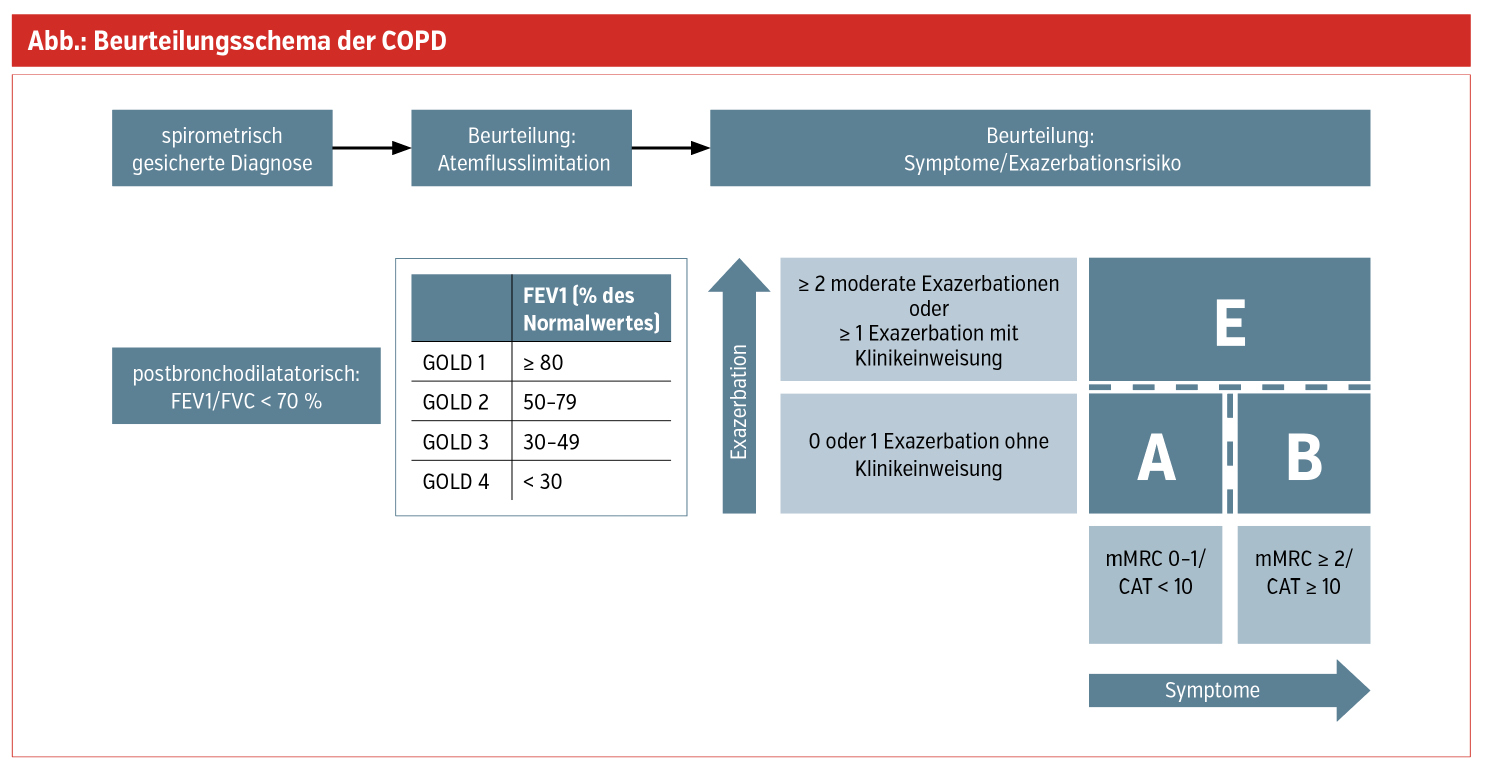
Die chronisch obstruktive Lungenerkrankung (COPD) wurde zunächst anhand der Klinik und der Lungenfunktionseinschränkungen klassifiziert und in Schweregrade nach GOLD (Global Initiative for Chronic Obstructive Lung Disease) von 1 bis 4 systematisiert und eingeteilt. Die Diagnose COPD wird lungenfunktionell definiert als Atemwegsobstruktion (FEV1/FVC < 70 %) nach medikamentöser Bronchodilatation. Im Rahmen des GOLD-Updates von 2011 erfolgte eine wichtige Erweiterung mit Einarbeitung der von Patient:innen berichteten Beschwerden (mMRC und CAT) und auch der Anzahl und des Schweregrads der Exazerbationen. Diese Parameter wurden in einer 4-Felder-Tafel als „ABCD“-Gruppen kategorisiert. In der nun erschienenen GOLD-Edition von 2023 werden die Gruppen A (wenig Symptome) und B (mehr Symptome) übernommen.
Einen besonderen Stellenwert in den neuen GOLD-Leitlinien hat die COPD-Exazerbation. Hierunter versteht man eine akute Zunahme der vorbestehenden respiratorischen Symptome, oftmals mit einer lokalen wie systemischen Inflammation. Große Studien zeigten den Einfluss der COPD-Exazerbation auf die Verschlechterung der Erkrankung, den Abfall der Lungenfunktion und eine Verschlechterung der Erkrankungsprognose. Die Gruppen C und D (die „Viel-Exazerbierer“) werden nun als E in der neuen „ABE“-3-Felder-Tafel zusammengefasst (siehe Abb.). Diese Zusammenlegung von C und D unterstreicht besonders die Relevanz der Exazerbationen für die Patientenprognose und vereinfacht die klinische Einteilung.
Neben den obengenannten subsumiert die COPD sehr heterogene Krankheitsbilder, die sich ätiologisch und klinisch voneinander unterscheiden. Daher wird aktuell über eine neue Nomenklatur für die unterschiedlichen Ätiologien der COPD nachgedacht:
- COPD-A – steht für COPD mit (kindlichem) Asthma
- COPD-G – genetisch determinierte Form (Alpha-1-Antitrypsin-Mangel AATD/u. ä.)
- COPD-C – durch Zigaretten bzw. inhalative Noxen induziert
- COPD-P – durch Umweltbelastung
- COPD-I – durch Infektion
- COPD-D aufgrund von pulmonalen Entwicklungsstörungen
- COPD-U – durch unbekannte Ursachen
Diese neue Taxonomie hat derzeit noch keine direkte Konsequenz, es zeigt allerdings auch die Heterogenität der Einflussfaktoren beziehungsweise Trigger-Faktoren für die Erkrankung.
Pharmakotherapie
Die Grundlage der COPD-Therapie stellt die Bronchodilatation da. Das bedeutet für Patient:innen mit wenig Symptomen in der GOLD-Gruppe A die Einleitung einer bronchienerweiternden Mono-Therapie (kurz- oder langwirksam). Patient:innen ab der Gruppe B – mit stärkeren klinischen Symptomen – wird nun nicht mehr eine Auswahl zwischen LAMA (langwirksamer Muskarinantagonist) oder LABA (langwirksamer Beta-2-Agonist) empfohlen, sondern direkt eine Therapie mit einer Kombination aus LAMA und LABA. Damit bekommen diese Patientenkollektive eine starke Basisbronchodilatation, die auf der Kombination der beiden Wirkmechanismen basiert.
In der neuen Gruppe E wird grundlegend eine Therapie mit LAMA und LABA empfohlen. Der zusätzliche Einsatz von inhalativen Kortikosteroiden (ICS) in der Gruppe E erfolgt, wenn Eosinophilenzahlen (EOS) ≥ 300 vorliegen, auch kann bei EOS ≥ 100 von einer LAMA/LABA-Kombination auf eine Triple-Kombination bei klinischer Indikation erweitert werden, wobei eine Single-Inhalator-Therapie gegenüber einer Kombination unterschiedlicher Inhalatoren bevorzugt werden sollte. Der Wechsel von Monobronchodilatation auf eine LABA+ICS-Kombination wird hingegen nicht mehr empfohlen.
Nichtpharmakologische Therapien
Neben den bekannten pharmakologischen Therapien sollten den Patient:innen auch nichtpharmakologische Therapien nahegebracht werden. Hierbei ist die Rauchentwöhnung ein wichtiger Ansatz, insbesondere in den Frühstadien. Es gibt verschiedene Angebote von stationären Möglichkeiten im Rahmen der Rehabilitation bis hin zu web- und telefonbasierten Programmen (zum Beispiel das „Rauchertelefon“). Auch ist die pneumologische Rehabilitation mit einem signifikanten Effekt auf die Mortalität der Patient:innen ein wichtiger Baustein in der COPD-Therapie.
Auch die Langzeitsauerstofftherapie kann (bei Hypoxämien < 55 mmHg) verordnet werden, individuell angepasste nichtinvasive Beatmungstherapien können ebenfalls Besserung bringen. Andere interventionelle Maßnahmen wie bronchoskopische Lungenvolumenreduktion und andere chirurgische Optionen bis zur Lungentransplantation sollten mit den Patient:innen besprochen werden, wobei es sich hierbei um ein sehr selektioniertes Patientenkollektiv handelt.