Delir oder Demenz?
Ein Delir ist immer ein medizinischer oder psychiatrischer Notfall, der bei bis zu 50% der älteren Patienten im Spital auftritt. Viele von ihnen sind bereits bei der Aufnahme oder während des stationären Aufenthaltes delirant. Stark vereinfacht kann man das Delir auch als akuten Verwirrtheitszustand bezeichnen. Der Delirbegriff ist spezifischer und unterscheidet zwischen einer akuten Notfallsituation und anderen chronischen Syndromen im höheren Lebensalter, wie der Demenz. Diese Unterscheidung kann eine große Herausforderung sein, vor allem, wenn beide Krankheiten gleichzeitig vorliegen. In den meisten Fällen erlauben jedoch die folgenden Kernsymptome eines Delirs eine richtige Diagnose.
Die ICD-10-Kriterien für ein Delir sind: Störungen
- des Bewusstseins
- der Kognition
- der Psychomotorik
- des Schlaf-wach-Rhythmus mit nächtlicher Verschlechterung, Albträumen und Halluzinationen
Plötzlicher Beginn und Tagesschwankungen sind typisch. Ein objektiver Nachweis durch Anamnese, körperliche, neurologische, psychiatrische und laborchemische Untersuchung für einen Krankheitsauslöser sollte gelingen. Eine Dysbalance der Gehirnphysiologie liegt meist vor.
Eine einfache Delirdiagnostik gelingt, wenn Sie auf diese vier Symptomebenen achten:
- Erkennen einer kognitiven Störung aus der Anamnese oder der klinischen Untersuchung: Der Patient redet völlig wirr oder völlig anders als früher. Der Patient ist unfähig, seine Aufmerksamkeit zu fokussieren oder sich umzustellen (dies spricht für die Kognitionsstörung und die Bewusstseinsstörung).
- Typische psychomotorische Störungen, wie „der Patient läuft in der Nacht im Haus herum“, „will die Wohnung verlassen“, „lässt sich nicht beruhigen und schreit“. Dies entspricht den Störungen der Psychomotorik.
- Die vegetative Symptomatik reicht vom Tremor zum max. Schwitzen. „Der Patient ist völlig durchgeschwitzt, unruhig und er zittert stark.“
- Wahrnehmungsstörungen, Wahnsymptome und Halluzinationen, wie z.B. „ich muss mit dem Hund in der Nacht spazierengehen“ (aber es gibt keinen Hund). „Ein fremder Mann ist im Zimmer“ oder „ich nehme keine Medikamente, da diese vergiftet sind“.
Da diese Symptome fluktuieren, kann es vorkommen, dass sie bei der Untersuchung im Tagesverlauf nicht gesehen werden. Vor allem nachts kommt es zu einer Aggravation. Derartige Symptome setzen immer akut ein.
Delirien werden vor allem bei Demenzpatienten, die hypoaktive Delirien zeigen, oder bei begleitenden visuellen Störungen oft nicht richtig erkannt. Vor allem in Pflegeheimen kann das Nichterkennen von Delirien verheerende Folgen haben, da primär die somatischen Ursachen behandelt werden, jedoch die psychiatrische Symptomatik, wie gestörter Schlaf-wach-Rhythmus, Wahn und Halluzinationen, der Aufmerksamkeit entgehen und zu einer höheren Morbidität und Mortalität führen können.
Demenzen erhöhen das Delirrisiko
Demenzen sind ein Syndrom von erworbenen Störungen des Gedächtnisses und anderer kognitiver Funktionen aufgrund von strukturellen neuronalen Schädigungen. Degenerative und vaskuläre Veränderungen führen zu den bekanntesten Demenzformen (Alzheimer-Demenz, vaskuläre Demenz, Mix-Demenz oder Lewy-Body-Demenz). Delirien treten bei stationär aufgenommenen Demenzpatienten in 22–89% der Fälle auf. Die akute, sofortige Unterscheidung von einer Demenz ist essenziell. Ein Delir kann entweder eine Demenz begleiten oder per se zu einer Hirnleistungsstörung führen. Bei Älteren sind vor allem Nebenwirkungen von zentral gängigen Medikamenten, eine Elektrolytverschiebung, Flüssigkeitsmangel und Infektionen für die gestörte Gehirnfunktion verantwortlich, wobei das Vorhandensein einer Demenz den Schwellenwert für ein Delir deutlich reduziert. Eine Demenz erhöht das Delirrisiko um das Fünffache. Nicht selten ist bei deliranten Patienten die Orientierungsfähigkeit erhalten, jedoch imponieren eine gestörte Aufmerksamkeit und Konzentration (ein einfacher Test, wie Monate rückwärts aufsagen, ist nicht möglich).
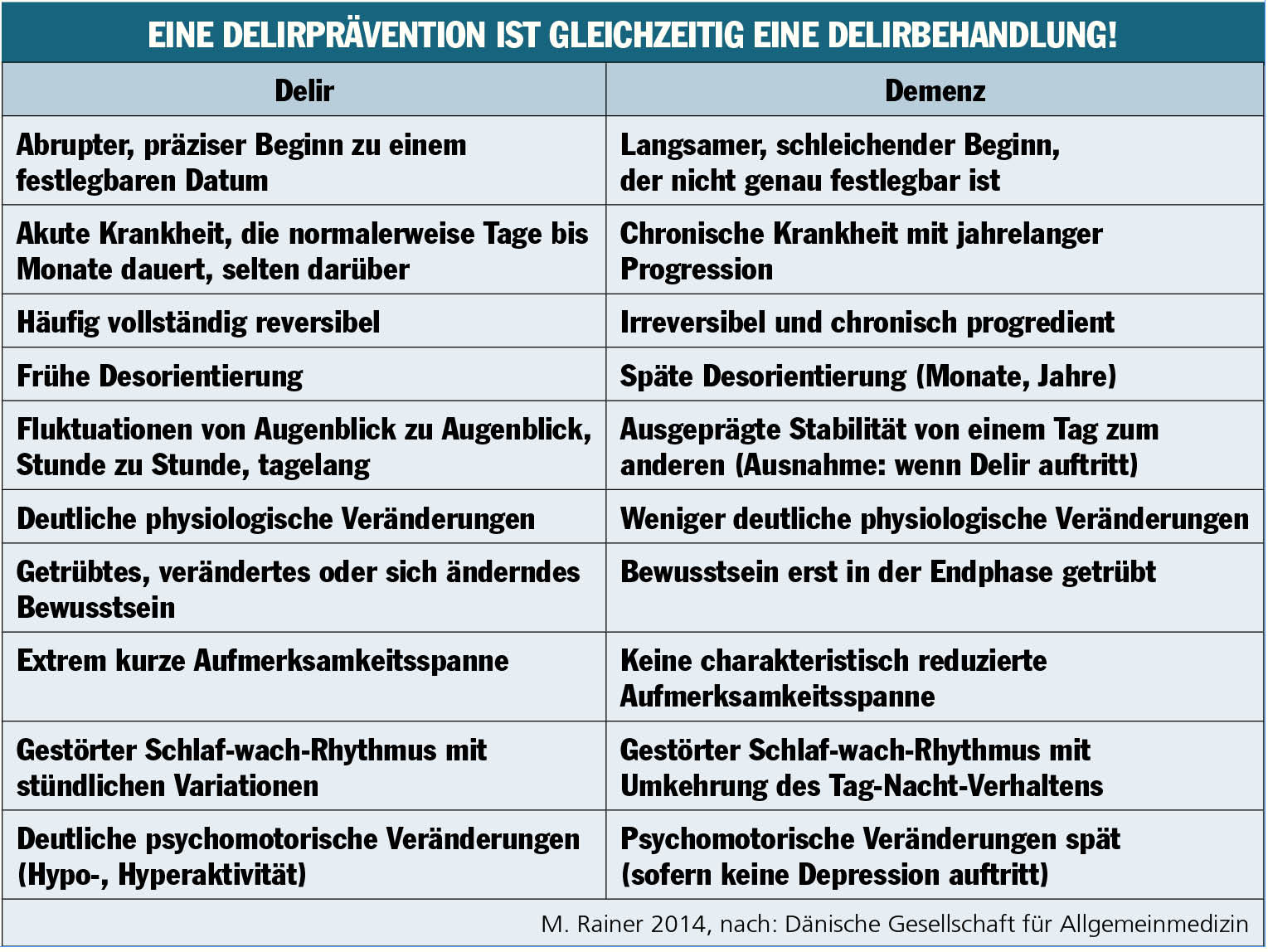
Unterschied zwischen Delir und Demenz?
Ein Delir tritt akut auf und spricht üblicherweise auf die medizinische Behandlung der zugrundeliegenden Erkrankung an. Wenn diese Erkrankung aber nicht identifiziert werden kann – weil angenommen wird, dass der Patient dement ist –, könnten die Konsequenzen fatal sein. Patienten mit unklaren kognitiven Störungen müssen auf mögliche somatische Ursachen untersucht werden, um zwischen Delir und Demenz differenzieren zu können.
- Die Demenz verläuft meist langsam, aber stetig, das Delir entwickelt sich plötzlich.
- Beim Delir kommt es zu kognitiven und Bewusstseinsfluktuationen und die „Verwirrtheit“ verschlechtert sich in der Nacht. Demenzpatienten zeigen hingegen keine Bewusstseinsveränderungen.
- Halluzinationen und Wahnideen sind beim Delir häufiger, phantastischer, und die emotionale Symptomatik steht beim Delirpatienten mehr im Vordergrund.
Durch die hohe Komorbidität bei Demenz erhöht sich das Delirrisiko. Demenzen werden häufig erstmals nach einer Delirepisode, die keine Restitutio ad integrum zeigt, evident. In der Differenzialdiagnose Delir und Demenz ist es wesentlich, genaue Informationen über den Beginn und den Verlauf der Symptome zu erheben, Wachsamkeit und Sensibilität auch für triviale körperliche Störungen zu zeigen und die Bereitschaft, eine genaue internistische Untersuchung durchzuführen, um die mögliche kausale Pathologie zu erkennen. Fluktuierende kognitive Leistungen, die wir bei der Lewy-Body-Demenz und der vaskulären Demenz sehen, können die Differenzialdiagnose erschweren. Eine genaue Medikamentenanamnese, bei der vor allem nach anticholinergen Medikamenten oder Benzodiazepinen gefragt wird, sollte auf keinen Fall fehlen.
Wie erkenne ich einen deliranten Demenzpatienten?
Die Diagnose ist oft als Bedside-Diagnose möglich. Sie erfordert jedoch eine 24-Stunden-Beobachtung und Informationen der Angehörigen oder Betreuer. Gibt es eine Veränderung der Kognition, der Funktionalität, des Verhaltens oder der Wahrnehmung gegenüber den früheren Wochen? Kommen Fluktuationen vor, sodass der Patient tagsüber normal erscheint, jedoch in den Abendstunden (Sundowning) oder in der Nacht unruhig und verwirrt wird? Sind neue visuelle Illusionen oder Halluzinationen, verändertes agitiertes Verhalten, wie Nesteln oder Greifen in der Luft, sowie eine hohe Ablenkbarkeit und eine geringe Aufmerksamkeit aufgetreten? Weitere Fragen sind: Wie lange war die Schlafdauer, traten Albträume oder nächtliche Unruhe, plötzliche Apathie und Rückzugsverhalten auf? Bei Demenzpatienten können sehr subtile delirante Symptome auftreten, wie plötzlicher Beginn einer Inkontinenz, Stürze, verweigerndes Verhalten, Immobilität, Dysphagie, Dysarthrie, stärkere Desorientierung oder ein verlangsamtes Denken.
Tests zur Unterscheidung von Delir und Demenz
Ein Delir kann man erkennen, indem man den Patienten alle Monate des Jahres von hinten nach vorne aufsagen lässt. Meist kommt er nicht über August oder Juli hinaus, spätestens dann schweift er durch sein Aufmerksamkeitsdefizit ab. Die Confusion Assessment Method ist eine einfache Beurteilung der
- Aufmerksamkeit
- Denkstörungen
- quantitativen Bewusstseinsstörungen
- des akuten Beginns und des fluktuierenden Verlaufes.
1 und 4 müssen mit Ja beantwortet sein und zusätzlich entweder 2 oder 3.
Zur Erkennung einer Demenz wird weltweit die Mini-Mental-State-Examination durchgeführt. An zweiter Stelle kommen der Uhrentest, ein verzögerter Worterinnerungstest, die Prüfung der Wortflüssigkeit, Erkennung von Gleichheiten und der Trail-Making-Test. Als Screeingins-trument hat sich die Montreal-Cognitive-Assesment-(MOCA-)Skala, die gratis auf www.mocatest.org heruntergeladen werden kann, bewährt. Sie beinhaltet einen Zahlen- und Buchstabenverbindungstest, das Kopieren eines Würfels, den Uhrentest und das Benennen von exotischen Tieren.
Therapie des Delirs
Vor der Verordnung der Medikamente sollte nach Ausschluss und Behandlung körperlicher, metabolischer oder infektiöser Ursachen die Medikationsliste überprüft werden. Absetzen oder Reduktion von potenziell delirogenen Substanzen, wie Analgetika (NSAR, Opioide), Anticholinergika (Atropine), Antidepressiva (TCA), Sedativa und Hypnotika (Benzodiazepine, Propofol), Kortikosteroide, Dopaminagonisten, ist essenziell. Antiarrhythmika, Betablocker, Digoxin, Antibiotika (Gyrasehemmer), Antiepileptika (Carbamazepin, Valproinsäure), gastrointestinale Medikamente (Antiemetika, H2-Rezeptorblocker) und Muskelrelaxanzien (Baclofen) erhöhen das Delirrisiko. Zur Grunderkrankungsbehandlung zählen Sauerstoffgabe, Rehydratation, Elektrolytausgleich. Bei zu schneller Rekompensation einer Hyponatriämie besteht die Gefahr einer pontinen Myelinolyse. Besteht eine positive Alkoholanamnese oder Verdacht einer Wernicke-Enzephalopathie, erhält der Patient Vitamin B1-Amp. i.v.
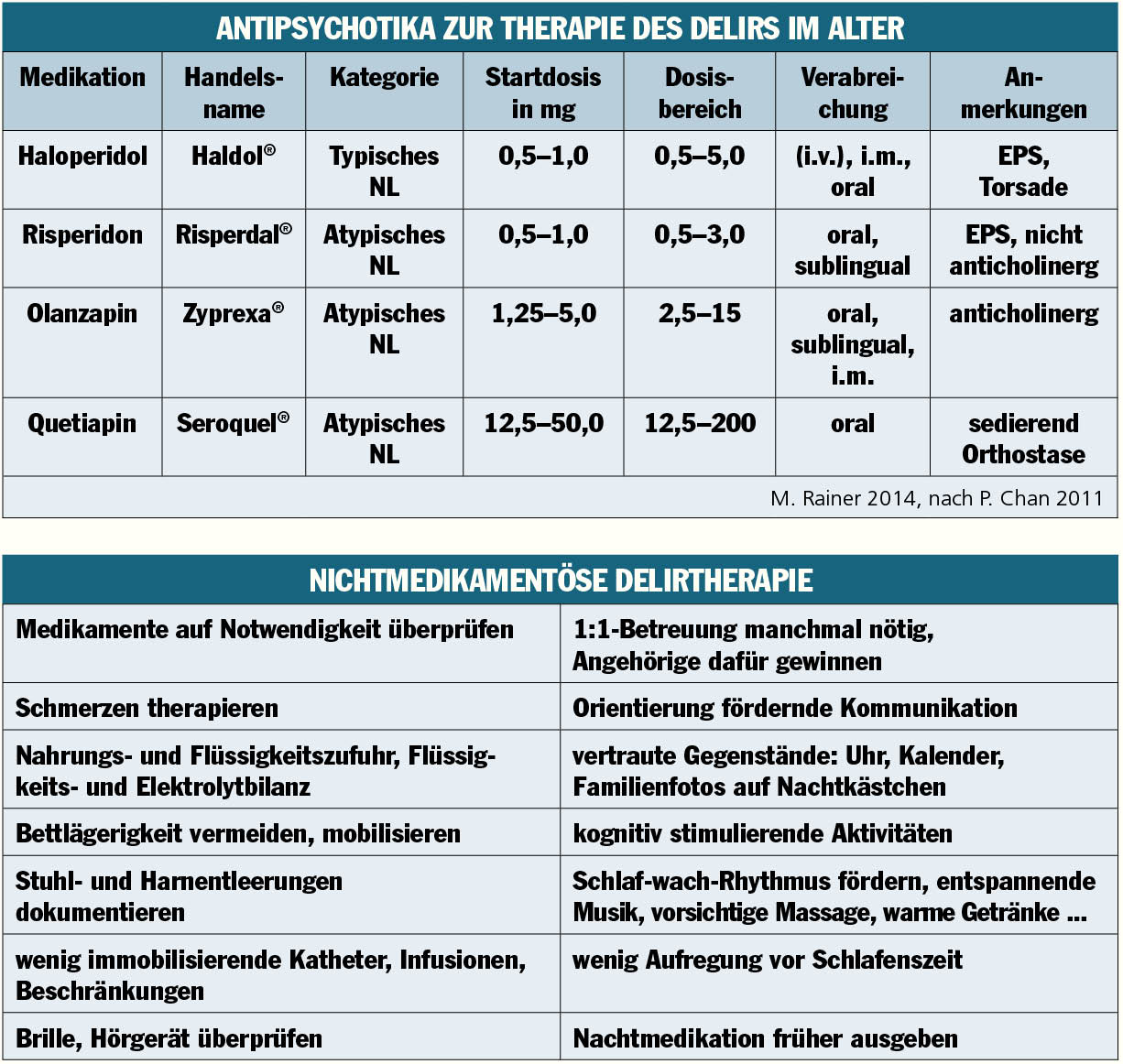
Antipsychotika
Haloperidol ist noch immer das Mittel der Wahl. Bei Demenzpatienten sollte jedoch auf das nebenwirkungsärmere Risperidon (0,25–1 mg 1–2-mal tgl.) zurückgegriffen werden. Dies vor allem bei primär hypoaktiven Patienten. Haloperidol wird in einer Dosierung von 0,5–2 mg alle zwei bis zwölf Stunden gegeben. Ist der Patient stark agitiert, kann Lorazepam 0,5–1 mg mit Dosiswiederholung nach vier bis sechs Stunden dazugegeben werden. Eine EKG-Kontrolle ist obligat, da es unter Haloperidol zu QTc-Verlängerungen kommen kann. Die i.v. Gabe von Haloperidol ist mittlerweile sehr umstritten und sollte vermieden werden. Haloperidol kann auch i.m. gespritzt werden. Keine Indikation liegt vor bei Lewy-Body-Demenz und Morbus Parkinson. Der größte Vorteil von Haloperidol liegt darin, dass es kaum anticholinerg ist und keine orthostatischen Synkopen auslöst. Es sollte jedoch nur so viel wie nötig und so kurz wie möglich gegeben werden. Aripiprazol (5–30 mg 1-mal pro Tag) zeigt eine gute Wirkung bei primär hypoaktiven Patienten. Olanzapin (2,5–5 mg 1–2-mal tgl.) wirkt zwar stärker sedierend, hat aber auch anticholinerge Eigenschaften und sollte deshalb beim Demenzpatienten vermieden werden. Quetiapin (12,5–100 mg) wirkt ebenfalls sedierend und führt oft durch die alphablockierenden Eigenschaften zu einer Hypotension. Vor allem in Kombination mit Alphablockern oder bei zu hoher Dosierung droht Sturzgefahr. Günstig ist Quetiapin, da es kaum zerebrovaskuläre Ereignisse provoziert und bei Lewy-Body-Demenz und Morbus Parkinson das Mittel der Wahl darstellt.
Eine spezielle Problematik ist das Delir bei Parkinson-Demenzpatienten, die unter Parkinson-Medikamenten delirant wurden. Hierbei sollte vor Behandlung mit Quetiapin daran gedacht werden, dass – in dieser Reihenfolge –
- Anticholinergika und trizyklische Antidepressiva,
- Amantadin und MAO-B-Hemmer
- Dopaminagonisten und
- COMT-Hemmer reduziert oder abgesetzt werden.
L-Dopa soll auf der niedrigstmöglichen Dosierung beibehalten werden.
Eine neue Alternative zur Delirbehandlung stellt Melatonin dar. Erste Versuche deuten auf eine signifikante Wirksamkeit hin. Rein experimentell sind derzeit Therapieversuch mit den Antipsychotika Floxapen (Adasuve®) und Benperidol (Glianimon®) und mit dem Antiepileptikum Gababentin (Neurontin®).
Pimavanserin, ein serotoninrezeptorinverser Agonist, konnte die psychotische Symptomatik bei Parkinson-Patienten signifikant verbessern, ist in Österreich aber noch nicht zugelassen.
Die Behandlung der Demenz
Bei leichter bis mittelschwerer Demenz (MMSE 26–10) sind die drei Cholinesterasehemmer Donepezil, Rivastigmin und Galantamin Mittel der Wahl. Für mittelschwere bis schwere Alzheimer-Demenz (MMSE 20–3) kommt Memantin zum Einsatz.
Alternativen bei Nichtwirksamkeit, bei starken Nebenwirkungen oder Kontraindikation sind Ginkgo biloba(240 mg/die) oder Cerebrolysininfusionsserien über 15–20 Tage (30 ml i.v.).