Diabetes: mehr als ein Zuckerproblem
Etwa 800.000 Menschen in Österreich leben mit der Erkrankung Diabetes, 90 % davon mit Diabetes mellitus Typ 2 (DM 2). Weitere etwa 350.000 Menschen mit Prädiabetes laufen Gefahr, innerhalb der nächsten Jahre an DM 2 zu erkranken, zudem können sich auch schon in dieser Phase irreversible Schäden an verschiedenen Organen oder Geweben entwickeln.Ein sehr gutes Beispiel dafür ist die periphere Neuropathie, deren Häufigkeit bei Menschen mit Prädiabetes mit jenen mit manifestem Diabetes mellitus Typ 2 vergleichbar hoch ist. Daraus ist klar ersichtlich, dass nur eine sehr frühe Intervention die Lebensqualität und Lebenserwartung der Betroffenen erhalten kann.
Prädiabetes
Als Prädiabetes wird eine gestörte Nüchternglukose oder Glukoseintoleranz bezeichnet. Die Diagnose wird anhand eines erhöhten Nüchternblutzuckerwertes (≥ 100 mg/dl und < 126 mg/dl), eines erhöhten HbA1c-Wertes (≥ 5,7 und < 6,5 %) oder eines erhöhten 2h-OGTT-Blutzuckerwertes (≥ 140 mg/dl und < 200 mg/dl) gestellt. Pro Jahr entwickeln 5–10 % aller PatientInnen mit Prädiabetes einen Diabetes mellitus Typ 2. Bei vielen Betroffenen tritt der Prädiabetes im Rahmen eines metabolischen Syndroms auf, das heißt, dass abgesehen von den erhöhten Glukosewerte auch noch arterielle Hypertonie, Dyslipidämie und möglicherweise Übergewicht als kardiovaskuläre Risikofaktoren hinzukommen. Das Vorliegen eines Prädiabetes hat sich auch als Risikofaktor für einen schweren COVID-19-Krankheitsverlauf herausgestellt.
Dieses Krankheitsstadium bietet die Möglichkeit einer frühzeitigen Intervention, das bedeutet im Falle von Übergewicht eine Gewichtsreduktion (hierfür wird eine kalorienreduzierte mediterrane Kost empfohlen), generell das Einhalten einer mediterranen Kost, körperliche Bewegung und Nikotinkarenz. Bei HochrisikopatientInnen (z. B. junges Alter) kann auch eine Off-Label-Therapie mit Metformin angedacht werden. Bei Vorliegen einer arteriellen Hypertonie sollte ein Blutdruckzielwert von < 130/80 mmHg (sofern keine spezifischen Begleiterkrankungen vorliegen oder es sich um ältere PatientInnen > 65. LJ handelt) und ein LDL-C-Zielwert von zumindest < 100 mg/dl (10-Jahres-Risiko für fatales kardiovaskuläres Ereignis: 1–5 %) erreicht werden. Bei multiplen kardiovaskulären Risikofaktoren liegt der LDL-C-Zielwert bei < 70 mg/dl (10-Jahres-Risiko für fatales kardiovaskuläres Ereignis: 5–10 %). Bei Vorliegen anderer kardiovaskulärer bzw. renaler Erkrankungen können auch niedrigere LDL-C-Zielwerte erforderlich sein.
Abklärung des Glukosestoffwechsels
Generell ist eine Evaluierung des Glukosestoffwechsels mittels Bestimmung von Nüchternglukose und HbA1c und gegebenenfalls ein OGTT bei allen Menschen ab dem 45. Lebensjahr und bei allen Patientinnen mit vorausgegangenem Gestationsdiabetes indiziert. Zudem sollte eine Abklärung bei allen Personen mit erhöhtem Risiko durchgeführt werden. Dazu zählen neben Menschen mit schon bekanntem Prädiabetes auch übergewichtige (BMI > 25 kg/m2) oder adipöse Personen, jene mit positiver Familienanamnese bei erstgradigen Verwandten, bei Vorliegen einer arteriellen Hypertonie, eines verminderten HDL-C, eines polyzystischen Ovarialsyndroms, einer Fettlebererkrankung, eines Hypogonadismus oder einer Akanthosis nigricans ebenso wie bei verminderter körperlicher Aktivität und chronischem Tabakkonsum. Die Häufigkeit der Evaluierung hängt vom individuellen Risikoprofil ab, sollte aber zumindest alle drei Jahre erfolgen; bei hohem Risiko wie Prädiabetes auf jeden Fall engmaschiger.
State-of-the-Art-Therapie des Diabetes mellitus Typ 2
Die Basistherapie des DM 2 stellen weiterhin Lebensstilmaßnahmen dar. Dazu gehören neben Nikotinkarenz, Einhalten einer mediterranen Kost (kalorienreduziert bei Übergewicht) auch reichlich körperliche Bewegung (mind. 150 min Ausdauertraining/Woche + Krafttraining). Außer bei geriatrischen oder multimorbiden PatientInnen sollte eine medikamentöse Therapie bei einem HbA1c ≥ 6,5 % – in erster Linie mit Metformin – eingeleitet werden. Bei kardiovaskulären oder renalem Hochrisikoprofil oder Vorerkrankungen ist Metformin HbA1c-unabhängig möglichst rasch mit einem SGLT2-Inhibitor oder einem GLP-1-Rezeptor-Agonisten (GLP-1-RA) mit nachgewiesenem kardiovaskulärem und/oder renalem Benefit zu kombinieren. Für alle anderen PatientInnen sollte bei Nichterreichen des individuellen HbA1c-Zielwertes eine Kombination mit einem SGLT2-Inhibitor, GLP-1-Rezeptor-Agonisten, DPP-IV-Inhibitor oder Pioglitazon begonnen werden.
Für einen Großteil der PatientInnen bedeuten die aktuellen internationalen und nationalen Therapieempfehlungen, dass nicht mehr Insulin, sondern GLP-1-RA die erste injizierbare Therapie darstellen. Eine Insulintherapie ist bei klinischen Zeichen des Insulinmangels, Akuterkrankungen, perioperativ, bei diätetisch unzureichend kontrolliertem Gestationsdiabetes, Kontraindikation oder Unverträglichkeit von anderen Antidiabetika und nach Ausschöpfen anderer antihyperglykämischer Therapien induziert.
Neben neuen Erkenntnissen über eindrucksvolle Nephro- und Kardioprotektion von SGLT2-Inhibitoren und GLP-1-Rezeptor-Agonisten hat es in den letzten Jahren auch neue Entwicklungen im Bereich der Insuline gegeben: Einerseits wird bei den Basisinsulinen an besonders langwirksamen Varianten gearbeitet und andererseits auch an kurzwirksamen Insulinanaloga mit noch schnellerem Wirkeintritt. Der individuelle HbA1c-Zielwert ist vor allem von der Diabetesdauer, den Komorbiditäten und der Komplexität der Therapie abhängig. Für junge, neu manifestierte Menschen mit Typ-2-Diabetes ist daher ein HbA1c-Wert < 6,5 % anzustreben, für einen Großteil der betroffenen PatientInnen ist ein HbA1c-Wert bis 7 % ausreichend, bei eingeschränkter Lebenserwartung oder entsprechenden Komorbiditäten kann dieser bis 8–8,5 % angesetzt werden, bei höheren Werten sind Akutkomplikationen und Hyperglykämie-Symptome zu erwarten.
Glukosemonitoring
Eine Blutzuckerselbstkontrolle ist bei all jenen PatientInnen notwendig, die aufgrund der medikamentösen Therapie einem Hypoglykämierisiko ausgesetzt sind (Therapie mit Insulin oder Sulfonylharnstoff). Zumindest gelegentliche Blutzuckerselbstkontrollen sind aber auch bei allen anderen PatientInnen zur Therapiekontrolle und Steigerung der Compliance sinnvoll.
Lipid- und Blutdruckkontrolle
Obwohl das kardiovaskuläre Risiko von Menschen mit Typ-2-Diabetes in den letzten Jahrzehnten sehr deutlich gesenkt werden konnte, liegt es weiterhin deutlich über jenem von nichtdiabetischen Menschen. Die Risikoreduktion in den letzten Jahren ist nicht nur Folge neuer Antidiabetika mit pleiotropen Wirkungen (speziell SGLT2-Inhibitoren und GLP-1-RA), sondern auch Folge einer effizienten LDL-Cholesterin-Senkung und Blutdruckkontrolle.
Der Zielblutdruck liegt bei PatientInnen mit Diabetes großteils bei < 130/80 mmHg (nicht < 120/70 mmHg), bei älteren PatientInnen (> 65. LJ) liegt der systolische Ziel-RR zwischen 130 und 139 mmHg. Als ini-tiale Therapie werden Modulatoren des Renin-Angiotensin-Systems empfohlen, häufig in Kombination mit einem Kalzium-Antagonisten oder Thiaziddiurektikum. Etwas komplexer sind die LDL-C-Zielwerte: Für einen Großteil der PatientInnen mit DM 2 liegen sie < 70 mg/dl oder < 55 mg/dl (bei Endorganschäden oder 3 weiteren Risikofaktoren). Basistherapie sind weiterhin die Statine, gegebenenfalls in Kombination mit Ezetimib. PCSK9-Hemmer sind bei Nichterreichen der Zielwerte unter maximal verträglicher Statindosis + Ezetimib indiziert. ATP-Citrat-Lyase-Inhibitoren können additiv bzw. bei Statinunverträglichkeit erwogen werden.
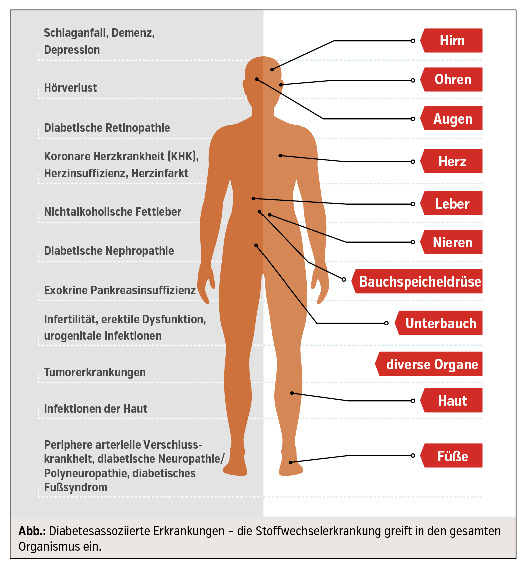
Diabetesassoziierte Erkrankungen
Neue britische Daten zeigen, dass bei Menschen mit Diabetes nicht mehr kardiovaskuläre, sondern onkologische Erkrankungen die häufigste Todesursache darstellen – generell ist das Spektrum der diabetes-assoziierten Folgeerkrankungen sehr breit (Abb.). Regelmäßige Screeninguntersuchungen (u. a. Albumin im Harn, Fußinspektion, augenärztli
che Untersuchung) sind daher ebenso wie Impfungen (CDC-Empfehlung: COVID-19, Influenza, Pneumokokken, Hepatitis B, Diphtherie/Tetanus/Pertussis, Herpes Zoster > 50. LJ) integraler Bestandteil der Behandlung von Menschen mit Diabetes mellitus.