Die diabetische Nierenerkrankung: Wo stehen wir 2022?
Die Zahl an Patienten mit Diabetes mellitus ist weiterhin im Anstieg begriffen und wird in den kommenden Jahren über eine halbe Milliarde Menschen erfasst haben. Diabetes ist nach wie vor die führende Ursache für eine chronische Niereninsuffizienz (CKD; „chronic kidney disease“), gefolgt von arterieller Hypertonie und einer prädiabetischen Stoffwechsellage, die allesamt ca. 75 % aller Ursachen einer CKD ausmachen.
Die diabetische Nierenerkrankung (DKD, „diabetic kidney disease“) wird durch eine reduzierte glomeruläre Filtrationsrate (eGFR) sowie eine erhöhte Albuminurie (> 300 mg/24 h) definiert und stellt eine progressive Erkrankung dar, die unbehandelt zu einer terminalen Niereninsuffizienz führt; in frühen Stadien einer DKD kann die GFR noch normal sein, die Albuminurie kann jedoch schon als Zeichen einer frühen Endothelschädigung erhöht sein.
Wichtig ist die Tatsache, dass bei Auftreten einer DKD nicht nur die Nierenfunktion selbst gefährdet ist, sondern das kardiovaskuläre Risiko des betroffenen Patienten dramatisch erhöht ist und mit Fortschreiten der DKD weiter steigt, sodass letztlich vor Erreichen einer terminalen Niereninsuffizienz die Mehrzahl der Patienten mit Diabetes an kardiovaskulären Ursachen verstirbt.
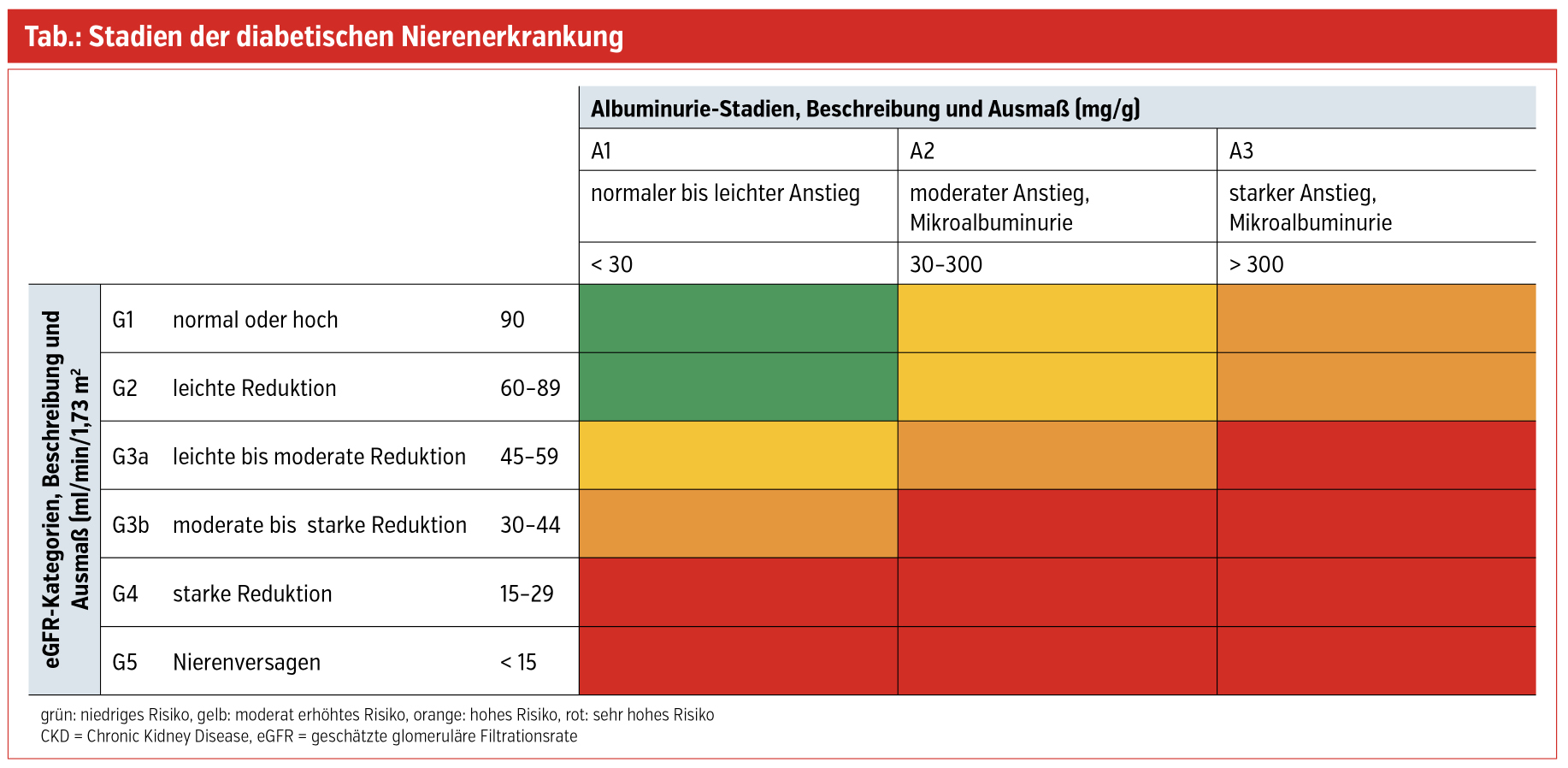
Die Erfassung einer DKD ist mit den beiden Serum- und Harn-Parametern eGFR und Albuminausscheidung (UACR) relativ einfach zu stellen. Entsprechend der Nierenfunktion (eGFR) und der Albuminurie kann die Stadieneinteilung der diabetischen Nierenerkrankung leicht durchgeführt werden (Tab).Mögliche andere Ursachen einer Nierenschädigung sollten ebenso erwogen werden bei:
- plötzlich auftretender großer Proteinurie
- rascher Verschlechterung der eGFR (> 5 ml/min pro Jahr eGFR-Abfall)
- pathologischem Harnstreifen (Erythrozyturie, Leukozyturie)
- auffälligem Nieren-Ultraschallbefund
- unauffälligem Netzhautbefund
Maßnahmen nach Diagnose
Ist die Diagnose einer DKD gesichert, so sind zuerst gesunde Lifestyle-Maßnahmen umzusetzen (Bewegung, Ernährung, Rauch-Stopp), zudem ist die Stoffwechselgüte so weit als möglich zu optimieren, da ein schlecht eingestellter Diabetes maßgeblich zur Progression einer DKD beiträgt. Weiters ist auf eine stringente Blutdruck-Kontrolle zu achten, mit systolischen Zielwerten < 130 mmHg, bei bestehender Albuminurie sogar von 120 mmHg: hier sollten in erster Linie ACE-Hemmer oder Sartane (diese nicht kombinieren!), sodann Kalzium-Antagonisten zum Einsatz kommen.
Weitere Therapiemöglichkeiten
SGLT-2-Hemmer
Als weitere Säule einer organprotektiven Therapie sollten wenn möglich SGLT-2-Hemmer eingesetzt werden. SGLT-2-Inhibitoren konnten in großen kardiovaskulären Endpunkt-Studien (Empagliflozin: EMPA-REG-Outcome; Canagliflozin: CANVAS, CREDENCE; Dapagliflozin: DAPA-CKD) nicht nur eine Reduktion der kardiovaskulären Sterblichkeit, sondern konsistent auch eine profunde Nephroprotektion belegen, d. h., der GFR-Abfall wurde deutlich abgebremst, und die Albuminurie on top zu ACE-Hemmern oder Sartanen wurde noch einmal deutlich reduziert. Dementsprechend existieren für betroffene Patienten mit Diabetes und einer DKD, wenn SGLT-2-Hemmer rechtzeitig eingesetzt werden, klare Überlebensvorteile. Da SGLT-2-Hemmer ihre antidiabetische Wirkung unterhalb einer GFR von 60 ml/min allmählich verlieren, ihr nephroprotektives Potenzial aber bis zumindest eine eGFR von 25–30 ml/min erhalten bleibt, hat dazu geführt, dass diese Substanzklasse als primär organprotektiv angesehen wird.
Mittlerweile konnten prospektive Studien auch zeigen, dass CKD-Patienten ohne Diabetes im gleichen Maß von der nephroprotektiven Wirkung der SGLT-2-Hemmer profitieren, sodass diese mittlerweile für die meisten Patienten mit CKD angewendet werden sollten.
GLP1-Rezeptoragonisten
Im Rahmen der Diabeteseinstellung wird der Substanzklasse der GLP-1-Rezeptoragonisten der Vorzug gegeben, da diese neben ihren günstigen kardiovaskulären Eigenschaften auch nephroprotektive Eigenschaften aufweisen, z. B. Senkung einer bestehenden Albuminurie.
Neues Therapie-Prinzip
Als neues Therapie-Prinzip konnten aufgrund größerer Studien sog. nichtsteroidale Mineralokortikoid-Rezeptorantagonisten (MRA) bei DKD-Patienten einen klaren nephroprotektiven Effekt zeigen. So liegt der Vorteil etwa von Finerenon als Vertreter dieser neuen Substanzklasse, der in Europa und den USA mittlerweile zur DKD-Therapie in den CKD-Stadien 3 und 4 zugelassen ist, im Fehlen der klassischen Nebenwirkungen steroidaler MRAs, wie z. B. Gynäkomastie. Zudem war in den Studien das Hyperkaliämie-Risiko insgesamt gering.
Während in den 80er-Jahren der eGFR-Verfall bei DKD-Patienten noch bei 10–12 ml/min/Jahr lag, so wurde v. a. mit der Einführung der ACE-Hemmer und Sartane dieser Nierenfunktionsverlust auf ca. 4–6 ml/min/Jahr reduziert. Mit den SGLT-2-Hemmern konnte noch einmal entscheidend der Nierenfunktionsverlust bis ca. 2–3 ml/min/Jahr abgebremst werden, eine eGFR-Abnahme von 0,7–0,9 ml/min/Jahr entspricht einer altersbedingten physiologischen GFR-Abnahme.
Es ist davon auszugehen, dass die Einführung von Finerenon noch zusätzlich eine Besserung des GFR-Abfalls bei DKD-Patienten bedingt und damit deren hohes renales sowie kardiovaskuläres Risiko weiter reduziert.
Interdisziplinäre Betreuung der Patienten
Klarerweise müssen CKD-Patienten auch hinsichtlich ihrer Blutzuckereinstellung, ihres Blutdrucks und ihres Lipidprofils sowie allfälliger Komorbiditäten optimal betreut werden. Eine Verlaufskontrolle je nach Nierenfunktion sollte 2- bis 4-mal im Jahr folgende Parameter erfassen: eGFR sowie Albuminurie, Überwachung der Blutdrucktherapie, HbA1c-Wert sowie Lipidstatus. Bei weiter eingeschränkter Nierenfunktion sind klarerweise erweiterte Nierenparameter auch zu erfassen (u. a. PTH, Vitamin-D, venöses Blutgas, Eisenstatus, Hämoglobin, Elektrolyte). Ab einem eGFR-Bereich von 30 bis 45 ml/min ist die Vorstellung bei einem nephrologischen Facharzt oder einem nephrologischen Zentrum im Sinne einer interdisziplinären Kooperation sinnvoll, bei rascher Nierenfunktionsverschlechterung sowie den oben dargestellten Befunden ist eine sofortige ärztliche Vorstellung angeraten.
Fazit: Früherkennung senkt Mortalität
Insgesamt haben gerade die letzten wenigen Jahre einen enormen Fortschritt in der Therapie von Patienten mit Diabetes und chronischer Nierenerkrankung gebracht. Da nur ein frühes Erkennen renaler Komplikationen ein rasches Handeln ermöglicht, welches letztlich die Mortalität Betroffener reduzieren kann, sollten wir daher alles daransetzen, um die Nierenfunktion aller Patienten mit Diabetes im Auge zu behalten, denn wir haben nun effiziente Möglichkeiten der therapeutischen Intervention in der Hand.