Herzinsuffizienz – altbewährte und neue Therapien
Graduiert wird die Herzinsuffizienz anhand ihrer linksventrikulären Pumpfunktion in Herzinsuffizienz mit reduzierter (HFrEF), mittelgradig reduzierter (HFmrEF) oder erhaltener (HFpEF) Linksventrikelfunktion. Während sich die unterschiedlichen Ätiologien in ihrer Therapie deutlich unterscheiden, ist die Symptomatik überschneidend. Patienten präsentieren sich häufig symptomatisch, mit Dekompensationszeichen, geprägt durch Dyspnoe, eingeschränkter Belastbarkeit und reduzierter Lebensqualität. Therapieziel der chronischen Erkrankung ist neben der Mortalitätsreduktion eine Verbesserung der Lebensqualität. Oft liegen Begleiterkrankungen vor, die das therapeutische Management vor mögliche Herausforderungen stellen.
Neben invasiven Therapieoptionen wie Herzklappeneingriffen oder der Resynchronisationstherapie stellt die medikamentöse Therapie die eigentliche Hauptsäule der Salutogenese dar.
Therapeutische Herausforderung: chronische HFpEF/HFmrEF
Bis heute gibt es für Patienten mit HFpEF oder HFmrEF keine spezifische Therapie, für die ein signifikanter Überlebensbenefit gezeigt werden konnte. Hier steht die symptomatische, vor allem diuretische Therapie im Vordergrund. Zudem ist eine optimale Reduktion von Risikofaktoren und die therapeutische Einstellung vorliegender Komorbiditäten unumgänglich und mit einer Reduktion von Hospitalisierungen und symptomatischer Verbesserung der Patienten verbunden.
„Old but gold“ in der chronischen HFrEF
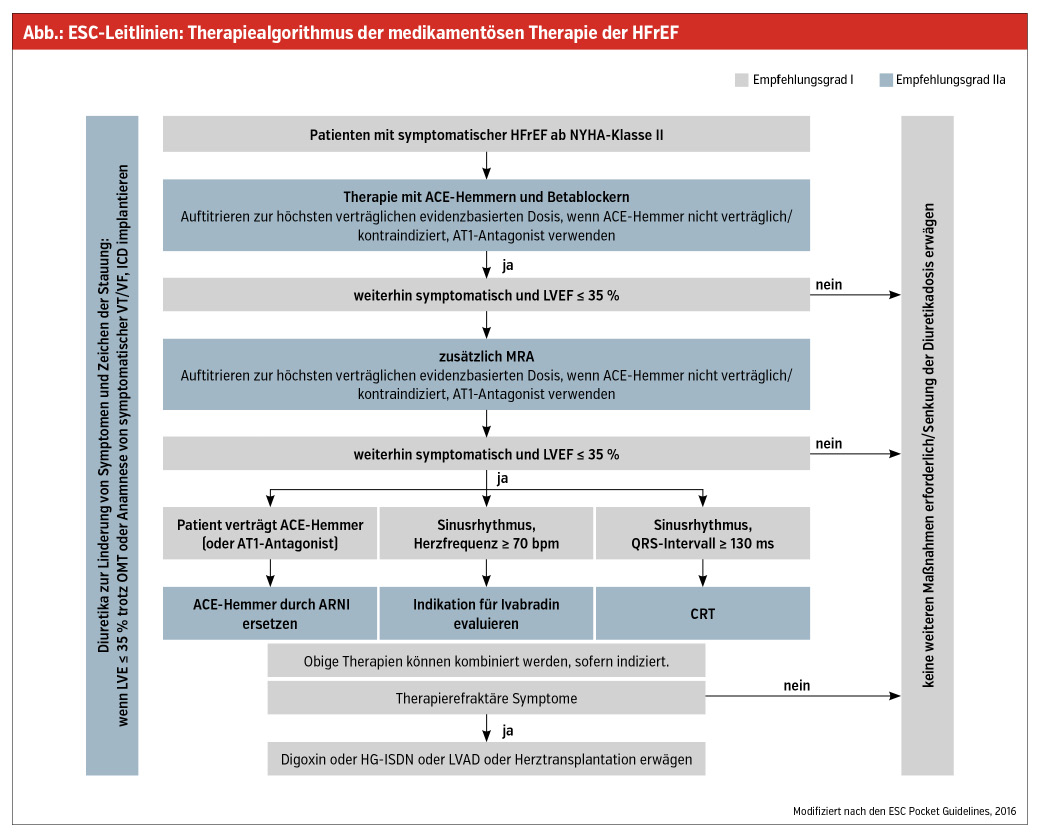
Die Goldstandard-Therapie der HFrEF setzt sich aus den drei wesentlichen Medikamentengruppen Betablocker, Renin-Angiotensin-System-Hemmer (ACE-Hemmer beziehungsweise Angiotensin-Rezeptor-Blocker) und Mineralokortikoid-Rezeptor-Blocker zusammen.1 Seit den Ergebnissen der PARADIGM-HF-Studie2 sollte die Therapieerweiterung der Neprilysin-Hemmung mit dem kombinierten Angiotensin-Rezeptor-Neprilysin-Inhibitor (ARNI) Sacubitril/Valsartan in der Therapie des symptomatischen Patienten mit HFrEF nicht fehlen.
Des Weiteren gilt für Patienten, die unter optimierter Therapie weiterhin symptomatisch sind und im Sinusrhythmus eine Herzfrequenz ≥ 70 bpm aufweisen, die Therapie mit Ivabradin als indiziert (Abb.).1
Überlebensbenefit und Reduktion von Herzinsuffizienzhospitalisierung und Symptomatik konnte für die genannten Medikamentengruppen gezeigt werden. Für sie alle gelten jedoch evidenzbasierte Maximaldosierungen, die aus multiplen Gründen in der klinischen Praxis oft nicht erreicht werden. Um den optimalen therapeutischen Nutzen für den Herzinsuffizienz-Patienten zu erzielen, gilt es jedoch eine Titration des jeweiligen Medikamentes bis zur Maximaldosierung anzustreben! Die Dosis der oft begleitende diuretische Therapie sollte so gering wie möglich gehalten werden.
Rezente Highlights in der HFrEF-Therapie
Nach der Inklusion des ARNI in die internationalen Leitlinien der Herzinsuffizienztherapie wurden rezent einige vielversprechende neue Medikamente mit potenziell signifikantem Stellenwert in der Herzinsuffizienztherapie in prospektiven randomisierten Studien getestet: SGLT-2-Hemmer, Myosin-Aktivator und Guanylatzyklase-Stimulator sind drei Substanzen, die in weiterer Folge kurz vorgestellt werden sollen.
SGLT2-Hemmer Gliflozine
Die aktuelle Datenlage zeigt, dass die ursprünglich zur Therapie des Typ-2-Diabetes (T2D) entwickelten SGLT2-Hemmer, auch ungeachtet des Vorliegens eines T2D, (kardiovaskuläre) Mortalität und Herzinsuffizienzhospitalisierung bei Patienten mit symptomatischer chronischer HFrEF signifikant um bis zu 26 % reduzieren und die Lebensqualität dieser Patienten verbessern. Die hier gültige Evidenz liefern die DAPA-HF-Studie3 (vorgestellt am ESC 2019) und die EMPEROR-Reduced-Studie4 (vorgestellt am ESC 2020). Die in den placebokontrollierten Studien beobachteten Nebenwirkungen traten in beiden Gruppen nahezu gleich selten auf und führten nur in wenigen Ausnahmefällen zum Therapieabbruch.
Auch wenn noch nicht in den Leitlinien zur Herzinsuffizienz-Therapie etabliert, sind die SGLT2-Hemmer aus der HFrEF-Therapie nicht mehr zu eliminieren. Im Positionspapier der Fachgesellschaften (ESC, AHA) wird ihr Einsatz zu Therapie oder Prävention von HFrEF bei Patienten mit T2D und manifesten kardiovaskulären Erkrankungen oder einem hohen kardiovaskulären Risiko empfohlen. Des Weiteren wird die Empfehlung zum Einsatz von Dapagliflozin oder Empagliflozin bei Patienten mit symptomatischer chronischer HFrEF, unabhängig vom Diabetesstatus, somit als Standard-Herzinsuffizienzmedikament ausgesprochen.5
Guanylatzyklase-Stimulator Vericiguat
Bei Patienten mit HFrEF ist der NO-sGC-cGMP-Signalweg komprimiert und wird durch den sGC-Stimulator Vericiguat wiederhergestellt. Vericiguat greift am Endothel an und sorgt dafür, dass Gefäße sich erweitern und im Myokard Versteifung, Fibrose und Remodelling reduziert werden. Der VICTORIA-Trial, eine Phase-III-Studie, hat aktuell die Wirksamkeit und Sicherheit dieser Therapie belegt. Vericiguat (10 mg/d) reduzierte das kombinierte Risiko von kardiovaskulärem Tod oder erstem Auftreten einer herzinsuffizienzbedingten Hospitalisierung statistisch signifikant um 10 % (relative Risikoreduktion [HR] 0,90; 95%-Konfidenz-intervall [KI] 0,82–0,98; p = 0,019). Auch wenn im Nebenwirkungsprofil Hypotonie, Synkope und Anämie etwas häufiger unter der Therapie beobachtet wurden, kam es zu keinen signifikanten Unterschieden im Vergleich zur Placebotherapie.6
Zum Einsatz von Vericiguat in der HFpEF liegen keine Outcome-Daten vor. Der VITALITY-HFpEF Trial untersuchte den Einfluss des Medikamentes auf den symptomatischen Status dieser Patienten, lieferte aber ein neutrales Ergebnis.7
Myosin-Aktivator Omecamtiv-Mecarbil
Omecamtiv-Mecarbil ist ein kardialer Myosin-Aktivator, der direkt auf die kontraktilen Mechanismen des Herzens wirkt. Der Wirkstoff verlängert die zyklusabhängige Interaktion von Myosin mit Aktin und bewirkt so eine Optimierung der kardialen Kontraktilität, ohne den Energiebedarf zu potenzieren.
Der GALACTIC-HF-Trial (Phase III) zeigte bei stabilen Patienten mit HFrEF, dass durch eine Therapie mit Omecamtiv-Mecarbil das Risiko für den primären kombinierten Studienendpunkt, kardiovaskuläre Mortalität und erstes herzinsuffizienzbedingtes Ereignis, im Vergleich zur Placebo-Therapie statistisch signifikant reduziert wird (HR: 0,92; 95%-KI: 0,86–0,99, p = 0,025). Im sekundären Endpunkt kardiovaskuläre Mortalität wurde keine Reduktion beobachtet. Unerwünschte Ereignisse waren in beiden Behandlungsarmen ausgeglichen. Die Daten zeigen, dass besonders Patienten mit stark reduzierter linksventrikulärer Auswurffraktion (LVEF < 28 %) besonders durch die Therapie mit Omecamtiv-Mecarbil profitieren könnten. Die Ergebnisse wurden am AHA-Kongress 2020 präsentiert.8
Fazit
Welchen expliziten Stellenwert die vorgestellten Medikamente in der immer komplexer werdenden Herzinsuffizienz-Therapie erhalten könnten, ist aktuell nicht eindeutig zu sagen. Der zunehmende wissenschaftliche und therapeutische Ansatz der Phänotypisierung und individualisierten Therapie erfordert diesbezüglich weitere Substudien und weitere Aufarbeitung der vorliegenden Daten.
- Für den Patienten mit HFrEF gilt, dass die Reevaluierung der Therapie bei jeder Visite empfehlenswert ist. Alle Medikamente verschrieben und maximal dosiert? (Betablocker + RAS-Hemmer [ACE-Hemmer/ARB/ARNI] + MRA)
- Bei allen Herzinsuffizienz-Patienten beachten: Volumenstatus (Diurese)? Alle Risikofaktoren und Komorbiditäten behandelt?
- Bei dennoch tendenziell progredienter Symptomatik, dem Vorliegen von unter anderem (sekundären) Klappenvitien, Rhythmusstörungen oder Asynchronie wird eine Zuweisung an ein Spezialzentrum empfohlen.
Literatur:
- Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JGF, Coats AJS et al., 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. European heart journal 2016; 37(27):2129–200
- McMurray JJ, Packer M, Desai AS, Gong J, Lefkowitz MP, Rizkala AR et al., Angiotensin-neprilysin inhibition versus enalapril in heart failure. The New England journal of medicine 2014; 371(11):993–1004
- McMurray JJV, DeMets DL, Inzucchi SE, Køber L, Kosiborod MN, Langkilde AM et al., A trial to evaluate the effect of the sodium-glucose co-transporter 2 inhibitor dapagliflozin on morbidity and mortality in patients with heart failure and reduced left ventricular ejection fraction (DAPA-HF). European journal of heart failure 2019; 21(5):665–75
- Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P et al., Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. The New England journal of medicine 2020; 383(15):1413–24
- Seferović PM, Fragasso G, Petrie M, Mullens W, Ferrari R, Thum T et al., Heart Failure Association of the European Society of Cardiology update on sodium-glucose co-transporter 2 inhibitors in heart failure. European journal of heart failure 2020; 22(11):1984–6
- Armstrong PW, Pieske B, Anstrom KJ, Ezekowitz J, Hernandez AF, Butler J et al., Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction. The New England journal of medicine. 2020; 382(20):1883–93
- Armstrong PW, Lam CSP, Anstrom KJ, Ezekowitz J, Hernandez AF, O’Connor CM et al., Effect of Vericiguat vs Placebo on Quality of Life in Patients With Heart Failure and Preserved Ejection Fraction: The VITALITY-HFpEF Randomized Clinical Trial. Jama 2020; 324(15):1512–21
- Teerlink JR, Diaz R, Felker GM, McMurray JJV, Metra M, Solomon SD et al., Cardiac Myosin Activation with Omecamtiv Mecarbil in Systolic Heart Failure. The New England journal of medicine 2020