KHK: Medikamentös, interventionell oder chirurgisch
Eine Revaskularisation kann sowohl aus prognostischen als auch aus symptomatischen Gründen indiziert sein, es muss jedoch jeweils ein objektiver Ischämienachweis vorliegen. Dieser kann mittels nichtinvasiver (Ergometrie, Koronar-Computertomografie, Magnetresonanzuntersuchung oder Myokardszintigrafie) oder invasiver Messung (fraktionelle Flussreserve, FFR oder „instantaneous wave-free ratio“, iwFR) erfolgen.
Die optimale medikamentöse Therapie ist dabei immer Voraussetzung für eine Revaskularisation. Sie beinhaltet neben einer optimalen Blutdruckeinstellung auch eine Cholesterinsenkung und eine thrombozytenhemmende Therapie. Der vor über 10 Jahren erbrachte Nachweis, dass eine medikamentöse Therapie bei einem relativ gering ausgeprägten Ischämieareal von maximal 10 % der interventionellen Therapie als gleichwertig zu betrachten ist, ist auch weiterhin gültig.
PCI versus Bypass
Eine Eingefäßerkrankung oder auch eine Zweigefäßerkrankung, bei der die LAD (linkes vorderes Herzkranzgefäß) nicht betroffen ist, stellt in aller Regel keine Indikation zu einer Bypassoperation (CABG) dar. Bei jeder anderen Form einer Mehrgefäßerkrankung ist die Bypassoperation immer eine empfohlene Therapieoption. Die perkutane Koronarintervention (PCI) ist bei Mehrgefäßerkrankung nur bis zu einem SYNTAX-Score (beschreibt Schweregrad bezie-hungsweise die Komplexität einer KHK) von 22 der Bypassoperation als gleichwertig zu sehen.
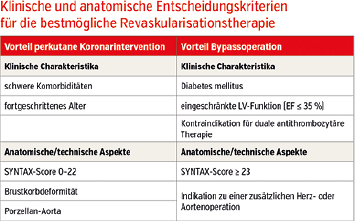
Bei Patienten mit Mehrgefäßerkrankung und Diabetes mellitus ist die Bypassoperation der PCI prinzipiell überlegen. Dies hauptsächlich deswegen, weil die Progressionsgeschwindigkeit der koronaren Herzerkrankung beim Patienten mit Diabetes eine schnellere ist und daher eine Überbrückung eines gesamten Gefäßsegments besser ist als die PCI, die nur eine fokale, zum jeweiligen Zeitpunkt vorliegende Stenose behandelt. Die klinischen und anatomischen Entscheidungskriterien für die jeweilige Wahl der bestmöglichen Revaskularisationstherapie sind in der Abbildung zusammengefasst.
Wie schnell zur Koronarangiografie?
Bei der Revaskularisierung im Rahmen eines akuten Koronarsyndroms mit Nicht-ST-Hebungs-Infarkt (NSTEMI-ACS) ist zu beachten, dass die vorgeschlagene Zeitspanne bis zur Koronarangiografie vom jeweiligen Risiko abhängt. So sind beispielsweise Patienten mit anhaltenden Beschwerden, die hämodynamisch instabil sind, lebensbedrohliche Arrhythmien haben oder an akuter Herzinsuffizienz leiden, innerhalb von zwei Stunden einer invasiven Untersuchung zuzuführen. Diese Patienten mit „sehr hohem Risiko“ sind gleich zu behandeln wie ein STEMI-Patient. Patienten mit einem „hohen Risiko“, definiert als GRACE-Score von > 140 sind innerhalb von 24 Stunden einer Koronarangiografie zuzuführen. Die „Intermediate risk“-Patienten, also beschwerdefreie Patienten mit Diabetes mellitus oder Niereninsuffizienz oder einer linksventrikulären Auswurffraktion von < 40 %, sind innerhalb von 72 Stunden mittels invasiver Koronarangiografie zu untersuchen. Für die Behandlung der STEMI-Patienten hat sich in den neuen Guidelines, im Vergleich zu den im Jahr 2017 publizierten ESC-STEMI-Guidelines, wenig Neues getan. Die Zeit von der STEMI-Diagnose mittels EKG bis zur Reperfusion („wire crosing“) sollte ≤ 120 Minuten, idealerweise sogar weniger als 90 Minuten betragen. Die vorgeschlagenen Zeitfenster sind gleichgeblieben, der gemessene Zielpunkt zur Zeitnehmung, nämlich das „wire crossing“, ist eine neue Definition.
Neue Empfehlungen
Eine relevante Neuerung in den aktuellen Guidelines ist die vorgeschlagene Revaskularisierung von Patienten, die im Rahmen des Herzinfarktes einen kardiogenen Schock entwickeln. Dabei sind aufgrund der rezenten CULPRIT-SHOCK-Studie von Prof. Thiele die Empfehlungen dahingehend abgeändert worden, dass im Rahmen der primären Herzkatheteruntersuchung nur die für den Herzinfarkt (und den kardiogenen Schock) ursächliche Läsion behandelt werden soll. Die allenfalls weiteren vorliegenden relevanten Stenosen sollen zweizeitig interveniert werden. Sollten jedoch mehrere höchstgradige, das heißt flusslimitierende Stenosen vorliegen beziehungsweise die Culprit-Läsion nicht klar identifizierbar sein, dann sollten alle Läsionen in der primären Katheteruntersuchung dilatiert und mittels Stents versorgt werden.
KHK plus Klappenvitium
Eine besondere Herausforderung im klinischen Alltag können Patienten mit einem relevanten und operativ zu behandelndem Vitium und gleichzeitig vorliegender koronarer Herzerkrankung sein. Dabei wird unterschieden, ob die primäre Indikation der Klappeneingriff oder die myokardiale Revaskularisation ist. Im ersteren Fall wird weiterhin eine (rein) angiografische Beurteilung der Stenosen als ausreichend empfohlen, was bedeutet, dass die invasive Abklärung mittels FFR beziehungsweise iwFR hier nicht erforderlich ist. Wenn hingegen die vorliegende koronare Mehrgefäßerkrankung die primäre Operationsindikation darstellt und zusätzlich eine mittelgradige Aortenklappenstenose oder Insuffizienz vorliegt, sollte die Entscheidung individuell getroffen werden, dies vor allem vor dem Hintergrund der sehr raschen Entwicklung auf dem Gebiet der Transkatheter-Klappen-Technologie. Bei Vorliegen einer mittelgradigen Mitralklappeninsuffizienz ist die Datenlage ebenso kontroversiell. Obwohl nur Beobachtungsstudien und nicht große randomisierte Studien vorliegen, sollte bei einer EROA („effective regurgitant orifice area“) > 0,2 cm2 und einem Regurgitationsvolumen von > 30 ml ein gleichzeitiger Mitralklappeneingriff in Erwägung gezogen werden, es wird aber auch in diesem Fall in den aktuellen Guidelines eine individuelle Entscheidung empfohlen.
Wiederholte Eingriffe
Die wiederholt notwendige Revaskularisierung ist im klinischen Alltag ebenfalls eine nicht selten vorkommende Herausforderung. Bei einer In-Stent-Restenose in einem „bare metal stent“ (BMS) oder in einem „drug eluting stent“ (DES) kann diese sowohl mit „drug eluting balloon“ (DEB) als auch mit einem weiteren DES behandelt werden.
Im Falle eines „early graft failure“ nach aortokoronarer Bypassoperation sollte primär das native Gefäß interveniert werden, dies vor allem deswegen, weil ein frischer Venenbypass beziehungsweise eine frische Anastomose interventionell nicht angegangen werden soll. Die Gefahr einer Embolisation beziehungsweise einer Perforation wäre in diesem Fall sehr hoch.
Zusammenfassend kann festgehalten werden, dass unter Berücksichtigung der aktuellen Leitlinien in den meisten Fällen eine gute Therapieentscheidung für die optimale Behandlung der koronaren Herzerkrankung beim jeweiligen Patienten getroffen werden kann.
Die von der Europäischen Kardiologischen Gesellschaft 2018 publizierten „Guidellines on myocardial revaskularization“, die in der aktuellen Version fast 100 Seiten und über 780 Zitate umfassen, sind Grundlage dieses Artikels. Die darin enthaltenen Empfehlungen zur optimalen Wahl der Revaskularisationsstrategie basieren auf über 20 randomisierten Studien und umfassen über 15.000 Patienten.