Neuropathische Schmerzen entwickeln sich als Folge von Läsionen oder Erkrankungen, die das somatosensorische Nervensystem entweder in der Peripherie oder zentral betreffen.
Typischerweise können zentrale neuropathische Schmerzen im Rahmen eines Schlaganfalles, einer MS-Erkrankung oder einer posttraumatischen Myelon-Läsion entstehen. Die Schädigungen im Bereich des peripheren Nervensystems sind auf fokale oder generalisierte neuropathische Syndrome zurückzuführen. Klassische Beispiele sind die diabetische, die alkoholtoxische und die medikamententoxische Polyneuropathie, die kompressive Radikulopathie sowie Engpasssyndrome wie beispielsweise das Karpaltunnelsyndrom.
Die Klassifikation neuropathischer Schmerzen ist komplex, Leitlinien dienen einer korrekten Einschätzung. Der traditionelle Ansatz klassifiziert neuropathische Schmerzen nach der zugrundeliegenden Ursache (z. B. diabetische Neuropathie, postherpetische Neuralgie) sowie nach der vermuteten Lokalisation der Nervenverletzung (peripher oder zentral).
Zu den Anzeichen und Symptomen, die mit dem Vorhandensein einer Neuropathie verbunden sind, gehören Allodynie, Hyperalgesie und Parästhesie genauso wie Hypästhesie und Hypalgesie. Bei Patient:innen, die unter neuropathischen Schmerzen leiden, ist der wahrgenommene Schmerz in der Regel spontan und manifestiert sich, ohne dass ein Reiz erforderlich ist. Dieser pathologische Zustand beeinträchtigt die Lebensqualität der Patient:innen erheblich.
Die diagnostische Abklärung bei Patient:innen mit Verdacht auf neuropathische Schmerzen sollte neben einer umfassenden körperlichen und neurologischen Untersuchung auch eine ausführliche Anamnese beinhalten. Die Anamnese soll Aufschluss über den Beginn, die Lokalisation und die Verteilung des Schmerzes und den möglichen Zusammenhang mit einem Trauma geben. Darüber hinaus sollte die Qualität des Schmerzes anhand von Schmerzdeskriptoren erfasst werden. Screeningfragebögen werden ebenso in der Diagnostik neuropathischer Schmerzen eingesetzt. Häufig verwendet werden der DN4-, painDETECT- sowie der LANSS-Fragebogen. Das Ausmaß der neuropathischen Komponente an einem chronischen Schmerzsyndrom kann mit dem Neuropathic Pain Symptom Inventory (NPSI) und der Neuropathic Pain Scale abgeschätzt werden.
Zu einer erweiterten Diagnostik in der Abklärung neuropathischer Schmerzen gehören bildgebende Verfahren (CT, MRT), elektrophysiologische Untersuchungen (EMG, NLG), eine quantitativ sensorische Testung, ein 3-Phasen-Skelettszintigramm bei Verdacht auf CRPS sowie diverse Laboruntersuchungen.
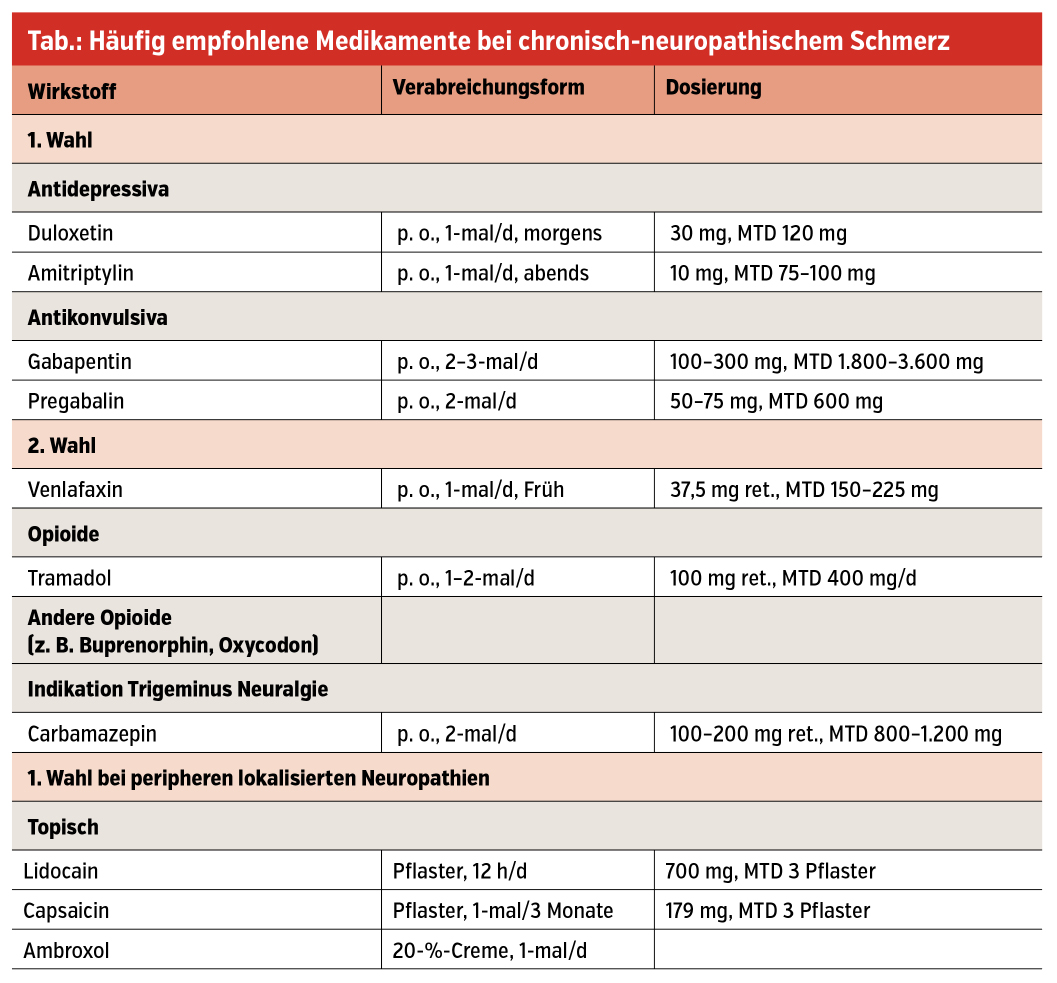
Die pharmakologische Therapie muss individuell angepasst werden. Eine Schmerzreduktion von 30 bis 50 % ist bei den meisten Patient:innen möglich und kann als Erfolg gewertet werden. Ziel ist immer eine Verbesserung der Lebensqualität und für berufstätige Patient:innen eine Rückführung in den Arbeitsprozess. Die Empfehlungen der DGN/ÖGN-Leitlinie sind in der Tabelle zusammengefasst (Tab.).
Systemische pharmakologische Therapien sind häufig mit ausgeprägten Nebenwirkungen verbunden. Unerwünschte Wirkungen wie Benommenheit, Schwindelgefühl oder auch sedierende Effekte können eine Aufdosierung des Medikamentes verhindern.
Als nichtmedikamentöse Therapien in der Behandlung neuropathischer Schmerzen kommen Methoden wie Physiotherapie, Ergotherapie, TENS-Behandlungen, Hochtontherapien etc. mit unterschiedlichem Erfolg zum Einsatz.
Zoster-Neuritis und postherpetische Neuropathie
Eine häufige Ursache für neuropathischen Schmerz stellt die Herpes-Zoster-Infektion dar. Berechnungen zufolge durchlebt fast jeder dritte Mensch im Laufe seiner Lebenszeit eine Zoster-Infektion und etwa die Hälfte jener, die das 85. Lebensjahr erreichen. Das Alter stellt den wichtigsten Risikofaktor für eine HZ-Infektion dar.
Typische klinische Anzeichen einer frischen Zoster-Infektion sind brennende oder stechende Schmerzen, Hauteffloreszenzen, Sensibilitätsstörungen und selten auch motorische Ausfälle oder Fieber. Die Ausbreitung des Exanthems entspricht meistens einem oder mehreren Dermatomen. Nach 7–10 Tagen verkrusten die Effloreszenzen, ab diesem Zeitpunkt sind sie auch nicht mehr infektiös. Meist sind thorakale und lumbale radikuläre Segmente betroffen. Bei ca. 10 % der Fälle findet sich eine Infektion im Gesichtsbereich (meist V1-Region des N. trigeminus).
Der Schmerz während der akuten Zoster-Phase soll nicht mit einer postherpetischen Neuropathie (PHN) verwechselt werden, die die häufigste Komplikation (bei ca. 20 %) der Zoster-Neuritis darstellt. Sie ist als anhaltender Schmerz für mindestens 90 Tage nach Beginn der Infektion definiert. PHN kann auch erst Monate nach einer akuten Neuritis auftreten. Unter-60-Jährige haben ein deutlich geringeres Risiko (ca. 2 %), eine PHN zu entwickeln.
Die PCR-Untersuchung der Effloreszenzen, des Serums oder des Liquors ist die sensitivste Methode, die zu der richtigen Diagnose führt.
Therapie: Patient:innen mit einer akuten Zoster-Infektion sollen innerhalb der ersten 72 Stunden antiviral behandelt werden. Bei einer unkomplizierten Erkrankung werden Valaciclovir (3-mal1000 mg/d p. o. für 7 d), Brivudin, Famciclovir oder Aciclovir empfohlen. Komplizierte Fälle oder immunsupprimierte Patient:innen sollen mit Aciclovir i. v. (10 mg/kg KG) über 10–14 d oder mit Foscarnet behandelt werden. Eine zusätzliche Gabe von Kortikosteroiden kann die akute Schmerzphase verkürzen. Zwar gibt es hierzu keine generelle Empfehlung, eine Ausbreitung der Erkrankung unter Prednisolon ist bei gleichzeitiger Gabe von Virostatika jedoch sehr unwahrscheinlich. Gegen die Schmerzsymptomatik in der Akutphase kann auch eine NSAR-Gabe erfolgen. Große Vorsicht ist jedoch auf Grund der möglichen akuten Niereninsuffizienz (v. a. Kombination NSAR und Virostatika) gegeben.
Die Schmerzintensität in der Akutphase der Infektion ist ein Risikofaktor für die Entstehung einer PHN. Aus diesem Grund sind eine konsequente Schmerztherapie und eine frühe antivirale Therapie entscheidend. Neuropathische Schmerzen sollen während der akuten Neuritis oder bei einer PHN leitliniengerecht wie sonstige neuropathische Schmerzen behandelt werden.
Da sich die Schmerztherapie oft schwierig gestaltet, ist eine Infektionsprophylaxe sehr wichtig. Eine aktive Immunisierung reduziert sowohl die Inzidenz der Erkrankung als auch die Ausprägung der Zoster-Neuritis. Zur Verfügung stehen der rekombinante Zoster-Impfstoff und ein Lebendimpfstoff.