Systemische Therapie der atopischen Dermatitis
Die atopische Dermatitis (AD) ist eine mit starkem Juckreiz assoziierte chronisch entzündliche Hauterkrankung. Emollienzien stellen die Basis der Therapie der AD dar, und viele Patienten mit milden bis moderaten Krankheitsverläufen finden damit, mit topisch angewandten antiinflammatorischen Substanzen, Phototherapie sowie dem Vermeiden von Auslösern der AD das Auslangen.1 Kann die AD allerdings mit topischer Therapie nicht ausreichend kontrolliert werden, so ist der Einsatz systemischer Therapien erforderlich, um die Entzündung der Haut zu kontrollieren, Symptome zu lindern, Flares zu verhindern und die Lebensqualität der Patienten zu verbessern.
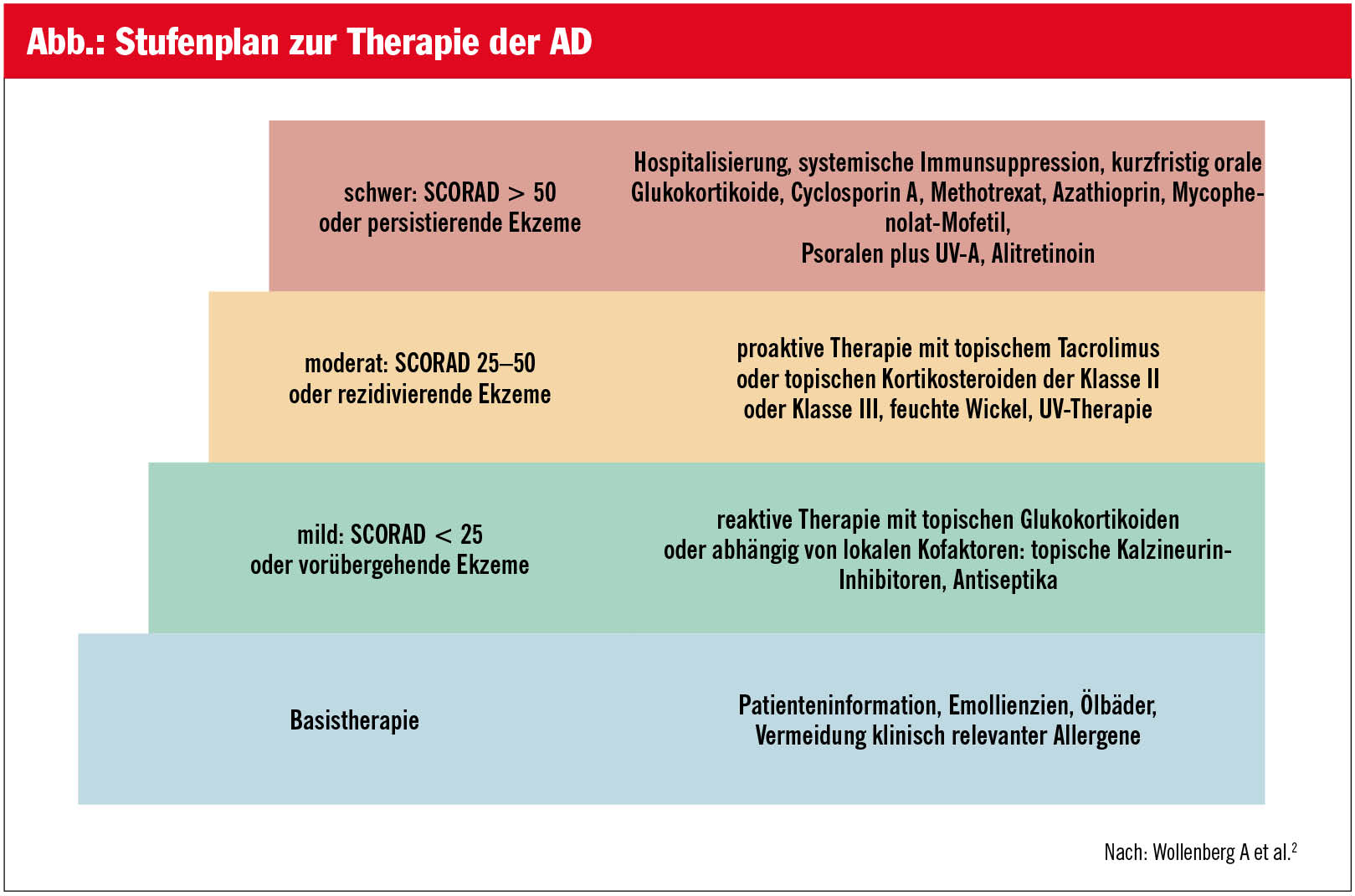
Die European Task Force on Atopic Dermatitis (ETFAD)/European Academy of Dermatology and Venereology (EADV) hat 2016 ein Positionspapier zum Management der AD publiziert, in dem ein stufenweises Vorgehen entsprechend der Schwere der Erkrankung, gemessen am SCORAD (Score of Atopic Dermatitis), empfohlen wird (Abb.).2
Systemische Immunsuppression
Obwohl sich in den ETFAD/EADV-Empfehlungen bei schwerer AD systemisch verabreichtes Cyclosporin A (CsA), Methotrexat (MTX) Azathioprin (AZA) sowie Mycophenolat-Mofetil (MM) erwähnt werden, ist in Europa nur CsA in dieser Indikation zugelassen. So kommt auch ein systematischer Review zu systemischen Therapien bei moderater bis schwerer AD zu dem Schluss, dass nur für CsA ausreichende Evidenz für eine starke Empfehlung vorliegt.3 Trotzdem liegen auch für die anderen Substanzen Daten aus klinischen Studien vor.
Zu CsA zeigen die gepoolten Daten von 12 Studien, dass niedrigdosiertes CsA (3 mg/kg) die Schwere der AD nach 2 Wochen Therapie um 22 % und hochdosiertes CsA (≥ 4 mg/kg) um 40 % reduziert.4 Nach 6 bis 8 Wochen CsA-Therapie lag die relative Wirksamkeit bei 55 %. In einer retrospektiven Untersuchung wurden Therapiedauer und Gründe für den Abbruch einer Therapie mit CsA analysiert.5 Dabei hat sich gezeigt, dass nach 1 Jahr noch 34 % der Patienten mit AD CsA eingenommen hatten und nach 6 Jahren noch 4 %. Gründe für das Beenden der Therapie waren Kontrolle der AD (26,4 %),Nebenwirkungen (22,2 %), Wirkungslosigkeit (16,3 %). Höheres Alter der Patienten war sowohl mit verkürzter Therapie-dauer aufgrund von Remission als auch aufgrund von Nebenwirkungen assoziiert.
MTX ist eine effektive Substanz zur Behandlung chronisch entzündlicher Erkrankungen wie Psoriasis oder rheumatischer Arthritis und wurde auch in der Indikation AD geprüft. So war in einer retrospektiven Studie nach 12 Wochen niedrigdosierter MTX-Therapie der SCORAD um 44,3 % gesenkt und die Lebensqualität der Patienten deutlich verbessert.6 Ein ähnliches Ergebnis wurde in einer randomisierten, kontrollierten Vergleichsstudie von MTX und AZA gezeigt, bei der in beiden Studienarmen nach 12 Wochen eine Reduktion im SCORAD von 42 % beobachtet wurde.7 Eine rezent publizierte Studie, in der MTX mit CsA verglichen worden war, hat gezeigt, dass MTX in der Dosierung von 15 mg/Woche bei moderater bis schwerer AD weniger effektiv ist als CsA 2,5 mg/kg/Tag; wird die MTX-Dosis jedoch auf 25 mg/Woche erhöht, war MTX CsA überlegen.8 Auch das Sicherheitsprofil von MTX war in dieser Studie günstiger als jenes von CsA.
Der Vergleich von Mycophenolat und CsA in der Langzeittherapie von Patienten mit schwerer AD hat gezeigt, dass Mycophenolat in der Erhaltungstherapie ebenso effektiv ist wie CsA, die Wirkung im Vergleich zu CsA allerdings verzögert eintritt.9 Im Gegenzug hält die Remission nach Absetzen von Mycophenolat länger an.
Systemische Steroide sollten laut ETFAD/EASD-Positionspapier und International-Eczema-Council-Consensus-Statement aufgrund des ungünstigen Nutzen-Risiko-Profils nur in wenigen ausgewählten Fällen und dann nur kurz zum Einsatz kommen.2, 10
Biologika bei AD
Monoklonale Antikörper, die an spezifische Zytokine binden, haben sich bei verschiedenen Erkrankungen wie Psoriasis oder rheumatoider Arthritis als wirksam und gut verträglich erwiesen. Eine Reihe von Studien zur AD wurde mit Biologika, die in anderen Indikationen wirksam sind, durchgeführt. Allerdings erwiesen sich Substanzen wie Infliximab, Etanercept, Rituximab oder Ustekinumab entweder als ineffektiv, oder die Datenlage ist für einen eindeutigen Wirkungsnachweis nicht ausreichend.
Mit dem kürzlich zur Behandlung der schweren AD zugelassenen monoklonalen Antikörper Dupilumab, einem Inhibitor der Interleukine IL-4 und IL-13, steht nun erstmals auch in dieser Indikation ein Biologikum zur Verfügung. Die Zulassung von Dupilumab erfolgte auf Basis der Ergebnisse zweier Phase-III-Studien (SOLO 1, SOLO 2), in die insgesamt 1.379 Patienten mit moderater bis schwere AD inkludiert wurden.11 Die Studien zeigten nahezu identische Ergebnisse. Von den Patienten, die wöchentlich oder jede zweite Woche mit Dupilumab behandelt worden waren, erreichten zwischen 36 und 38% das Therapieziel, die Reduktion des Schweregrads der Krankheitssymptome um mindestens zwei IGA-Skalenpunkte und damit weitgehende Beschwerdefreiheit. In den Placeboarmen der beiden Studien war dies nur bei 10 beziehungsweise 8 % der Patienten der Fall. Darüber hinaus zeigten deutlich mehr Patienten, die mit Dupilumab behandelt worden waren, eine 75%ige Reduktion der Hautläsionen (EASI-75). Zusätzlich waren bereits 2 Wochen nach Therapiebeginn der Juckreiz, die innere Unruhe und Depressionen vermindert, während sich gleichzeitig die Schlaf- und Lebensqualität verbesserte. Nebenwirkungen unter Dupilumab waren Hautreaktionen an der Einstichstelle sowie Konjunktivitiden.
Den Pruritus stoppen
Juckreiz ist ein für Patienten sehr belastendes Symptom der AD. Eine Behandlung des Pruritus soll den Teufelskreis von Jucken und Kratzen, der eine zusätzliche Schädigung der Hautbarriere zur Folge hat, durchbrechen. Ein wichtiges pruritusinduzierendes Zytokin ist IL-31, das in der Haut von Patienten mit AD überexprimiert ist. Nemolizumab ist ein monoklonaler Antikörper, der die Signalwege von IL-31 unterbricht.
In einer Phase-II-Studie konnte nun die juckreizstillende Wirkung von Nemolizumab an 264 Patienten mit schwerer AD nachgewiesen werden.12 Nach den in vierwöchigem Abstand verabreichten subkutanen Nemolizumab-Injektionen kam es dosisabhängig zu einer signifikanten Reduktion des Pruritus. Unter der niedrigsten Dosierung von 0,1 mg/kg ging der Juckreiz auf der VAS um 43,7 % zurück, unter der zweithöchsten Dosierung von 0,5 mg/kgbesserte sich der VAS-Wert um 59,8 %, und unter der höchsten Dosierung von2,0 mg/kg kam es zu einer Verbesserung um 63,1 %. Im Placeboarm kam es zu einer leichten Verbesserung um 20,1 %. Darüber hinaus kam es unter den drei Nemolizumab-Dosierungen zu einer Reduktion im EASI-75 um 23 %, 42,3 % respektive 40,9 %, während es unter Placebo 26,6 % waren. Die Autoren schließen aus diesen Daten, dass die Blockade von IL-31 eine effektive Linderung des Pruritus bei AD bewirkt. Weiterführende Studien werden empfohlen.
Literatur:
1 Simpson EL et al., J Am Acad Dermatol 2017; 77(4):623–633
2 Wollenberg A et al., J Eur Acad Dermatol Venereol 2016; 30(5):729–47
3 Roekevisch E et al., J Allergy Clin Immunol 2014; 133(2):429–38
4 Schmitt J et al., J Eur Acad Dermatol Venereol 2007; 21(5):606–19
5 van der Schaft J et al., Br J Dermatol 2015; 172(6):1621–7
6 Lyakhovitsky A et al., J Eur Acad Dermatol Venereol 2010; 24(1):43–9
7 Schram ME et al., J Allergy Clin Immunol 2011; 128(2):353–9
8 Goujon C et al., J Allergy Clin Immunol Pract 2017; [Epub ahead of print]
9 Haeck IM et al., J Am Acad Dermatol 2011; 64(6):1074–84
10 Drucker AM et al., Br J Dermatol 2017; [Epub ahead of print]
11 Simpson EL et al., N Engl J Med 2016; 375:2335–2348
12 Ruzicka T et al., N Engl J Med 2017; 376:826–835