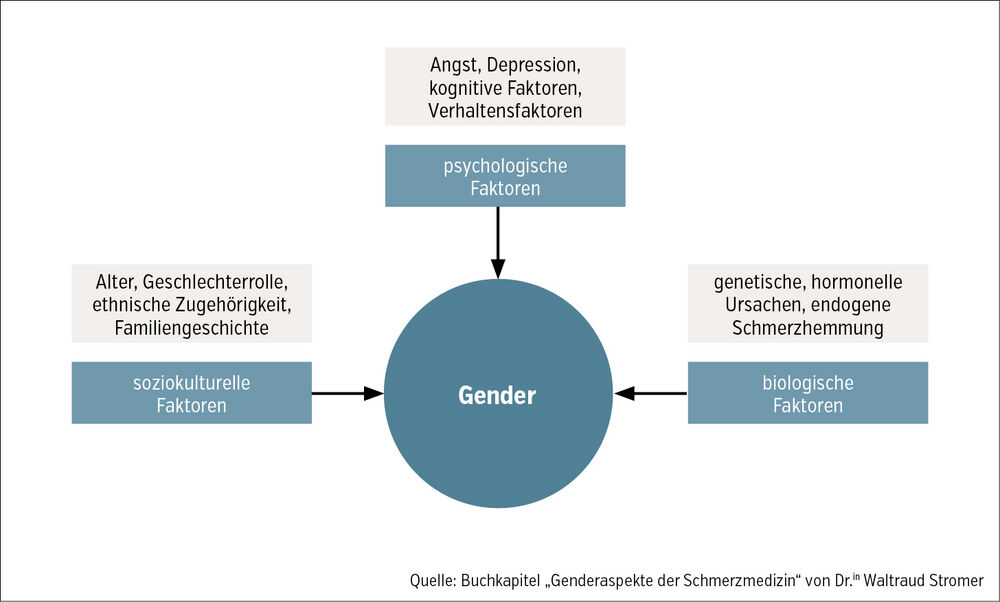
Unterschiede zwischen den Geschlechtern
Unter standardisierten Bedingungen reagieren Frauen und Männer unterschiedlich auf einen Schmerzreiz. So schätzten Frauen die Schmerzintensität bei Hitze- oder Druckreizen bei experimentellen Versuchen höher ein und hielten den Schmerz weniger lange aus, außerdem wurden niedrigere Reize bereits als schmerzhaft empfunden. Demzufolge scheinen Frauen biologisch gesehen eine niedrigere Schmerzschwelle aufzuweisen und Schmerzen stärker als Männer zu empfinden. Epidemiologische Studien weisen fast immer nach, dass Frauen häufiger Schmerzen haben und öfter an einer Schmerzerkrankung leiden als Männer. Insbesondere chronischer Spannungskopfschmerz, rheumatoide Arthritis, das irritable Darmsyndrom, Fibromyalgie, Spannungskopfschmerz und Migräne sind bei Frauen deutlich häufiger zu finden. Früher wurden bei der Sozialisation von Männern Schmerzäußerungen als Zeichen von Schwäche gesehen, weshalb sie dazu angehalten wurden, diese zu negieren. Frauen wurden hingegen eher zu Gefühlsäußerungen ermutigt; mittlerweile spielen diese Aspekte jedoch eine eher untergeordnete Rolle. Vielmehr scheint eine Kombination biologischer (genetischer/hormoneller), psychologischer und soziokultureller Faktoren die Ursache zu sein, dass Frauen das stärker mit Schmerz assoziierte Geschlecht sind (Abb.).
Neurobiologische Faktoren
Die Schmerzsensoren scheinen bei Frauen empfindlicher zu sein als bei Männern. Es gibt auch Hinweise, dass bei ihnen die Schmerzverarbeitung im ZNS deutlich sensibler ist, wodurch der Prozess der Chronifizierung begünstigt wird. Untersuchungen zur Summation von Schmerzwahrnehmung konnten zeigen, dass bei kurzfristig aufeinanderfolgenden Reizen die Schmerzwahrnehmung bei Frauen deutlich zunimmt. Diese Hypersensibilisierung ist ebenso ein Risikofaktor bei der Schmerzchronifizierung. Frauen leiden auch 6-mal häufiger an einem chronischen Schmerzsyndrom als Männer. Beim Gleichgewicht zwischen zentralnervöser Erregung und Hemmung sind u. a. GABA- und NMDA-Rezeptoren beteiligt, die von Sexualhormonen beeinflusst werden. GABA ist der wichtigste hemmende Neurotransmitter des menschlichen Nervensystems, während Glutamat (bindet an NMDA-Rezeptor) eine erregende Wirkung hat. Östrogene wirken an beiden Rezeptortypen exzitatorisch, während Progesteron Dauer und Intensität der GABA-Wirkung verstärkt und einen anxiolytischen, hypnotischen und antikonvulsiven Effekt hat. Testosteron kann über seine Metabolite sowohl GABAerg als auch über die Blockade der NMDA-Rezeptoren antiexzitatorisch wirken.
Sexualhormone
Hormone sind nicht isoliert zu betrachten, von Bedeutung ist die relative Konzentration der Hormonspiegel zusammen mit ihrer dynamischen Veränderung. Androgene scheinen dabei eher schmerzhemmende Effekte zu haben und eine Chronifizierung zu unterdrücken. Progesteron verringert die Aktivität des Immunsystems, während Östrogene dessen Aktivität eher fördern und proinflammatorisch wirksam sind. Störungen des Immunsystems sind auch häufiger bei Frauen zu finden, darüber hinaus dürften Östrogene die Entwicklung chronischer Schmerzen begünstigen.
Schwangerschaft
Man vermutet, dass während der Schwangerschaft das endogene Hemmsystem unter den hormonellen Bedingungen immer stärker wird, womit Frauen ermöglicht wird, den Geburtsschmerz auszuhalten. Auch Oxytocin könnte eine Rolle bei der Schmerzhemmung und der Verhinderung der Chronifizierung spielen. Progesteron verstärkt die Dauer und Intensität der hemmenden GABA-Wirkung. Der steigende Progesteronspiegel in der Schwangerschaft dürfte mit der Schmerzschwellenzunahme in der Schwangerschaft zusammenhängen und hat eine erhöhte Produktion von Enkephalinen und Endorphinen zur Folge. Die steigenden Opioidspiegel lassen sich auch im Blutplasma nachweisen, die kurz nach der Geburt wieder abfallen.
Pharmakokinetik und Pharmakodynamik
Das individuelle Ansprechen auf eine Substanz hängt von pharmakokinetischen und pharmakodynamischen Faktoren ab. Geschlechtsspezifische Unterschiede in der Verteilung von Arzneimitteln beruhen auf Abweichungen in der Körpergröße und Muskelmasse sowie im Fett- und Wassergehalt, die durch Sexualhormone gesteuert werden. Frauen haben einen deutlich höheren Fettanteil, während Männer mehr Muskelgewebe und mehr Wasser aufweisen. Dadurch ergibt sich ein längerer Verbleib lipophiler Arzneimittel im Körper von Frauen. Diese müssen erst aus dem Fettgewebe metabolisiert werden, wodurch ein zeitverzögerter Abbau erfolgt. Wirkung und etwaige Nebenwirkungen halten dadurch länger an. Für hydrophile Substanzen gilt Gegenteiliges, die Plasmakonzentration von wasserlöslichen Arzneien ist bei Männern niedriger als bei Frauen.
Geschlechtsspezifische pharmakologische Unterschiede betreffen vorrangig die Dosierung von Analgetika. Beispielsweise wird Acetylsalicylsäure bei Frauen um 30–40 % langsamer metabolisiert als bei Männern. Die hepatische Clearance durch Leberenzyme ist bei Frauen um ca. 30 % niedriger für Opioide und NSAR sowie um 50 % niedriger für Paracetamol. Die Aktivität dieser Enzyme wird von Zyklusphase, oraler Kontrazeption oder Schwangerschaft beeinflusst, eine Dosisanpassung orientiert sich daher an klinischen Zeichen. Zu beachten ist, dass die Analgesie durch Opioide bei Frauen langsamer anschlägt, später nachlässt und dadurch 2–3-mal potenter als bei Männern wirkt. Frauen reagieren auch häufiger mit Übelkeit.
Klinische Implikationen
Bis 1988 wurden die meisten Medikamentenstudien wegen möglicher Schwangerschaften sowie Einflüssen von Hormonschwankungen ausschließlich an Männern durchgeführt, obwohl der Medikamentenverbrauch bei Frauen deutlich höher ist. Trotzdem werden auch heute noch an Männern gewonnene Studienergebnisse auf Frauen übertragen, was unangemessene Dosierungen und Unverträglichkeiten zur Folge haben kann. Frauen haben ein um 50–70 % erhöhtes Risiko für unerwünschte Arzneimittelreaktionen, wodurch häufiger Therapieabbrüche beobachtet werden.
Weitere Forschung könnte dazu beitragen, unterschiedliche Therapieansätze bei Frauen und Männern zu entwickeln. Aus schmerzmedizinischer Sichtweise gibt es noch einige offene Fragestellungen zu klären, wie z. B. die Rolle der einzelnen Sexualhormone bei starken klinischen Schmerzzuständen und im Prozess der Schmerzchronifizierung oder die Bedeutung verschiedener Faktoren als wichtige Genderaspekte. Darüber hinaus sind hormonelle Behandlungsstrategien bei der Therapie chronischer Schmerzsyndrome denkbar; eventuell wäre eine Antiöstrogentherapie bei rheumatoider Arthritis oder Fibromyalgie wirksam.