Ende 2023 berichteten chinesische Medien über eine auffallende Zunahme zunächst unklarer Pneumonien, wobei ein neuer „Superbug“ befürchtet wurde. Später wurden diese jedoch als Mykoplasmen-Pneumonien identifiziert. Diese deutliche Häufung an Mykoplasmeninfektionen wurde in verschiedenen Regionen weltweit beobachtet. In Europa vermeldete die Schweiz als eines der ersten Länder ab Herbst 2023 eine ungewöhnliche Häufung atypischer Pneumonien.
Belastbare Zahlen für Europa sind nur eingeschränkt verfügbar, da es kaum Länder mit flächendeckenden Meldesystemen hinsichtlich Mykoplasmeninfektionen gibt. Eine Ausnahme stellt das deutsche Bundesland Sachsen mit entsprechender Meldepflicht dar. Wurden hier 2019, also noch vor der Corona-Pandemie, 1.238 Fälle gemeldet, waren es 2023 bereits 2.019 Fälle und 2024 weit über 12.000 Fälle.
Um diese Entwicklung einzuordnen, ist einerseits zu betonen, dass es auch in den letzten Jahrzehnten immer wieder – üblicherweise alle 3 bis 5 Jahre – Mykoplasmen-Epidemien gab, andererseits gehen die in den letzten 1,5 Jahren beobachteten Zahlen deutlich über das erwartbare Ausmaß hinaus. Seit Ende 2023 haben wir es jedenfalls auch in Mittel- und Westeuropa mit einer erneuten Mykoplasmen-Epidemie zu tun.
Wie bei anderen respiratorischen Infektionen sind diese überschießenden Erkrankungszahlen auf die nur minimale Zirkulation der Erreger in den Jahren 2020 bis 2022 aufgrund von Maßnahmen während der COVID-19-Pandemie zurückzuführen. Durch die abnehmende Herdenimmunität konnten sich die Erreger nach Aufhebung der Kontaktrestriktionen rascher in der Bevölkerung ausbreiten. Auffallend ist der spätere Anstieg der Infektionszahlen durch Mykoplasmen als bei anderen Bakterien wie Pertussis oder Pneumokokken.
Gründe dafür könnten u.a. eine länger nachwirkende Herdenimmunität nach der letzten Mykoplasmen-Epidemie 2019/2020 sein, aber auch das langsamere Erregerwachstum, die längere Inkubationszeit und die Notwendigkeit eines engeren Kontaktes für eine Transmission. Bisher nicht ausreichend bestätigte unter Expert:innen diskutierte Theorien sind eine alterierte Immunantwort nach durchgemachter schwerer COVID-19-Infektion, die den Boden für gehäufte respiratorische Infekte bereitet, oder auch ein alteriertes respiratorisches Mikrobiom mit besseren Wachstumsbedingungen für z.B. Mykoplasmen.
Atypische Pneumonie-Erreger
Mykoplasmen zählten auch schon lange vor der aktuellen epidemiologischen Situation zu den häufigsten bakteriellen Erregern ambulant erworbener Pneumonien – wenn auch weit abgeschlagen hinter den Pneumokokken. Mykoplasmen gelten gemeinhin als atypische Pneumonie-Erreger, was vor allem auf wesentliche Unterschiede zu den Pneumokokken als klassischen Erregern zurückzuführen ist. So sind Mykoplasmen beispielsweise zellwandlose Bakterien, was mit einer fehlenden Darstellbarkeit in der Gram-Färbung einhergeht und eine intrinsische Resistenz gegenüber Penicillinen mit sich bringt (Tab. 1).
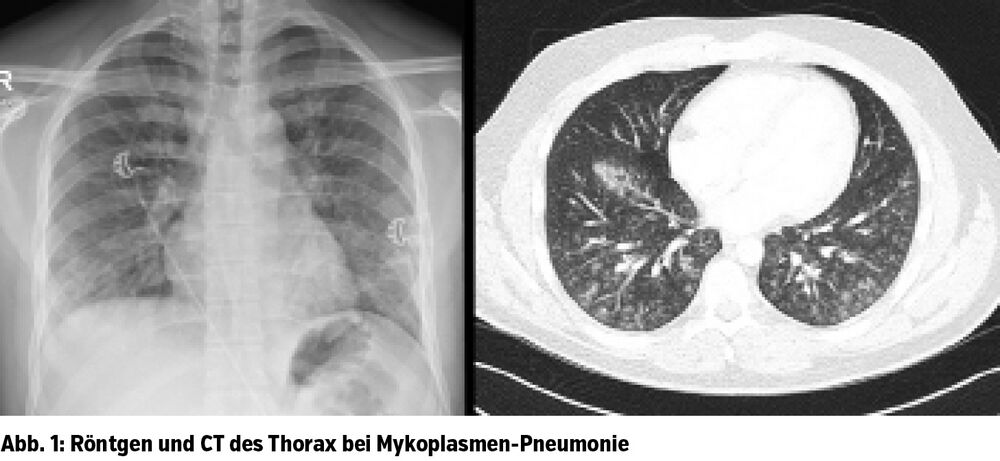
Wie in der Tabelle 1 erwähnt, stellen sich Pneumonien durch Mykoplasmen radiologisch oftmals anders dar als andere bakterielle Pneumonien – siehe auch Abbildung 1. So sind häufiger eine retikulonoduläre Zeichnungsvermehrung, zentrilobuläre Noduli und peribronchiale Verdichtungen als Ausdruck einer bronchiolären Beteiligung und auch Milchglasverschattungen nachweisbar. Die Veränderungen sind teilweise diskret, manchmal nur in der Computertomografie auszumachen. Dichte Konsolidierungen und begleitende Pleuraergüsse sind vergleichsweise seltener. Zu betonen ist aber, dass die Radiologie – trotz beschriebener möglicher Besonderheiten – allenfalls hinweisend auf sogenannte atypische Erreger sein kann, jedoch niemals einen sicheren Rückschluss auf einen zugrunde liegenden Erreger zulässt!
Ebenso eine Besonderheit von Mycoplasma-pneumoniae-Infektionen ist das gehäufte Auftreten extrapulmonaler Manifestationen. So kann es durch autoimmune und vaskulitische Mechanismen zu neurologischen Manifestationen wie Meningitis, Enzephalitis oder Guillain-Barré-Syndrom kommen, aber auch Exantheme, Myo- oder Perikarditiden, hämolytische Anämien, Arthritiden bzw. Arthralgien, Nephritiden oder gastrointestinale Symptome können vorkommen.
In der Diagnostik hat die Molekulargenetik die Serologie abgelöst. Die PCR (Polymerase-Kettenreaktion) aus Nasopharyngealabstrich, Sputum oder Bronchialsekret gilt als Goldstandard, während die serologische Diagnostik oft nur durch einen Titeranstieg im Verlauf aussagekräftig ist. Laborchemisch finden sich oft hohe CRP-(C-reaktives-Protein-)Werte bei vergleichsweise niedrigen PCT-(Procalcitonin-)Werten. Eine CRP-PCT-Ratio > 400 mg/µg gilt neben anderen genannten Punkten als hinweisend auf eine atypische Pneumonie.
Therapeutische Überlegungen
Therapeutisch ist die schon erwähnte intrinsische Resistenz gegenüber Penicillinen zu berücksichtigen und vor allem in der empirischen Therapie zu bedenken. Laut der deutsch-österreichischen S3-Leitlinie zur ambulant erworbenen Pneumonie ist bei leichtgradiger, ambulant geführter Pneumonie Amoxicillin als Mittel der ersten Wahl empfohlen. Damit sind vor allem Pneumokokken als häufigste Erreger optimal abgedeckt, nicht aber Mykoplasmen. Erst als 2.Wahl sind Doxycyclin, Azithromycin, Levofloxacin oder Moxifloxacin empfohlen, die alle eine gute Mykoplasmen-Wirksamkeit haben. Allerdings sind Pneumokokken in Österreich mittlerweile in ca. 10 % der Fälle makrolidresistent. Zudem haben Fluorchinolone zwar eine ausgezeichnete Wirksamkeit, allerdings gibt es von der Europäischen Arzneimittel-Agentur (EMA) Warnungen vor lebensqualitätbeeinträchtigenden, anhaltenden und möglicherweise irreversiblen Nebenwirkungen an Bewegungsapparat und Nervensystem.
Als Conclusio ist festzuhalten, dass in Zeiten von Epidemien Pneumonien durch entsprechende Erreger erwartet werden müssen und diese in empirische Behandlungskonzepte einzuschließen sind. Somit sind wir aktuell auch in Österreich angehalten, bei entsprechender Vortestwahrscheinlichkeit (vgl. Tab.1) durchaus teilweise auf die erwähnten Antibiotika der 2. Wahl zurückzugreifen bzw. diese in der empirischen Therapie hinzuzufügen (z. B. Amoxicillin plus Azithromycin). Bei schwerer verlaufenden Pneumonien mit Hospitalisierung soll laut S3-Leitlinie ohnehin ein Makrolid den Betalaktamen bzw. Cephalosporinen in der empirischen Therapie zugegeben werden.
Wurde Mycoplasma pneumoniae mittels Erregerdiagnostik bestätigt, sind Doxycyclin oder Azithromycin als 1. Wahl in der kalkulierten Therapie zu sehen. Moxifloxacin oder Levofloxacin bleiben auch hier 2. Wahl. Die Therapiedauer beträgt im Normalfall 5–7 Tage, nur in Ausnahmefällen länger. Die früher gelebte Praxis, bestätigte Mykoplasmen-Infektionen grundsätzlich über mehrere Wochen antibiotisch zu behandeln, wurde aufgrund fehlender Evidenz mittlerweile verlassen.