Trotz zunehmender Therapieoptionen ist die Herzinsuffizienz nach wie vor unterdiagnostiziert und untertherapiert. Registerdaten zeigten zuletzt sogar einen erneuten Anstieg der Inzidenz und Mortalität von Herzinsuffizienz-patient:innen.1 Die Beobachtung ist multi-faktoriell beeinflusst wie u. a. durch eine Verbesserung der Akutversorgung von Patient:innen mit akutem Koronarsyndrom, durch eine zunehmend optimierte Therapie von Krankheiten, die mittelfristig zur Herzinsuffizienz führen können (z. B. Kardioonkologie), oder durch die Schärfung des Bewusstseins für die Diagnosestellung vor allem der Herzinsuffizienz mit erhaltener linksventrikulärer Auswurffraktion. Die Daten müssen aber als Warnsignal interpretiert werden, um unsere Aufmerksamkeit für die Erkrankung und ihre Therapie zu schärfen. Denn die Herzinsuffizienz hat eine schlechtere Prognose als viele Krebserkrankungen, und eine verzögerte Therapieinitiierung beeinflusst den Krankheitsverlauf nachweislich negativ.2–4
Im Sinne des Screenings für Patient:innen mit typischen Symptomen (Dyspnoe, Ödeme, Leistungsknick), der frühen Diagnosestellung und der optimierten Versorgung wurde von der Arbeitsgruppe für Herzinsuffizienz der Österreichischen Kardiologischen Gesellschaft in Kooperation mit der Österreichischen Gesellschaft für Allgemein- und Familienmedizin ein Positionspapier entwickelt, das die unterschiedlichen Versorgungsebenen des Gesundheitssystems berücksichtigt und eine Orientierung geben soll, den Krankheitspfad unsere Patient:innen positiv zu beeinflussen.5 Ungeachtet des Krankheitsbeginns – chronisch schleichend oder akut – ist die rasche Therapieinitiierung unabdingbar, um das Outcome unserer Patient:innen zu verbessern.2
Ziel der evidenzbasierten Therapie ist die Verbesserung von Symptomen und der Lebensqualität, die Verringerung von Hospitalisierungen sowie die Verhinderung des vorzeitigen Todes. Hierzu verfügbare Ansätze im multidisziplinären Setting umfassen primär die medikamentöse Therapie, aber auch die Device-Therapie, weitere invasive Eingriffe (z. B. gezielte Klappentherapie), die Optimierung potenzieller Komorbiditäten, die kardiale Rehabilitation und letztlich im fortgeschrittenen Stadium für einzelne Patient:innen die Kunstherz-Therapie (VAD)oder die Herztransplantation.
Formen der Herzinsuffizienz
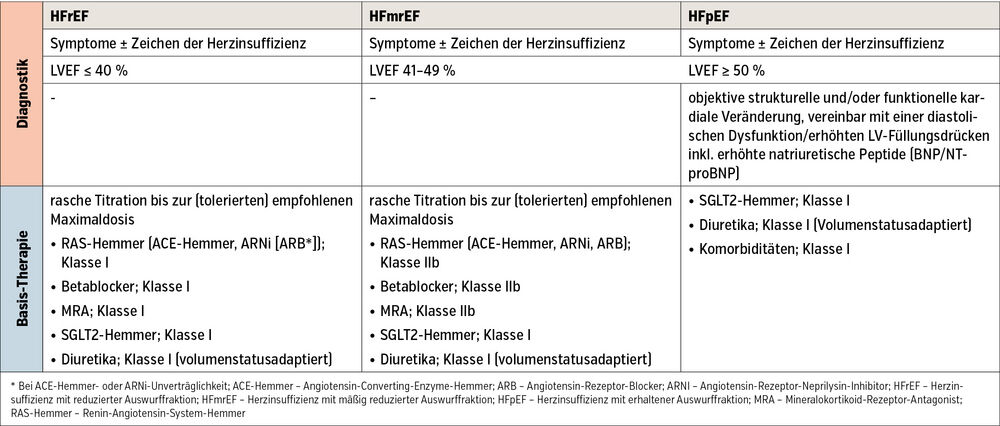
Trotz zunehmend phänotypenorientiertem individualisiertem Therapiemanagement basiert die von der Europäischen Gesellschaft für Kardiologie empfohlene leitliniengerechte Herzinsuffizienztherapie primär auf der linksventrikulären systolischen Funktion (Tab.), wobei 3 Gruppen unterschieden werden:
- Herzinsuffizienz mit reduzierter linksventrikulärer Auswurffraktion (HFrEF: LVEF ≤40%)
- Herzinsuffizienz mit mäßiggradig reduzierter Auswurffraktion (HFmrEF: LVEF 41–49%) und
- Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF: LVEF ≥50%).
Medikamentöse Therapie
HFrEF
Die größte Evidenz und das breiteste Therapieangebot gibt es für Patient:innen mit HFrEF. Die Basistherapie der HFrEF umfasst 4 Therapiegruppen, die jede:r Patient:in in maximal tolerierter Dosierung erhalten soll (Klasse-I-Indikation): i) Renin-Angiotensin-System-Blockade mit einem Angiotensin-Rezeptor-Neprilysin-Inhibitor (ARNi) oder einem ACE-Hemmer (bei Unverträglichkeit Angiotensin-Rezeptor-Blocker [ARB]), ii) Betablocker, iii) Mineralokortikoid-Rezeptor-Antagonist (MRA) und SGLT2-Hemmer. Die diuretische Therapie ist in der HFrEF eine symptomatische Therapie, die das Überleben der Patient:innen nicht nachweislich verbessert, und sollte somit orientiert am Volumenstatus regelmäßig (re)evaluiert und adaptiert werden.4
Spätestens mit den Daten von STRONG-HF2 haben wir Evidenz, dass insbesondere in der vulnerablen Phase einer Hospitalisierung aufgrund einer De-novo-Herzinsuffizienz oder einer akut dekompensierten chronischen Herzinsuffizienz die rasche, intramurale Initiierung und Titration der gezielten „4-Säulen-Therapie“ sicher ist und einen Überlebensvorteil bringt.
Für die klinische Praxis gilt, dass Patient:innen zum Entlassungszeitpunkt nach Möglichkeit auf zumindest 50 % der empfohlenen maximalen Therapiedosis sind und die weitere Titration im Rahmen engmaschiger ambulanter Verlaufskontrollen innerhalb der ersten 6 Wochen erfolgt.³
HFmrEF
Für die HFmrEF gelten die Therapiesäulen der HFrEF mit starker Empfehlung für die SGLT2-Hemmer und abgeschwächter Evidenz für RAS-Blockade, Betablocker und MRA.4
HFpEF
Die geringste gezielte Therapieoption gibt es nach wie vor für Patient:innen mit HFpEF. Hier konnte lediglich für die SGLT2-Hemmer Dapagliflozin und Empagliflozin eine signifikante Hospitalisierungs- oder kardiovaskuläre Mortalitätsreduktion gezeigt werden, sodass diese Präparate seit 2023 eine Klasse-I-Empfehlung zur Therapie der HFpEF-Patient:innen haben.3 Daneben profitieren diese Patient:innen insbesondere von einem optimierten Volumenstatus (diuretische Therapie) und der Kontrolle möglicher Komorbiditäten.3, 4
Therapie häufiger Komorbiditäten
Eisenmangel
Viele Patient:innen mit Herzinsuffizienz leiden an Eisenmangel – in der Herzinsuffizienz definiert als Ferritin <100ng/ml oder Ferritin 100–299ng/ml und Transferrinsättigung <20% –, der ungeachtet einer kombinierten Anämie den Krankheitsverlauf negativ beeinflusst. Für Patient:innen mit einer LVEF <45% empfehlen daher die aktuellen Leitlinien die intravenöse Eisensubstitution (i. v. Eisencarboxymaltose, i. v. Eisen-Derisomaltose, keine orale Eisentherapie!) zur Verbesserung von Symptomen und Lebensqualität und zur Reduktion von Hospitalisierungen. Eine Übersicht zur Eisentherapie im niedergelassenen Bereich findet sich unter www.eisencheck.at.
Hyperkaliämie
Generell gilt es bei der Herzinsuffizienz, nach Möglichkeit die Reduktion, das Pausieren oder gar Absetzen der mit einem Überlebensvorteil verbundenen herzinsuffizienzspezifischen Therapie zu vermeiden. Das Auftreten einer Hyperkaliämie gibt u. a. oft den Impuls der Medikamentenreduktion. Neben der Ernährungsberatung stellt hier der transiente oder langfristige Einsatz sogenannter Kaliumbinder (z. B. Patiromer, oder Natrium-Zirkonium-Cyclosilikat) eine gute Möglichkeit, den Kaliumspiegel unter Beibehaltung der Therapie zu kontrollieren.
Ausblick: Adipositas, Diabetes oder chronische Niereninsuffizienz
Im Sinne der Komorbiditäten-Optimierung gibt es für Patient:innen mit HFpEF und Adipositas erste Daten, die eine signifikante Gewichtsreduktion und symptomatische Verbesserung unter der Therapie mit einem GLP-1-Rezeptoragonisten (GLP-1-RA) zeigen.6 Ob diese Therapie auch einen Einfluss auf das Outcome dieser Patient:innen hat, wird voraussichtlich zum Ende des Jahres der SUMMITTrial zeigen (NCT04847557). Für Patient:innen mit Herzinsuffizienz und reduzierter systolischer Funktion ist – basierend auf der aktuellen Evidenz – im Zusammenhang mit dem Einsatz von GLP-1-RA Vorsicht geboten. Hier gibt es das vorbehaltliche Signal, dass die Therapie mit einer gesteigerten Event-Rate einhergeht (rhythmologische Events, Hospitalisierung, Mortalität).7, 8 Für Finerenon, ein nichtsteroidaler selektiver Mineralokortikoid-Rezeptor-Antagonist, konnte bei Patient:innen mit T2DM und chronischer Niereninsuffizienz gezeigt werden, dass die Therapie ungeachtet einer vorbekannten kardialen Erkrankung zur Reduktion von Herzinsuffizienz-Hospitalisierungen führt.9, 10 FINEARTS-HF untersucht aktuell den Einsatz von Finerenon bei Patient:innen mit Herzinsuffizienz (LVEF ≥40 %) ungeachtet des Vorliegens einer diabetischen Nephropathie. Die in den kommenden Monaten zu erwartenden Studienergebnisse bergen insbesondere für HFpEF-Patient:innen das Potenzial für eine weitere gezielte Therapiesäule (primärer Studienendpunkt: kardiovaskulärer Tod und Herzinsuffizienz-Event; NCT04435626).