Der Begriff „Kardiomyopathie“ beschreibt allgemein eine Erkrankung des Herzmuskels, die durch strukturelle oder funktionelle Abnormitäten auffällt. Bei allen Formen kommt es zu einer Veränderung der Struktur des Herzmuskelgewebes. Aufgrund der vielfältigen Präsentation – sowohl aufgrund der unterschiedlichen Ätiologie als auch der Ausprägung, die sich im Laufe der Erkrankung auch ändern kann – ist eine klinisch sinnvolle Einteilung eine Herausforderung. Regelmäßig wurden von nationalen und internationalen Fachgesellschaften neue Definitionen und Klassifikationsschemata bereitgestellt. Aus historischen Gründen werden die ischämische, valvuläre, kongenitale sowie hypertensive Kardiomyopathie, bei denen die Ursache bekannt zu sein scheint, unter dem engeren Begriff der Kardiomyopathien nicht abgehandelt. Im Jahr 2023 wurde nun von der Europäischen Gesellschaft für Kardiologie (ESC) die erste internationale alle Formen umfassende Leitlinie zum Management der Kardiomyopathien veröffentlicht. Kardiomyopathien können klinisch unauffällig sein und nur zufällig entdeckt werden oder sich primär durch eine Arrhythmie oder Herzinsuffizienz manifestieren. Die Gründe für die Erstvorstellung bewegen sich dementsprechend auf einem weiten Spektrum. Die Patient:innen können aufgrund eines Zufallsbefundes in der Bildgebung elektrokardiografische Auffälligkeiten, kardiale Symptome, manifeste Herzinsuffizienz, Herzrhythmusstörungen bis zum plötzlichen Herztod, aber auch wegen auffälliger Ergebnisse beim Familienscreening bei Angehörigen oder aufgrund einer Abklärung bei einer Multiorganerkrankung zugewiesen werden. Im Verlauf schreitet die Erkrankung immer weiter voran, mit teils schwerwiegenden Verlaufsformen. Bei unter 55-jährigen Menschen sind Kardiomyopathien die Hauptursache für eine Herztransplantation.
Die Diagnose Kardiomyopathie sollte unbedingt die Suche nach ihrer Ursache zur Folge haben. Das Wissen über die Ursache hat Auswirkungen auf die Patientenaufklärung, die Prognoseabschätzung, die Bewertung hinsichtlich des Risikos für plötzlichen Herztod (SCD), das generelle Management und in einigen speziellen Fällen auch auf die Therapie. Bei familiären Formen spielt auch die Indikationsstellung zum genetischen Testen sowie die Früherkennung oder Therapie der betroffenen Familienmitglieder eine wichtige Rolle.
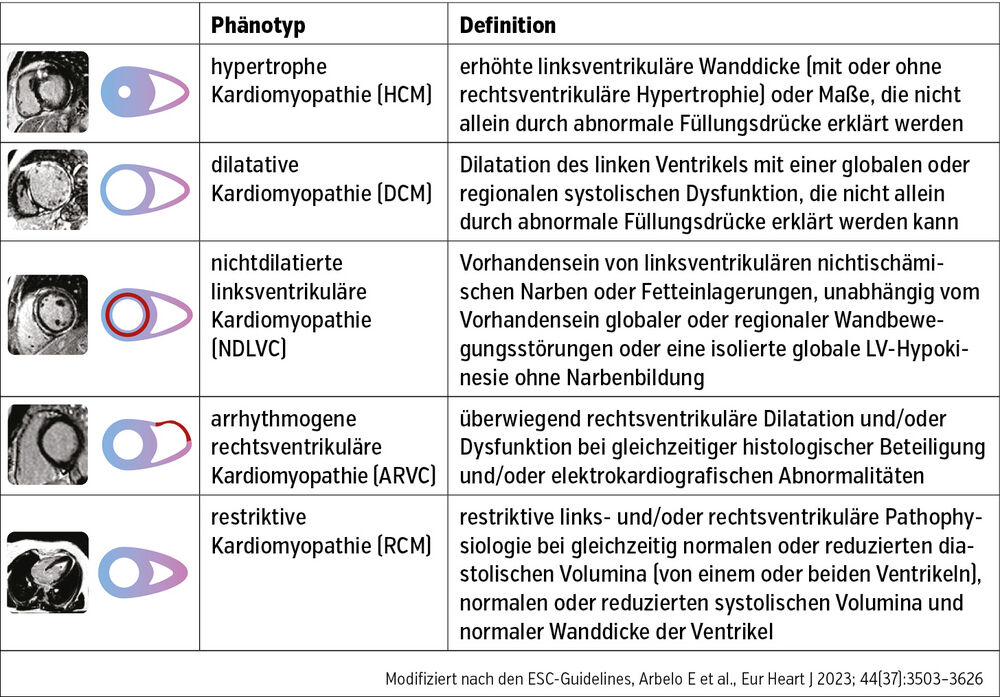
Am Beginn des diagnostischen Pfades steht die Beurteilung des Phänotyps (Tab.).
Der Phänotyp und eventuelle klinische Red Flags helfen bei der Priorisierung der Diagnostik, da einige der Ursachen mehr oder weniger wahrscheinlich sind. Man kann auch zwischen primären (z. B. genetische Formen, Myokarditis) und sekundären Kardiomyopathien (z. B. als Teil einer Systemerkrankung) unterscheiden. Einige Formen wie die hypertrophe Kardiomyopathie zeigen eine starke Assoziation ihrer Ausprägung und ihres Verlaufs mit einzelnen genetischen Mutationen. Jedoch dürfte ein bestimmter genetischer Hintergrund den meisten Formen im Sinne einer erhöhten Suszeptibilität oder Second-Hit-Theorie zugrunde liegen.
Therapiemöglichkeiten
Generell gelten für die Kardiomyopathien bei entsprechender Klinik die Behandlungsrichtlinien der Herzinsuffizienz und der Arrhythmien. Steht eine Herzinsuffizienz mit eingeschränkter Pumpfunktion im Vordergrund, sollten alle hier evidenzbasierten Therapien verschrieben werden (4-Säulen-Konzept). Ein wichtiger Punkt bei Kardiomyopathien stellt die Bewertung des SCD-Risikos dar. Bei erhöhtem Risiko wie etwa bei Vorliegen von Hochrisiko-Mutationen kann eine primär prophylaktische ICD-(Implantierbarer-Kardioverter-Defibrillator-)Implantation außerhalb des klassischen Indikationsbereiches, also auch bei einer LVEF >35 %, erfolgen. Bei sekundären Kardiomyopathien, also Mitbeteiligung des Herzens im Rahmen von anderen Erkrankungen, steht neben der kardialen Therapie die Behandlung der Grunderkrankung im Fokus. Intensive körperliche Belastungen sollten in einigen selektierten Patientengruppen vermieden werden, aber in den meisten Fällen ist eine moderate körperliche Betätigung in Absprache mit den behandelnden Ärzt:innen möglich und wird sogar empfohlen.
Zur Zeit wird intensiv an Therapien für spezifische Kardiomyopathien geforscht und seltene Formen in internationalen Registern gesammelt, um das Wissen zu erweitern. Große Fortschritte konnten bereits in der pharmakologischen Therapie bei der kardialen ATTR-Amyloidose, einer infiltrativen Kardiomyopathie (TTR-Stabilisatoren wie Tafamidis, Synthesereduktion durch RNA-Silencing wie Patisiran und Vutrisiran oder Antisense-Oligonukleotid wie Inotersen und zukünftig eventuell „Depleter“-Antikörper) sowie der hypertrophen obstruktiven Kardiomyopathie (kardiale Myosin-Inhibitoren wie Mavacamten und Aficamten) erzielt werden.