Stimulus-MDS1-Studie
Erste Analyse der Stimulus-MDS1-Studie mit Sabatolimab
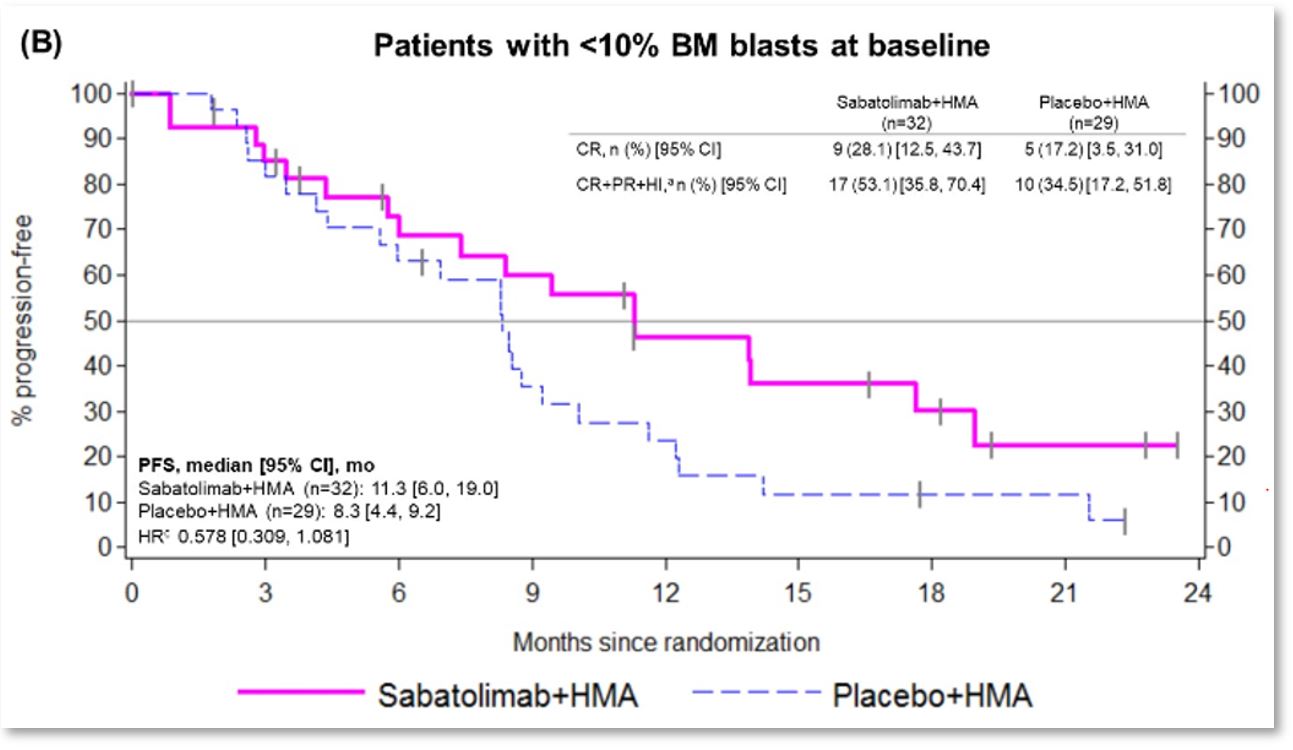
Sabatolimab (MBG453) als neuer Checkpoint-Inhibitor (Target TIM-3) wird in Kombination mit hypomethylierenden Substanzen untersucht. Am ASH wurden die ersten Daten der randomisierten placebokontrollierten Phase-2-Studie bei 127 Patienten mit intermediärem oder hohem Risiko präsentiert. Sabatolimab oder Placebo wurde an den Tagen 8 und 22 von 28-Tage-Zyklen verabreicht, Azacytidin (89 %) oder Decitabin (11 %) nach Standardprotokoll. In den primären Endpunkten PFS (11,1 vs. 8,5 Monate) und CR-Rate (21,5 % vs. 17,7 %) fand sich kein signifikanter Unterschied. In der Subgruppe der Patienten unter 10% Blasten oder intermediärem IPSS-R war ein Vorteil im PFS und der CR-Rate zu verzeichnen. Zusätzlich zeigt sich in der Kaplan-Meyer-Kurve ein Hinweis auf einen verzögerten Effekt (was für Checkpointinhibitoren nicht untypisch wäre). Die Hämatotoxizität war nicht unterschiedlich, eine schwere Pneumonitis wurde verzeichnet.
Bedeutung für die Praxis: Auch wenn die primären Endpunkte der Studie nicht erreicht wurden, bleibt die gut verträgliche Substanz von Interesse. Vorgestellte Daten suggerieren einen Vorteil bei geringerem Risiko und längerer Beobachtungsdauer. Die Folgestudie STIMULUS-MDS2 mit dem primären Endpunkt Gesamtüberleben hat bereits fertig rekrutiert und wird weitere Informationen bieten.