ASC4FIRST-Studie: Asciminib vs. Standard-TKIs
Asciminib ist der erste BCR::ABL1-Inhibitor, der speziell auf die ABL-Myristoyl-Tasche (STAMP) abzielt. ASC4FIRST ist eine randomisierte Phase-III-Studie zu Asciminib im Vergleich zu allen aktuellen Standard-TKIs in der Erstlinientherapie von Patienten mit neu diagnostizierter CML-Erkrankung.
Primärer Endpunkt:
MMR-Rate in Woche 48 mit ASC vs. vom Prüfarzt ausgewählter TKI (IS)
Design:
1:1 randomisiert und erhielten einmal täglich 80 mg ASC oder einen IS-TKI in Standarddosierung des jeweiligen TKI (IM oder 2 Gen TKI)
Stratifiziert nach ELTS-Risikokategorie und PRS-TKI (IM oder 2G-TKIs)
Die Patienten erhielten ASC (n = 201: ASCIMA, n = 101; ASC2G, n = 100) oder einen IS TKI (n = 204: IS TKI-IM, n = 102; IS TKI-2G, n = 102)
Medianes Follow Up: ca. 16 Monate
Ergebnisse:
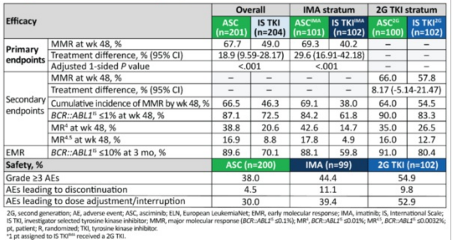
MMR-Rate in Woche 48:
ASC vs. IS TKI: 67,7 % vs. 49,0 %
ASCIMA vs. IS-IM: 69,3 % vs. 40,2 %, p < 0,001
ASC vs. IS TKI2G: 66,0 % vs. 57,8 %
Nebenwirkungen:
Asciminib war im Vergleich zu IM und 2G-TKs besser verträglich und hatte geringere Abbruchraten und Dosisanpassungen aufgrund von Nebenwirkungen
Zusammenfassung:
Die ASC4FIRST Studie, ist der einzige direkte Vergleich gegen alle aktuellen Standard-TKIs in der Erstlinie der CP-CML. Asciminib zeigte eine signifikante und überlegene Wirksamkeit und ausgezeichnete Sicherheit und Verträglichkeit im Vergleich zu IMA- und 2G-TKIs bei Patienten mit neu diagnostizierter CML. ASC kann das TFR-Potenzial steigern.