Neues beim metastasierten Urothelkarzinom
Neue Standards in der Erstlinientherapie des metastasierten Urothelkarzinoms
Gleich zwei neue Kombinationen haben seit 2023 die Therapielandschaft beim fortgeschrittenen Urothelkarzinom neu definiert.
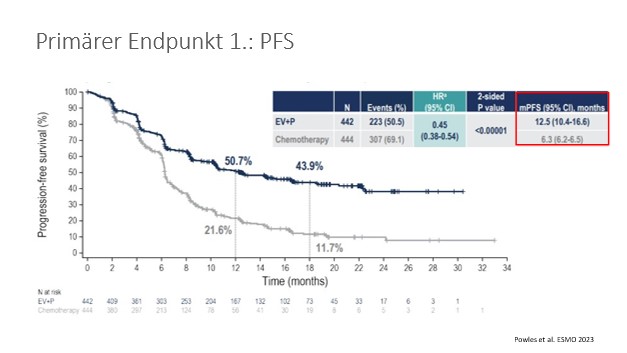
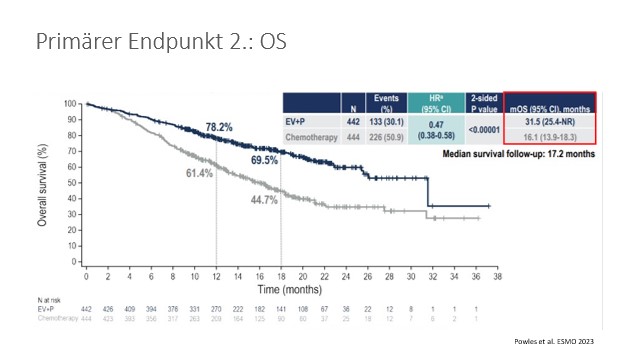
Mit der Präsentation der EV-302-Studie, in der das gegen Nectin-4 gerichtete Antibody-Drug-Konjugat (ADC) Enfortumab vedotin (EV) in Kombination mit Pembrolizumab (P) untersucht wurde, wurde mit einem Schlag eine jahrzehntelange Platin-Ära beendet. In der Studie erhielten die Patienten EV (Tage 1, 8) + P (Tag 1) alle 3 Wochen versus Platin + Gemcitabine, nach einem Amendment gefolgt von einer Erhaltungstherapie mit Avelumab. Die dualen primären Endpunkte (PFS und OS) wurden statistisch hochsignifikant erreicht, das progressionsfreie Überleben und das Gesamtüberleben beinahe verdoppelt. (Abb. 1) In den vordefinierten Subgruppenanalysen überzeugte die Kombination unabhängig von der Platin-Tauglichkeit, dem PD-L1-Status oder dem Metastasierungsmuster (viszerale Metastasen vs. Lymphknoten allein). Die Gesamtansprechrate mit 67,7 vs. 44,4 % und eine komplette Remissionsrate von 29,1 % überzeugen ebenfalls. Das Nebenwirkungsprofil, mit 55,9 % ≥ Grad 3 Toxizität darf jedoch nicht unterschätzt werden. Besonders die Hauttoxizität sowie eine periphere Neuropathie im späteren Therapieverlauf können herausfordernd werden und müssen vom betreuenden Ärzteteam regelmäßig evaluiert werden. Eine Zulassung dieser Kombination wird für Herbst 2024 erwartet.
Zeitgleich wurde die Checkmate-901 Studie präsentiert, in welcher erstmalig ein Vorteil für die Upfront-Kombination eines Checkpointinhibitors mit einer Cisplatin-haltigen Chemotherapie gezeigt werden konnte. Cisplatin + Gemcitabine + Nivolumab gefolgt von einer Nivolumab-Erhaltungstherapie zeigte sowohl beim Gesamtüberleben als auch beim progressionsfreien Überleben eine statistische Signifikanz, wobei der Benefit im OS mit etwa 3 Monaten und eine Erhöhung der ≥ Grad 3-Toxizität von 10 % kritisch diskutiert werden sollte. Die Gesamtansprechrate mit 57,6 % vs. 43,1 % und eine komplette Remissionsrate von beinahe 22 % überzeugen wiederum nachhaltig.
Nach der kompletten Neugestaltung der Erstlinientherapie beim la/mUrothelkarzinom bleiben einige spannende Frage offen, u.a. wer für EV + P unfit ist, jedoch für eine Cisplatin-haltige Therapie in Kombination mit Nivolumab in Frage käme, was folgt nach EV+P in höheren Therapielinien u.v.m.
Höhere Therapielinien und neue Targets beim Urothelkarzinom
FGFR3/2alt, HER2 und TROP-2 sind nach Nectin-4 und PD-L1 die neuen Targets, die in höheren Therapielinien als Therapieziel dienen.
Als wichtigster neuer molekularer Marker präsentiert sich eine FGFR2/3-Alteration, welche bei bis zu 20 % der Patient:innen mit la/m UC detektiert werden kann. In der Phase-III THOR-Studie erhielten die Patient:innen mit einer FGFR2/3-Fusion oder -Mutation nach 1-2 Systemtherapien inkl. einem PD-(L)1-Inhibitor, 8 mg Erdafitinib, einen pan-FGFR-Inhibitor, 1x tgl. p.o. vs. Docetaxel oder Vinflunine. Der primäre Endpunkt, das Gesamtüberleben, wurde mit 12,1 vs. 7,8 Monaten (HR 0,64) signifikant erreicht, die Ansprechrate von 11,5 auf 45,6 % erhöht. Somit stellt Erdafitinib den neuen Standard bei entsprechender vorliegender Alteration in dieser Population dar. Die Kohorte 2 dieser Studie, in der Patient:innen bereits nach einer Systemtherapie ohne PD-(L)1-Inhibitor inkludiert wurden, konnte den Benefit im OS, trotz höheren Ansprechraten für Erdafitinib, nicht bestätigen. Dadurch wird Erdafitinib erst nach 2 Vortherapien inkl. eines PD-(L)1-Hemmers von den Guidelines empfohlen. Darüber hinaus ist das Toxizitätsprofil dieser Substanz, bestehend aus Hand-Fuß-Syndrom, Stomatitis, Nagelveränderungen, Sehstörungen und Hyperphosphatämien, durchaus fordernd und bedarf eines entsprechenden Therapiemanagements. Eine Zulassung in Europa wird ebenfalls für Herbst 2024 erwartet.
Falls Patient:innen keine FGFR2/3-Alteration aufweisen, kann in höheren Therapielinien Sacituzumab Govitecan (SG), ein ADC gegen TROP-2, eingesetzt werden. Mit Ansprechraten von beinahe 30 %, einem PFS von 5,4 Monaten und einem OS von 10,9 Monaten, ist es eine potente Option für schwer vortherapierte Patient:innen.
In naher Zukunft werden gegen HER2 gerichtete ADCs wie Disitamab vedotin oder Trastuzumab deruxtecan für Patient:innen mit einer HER2/neu-Überexpression die Therapielandschaft erweitern.
Ob in weiterer Zukunft Triplet-Kombinationen mehrerer ADCs, sogenannter DADs (doppelte ADCs), mit IOs der aktuellen Duplette (EV+P) überlegen sind, ist abzuwarten. Definitiv werden diese hochpotenten Substanzen bereits in früheren Therapielinien (neoadjuvant, adjuvant) untersucht und werden womöglich beim muskelinvasiven Stadium (MIBC) den Einzug schaffen.