Chronische Inflammation: Angriffspunkte der therapeutischen Intervention

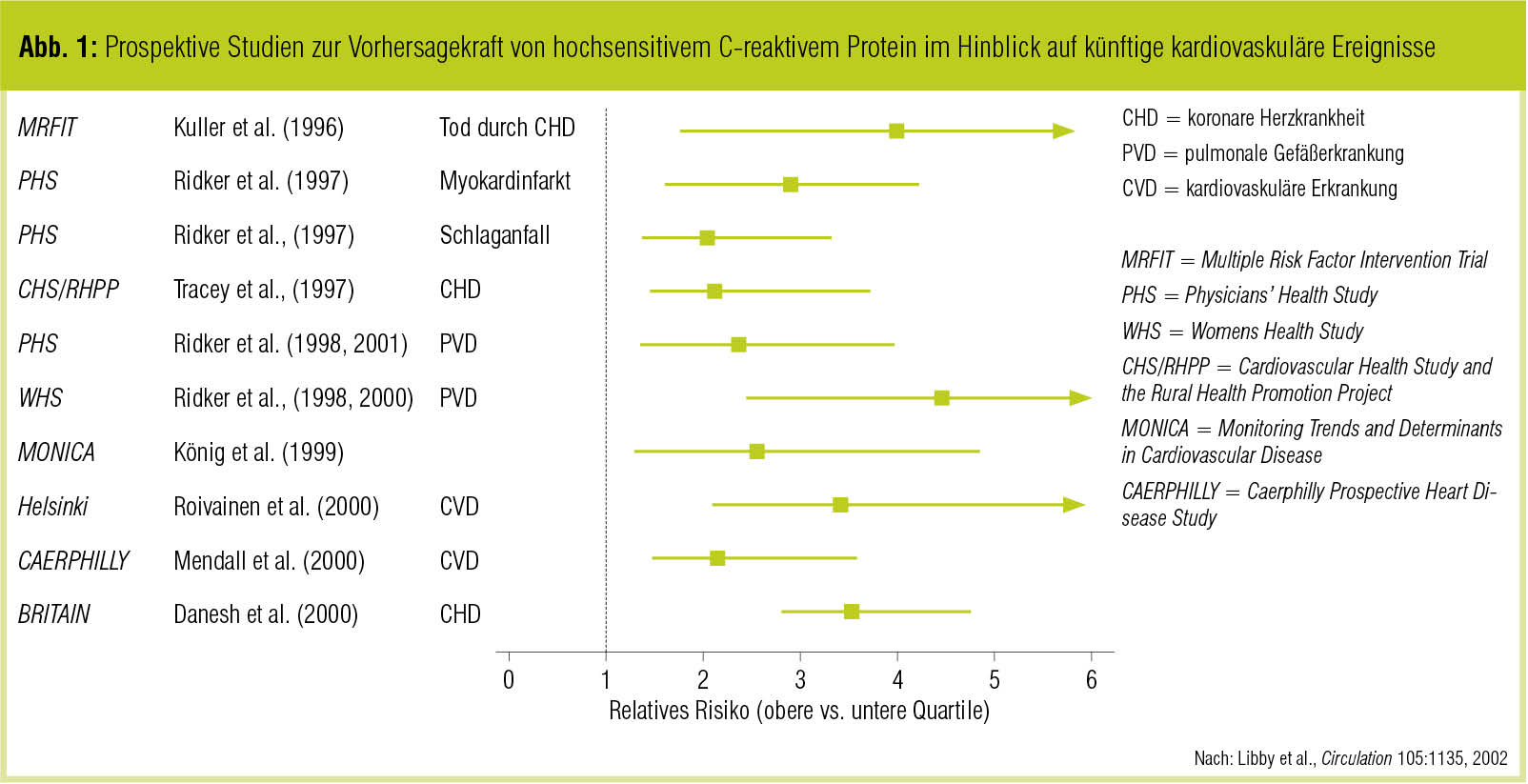
Im komplexen Zusammenspiel der Faktoren, über die Adipositas, Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen in Verbindung stehen, spielt Inflammation eine zentrale Rolle. Im Tiermodell und ebenso beim Menschen gehen atherosklerotische Ablagerungen in der Arterienwand Hand in Hand mit inflammatorischen Prozessen (Libby et al., Circulation 2002). In epidemiologischen Untersuchungen waren erhöhte Leukozytenzahlen und inflammatorische Biomarker wie C-reaktives Protein (CRP) und Interleukin 6 (IL-6) mit der Inzidenz von metabolischem Syndrom, Typ-2-Diabetes und kardiovaskulären Komplikationen assoziiert (Ridker et al., N Engl J Med 1997; Pradhan et al., JAMA 2001; Shoelson et al., J Clin Invest 2006). In Übereinstimmung damit belegt eine ganze Reihe populationsbasierter Untersuchungen den prädiktiven Wert von CRP im Hinblick auf die Abschätzung des kardiovaskulären Risikos (Abb. 1).
Adipositas und Inflammation
Bei Stoffwechselgesunden korreliert der CRP-Spiegel mit dem Ausmaß der Übergewichtigkeit. In der Insulin Resistance Atherosclerosis Study (IRAS); Festa et al., Circulation 2000) und in der deutschen VERA-Studie (Fröhlich et al., Diabetes Care 2000) lagen die durchschnittlichen CRP-Werte desto höher, je mehr Faktoren des metabolischen Syndroms vorlagen.
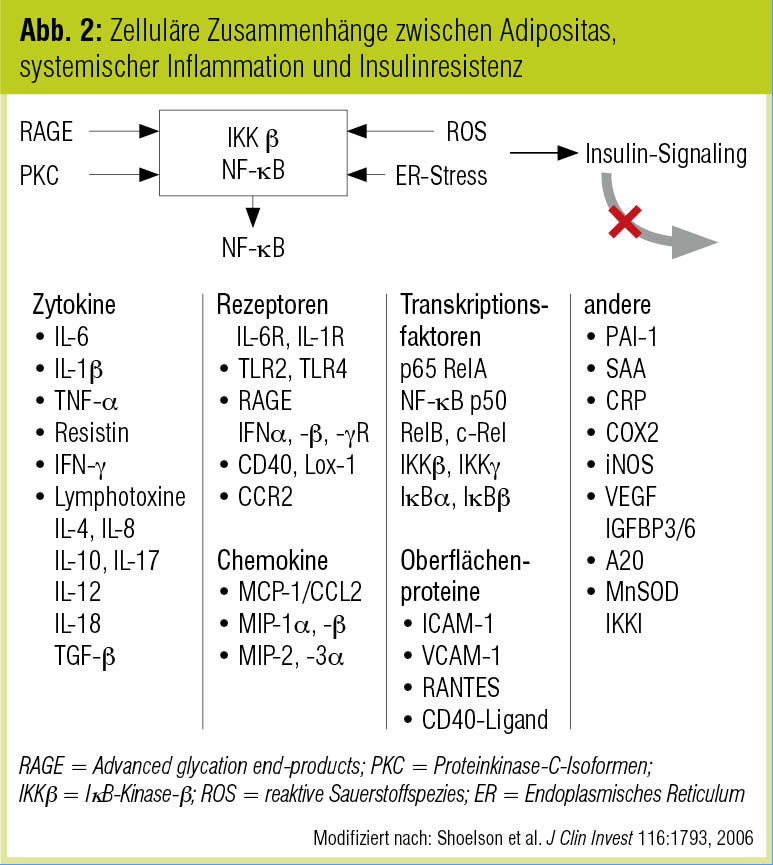
Adipositas ist die wichtigste pathogenetische Grundlage von Insulinresistenz und Typ-2-Diabetes. Das viszerale Fettgewebe ist aber auch jenes Organ, in dem die mit der Insulinresistenz einhergehende systemische Inflammation ihren Ausgang nimmt, indem inflammatorische Peptide wie Tumornekrosefaktor α (TNF-α), Chemoattractant Protein 1 (MCP-1) und IL-6 freigesetzt und damit die Atherogenese unabhängig von den Effekten von Insulinresistenz und Dyslipidämie verstärkt wird. Im Zentrum dieses Prozesses steht der IKKβ/NF-κB-Signalweg (Barnes & Karin, N Engl J Med 1997), der im Zusammenhang mit der metabolischen Dysregulation durch diverse Stimuli (darunter oxidativer Stress, Advanced glycation end-products, Aktivierung von Proteinkinase-C etc.) aktiviert wird und eine Vielzahl von proinflammatorischen und proatherogenen Genprodukten moduliert (Abb. 2). Aus der viszeralen Adipokinfreisetzung resultiert in weiterer Folge unter anderem die vermehrte Sekretion von CRP in der Leber (Shoelson et al., J Clin Invest 2006).
Therapeutische Konsequenzen
Nachdem nachgewiesen wurde, dass im viszeralen Fettgewebe produzierter TNF-α die Insulinresistenz fördert (Hotamisligil et al., Science 1993), versuchte man, die in der Rheumatologie so erfolgreiche TNF-α-Blockade auch im Kontext des metabolischen Syndroms zu nutzen. Die im Tiermodell erzielten Erfolge ließen sich beim Menschen – im Sinn einer klinisch relevanten Verbesserung der adipositasassoziierten Dysglykämie und Inflammation – bisher jedoch nicht bestätigen (Bernstein et al., Arch Intern Med 2006; Stanley et al., J Clin Endocrinol Metab 2010).
Gewichtsreduktion. Etablierte Maßnahmen zur Reduktion des Körpergewichts können nicht nur die Diabetesmanifestation verhindern, sondern auch die chronische Inflammation verbessern. In einer kleineren Querschnittstudie bei adipösen postmenopausalen Frauen identifizierten Tchernof et al. (Circulation 2002) die viszerale Fettmenge als verlässlichen Prädiktor für den CRP-Spiegel im Plasma; diätetisch induzierte Gewichtsabnahme hatte eine Abnahme der CRP-Werte zur Folge. Monzillo et al. (Obes Res 2003) fanden bei adipösen Personen (n = 24) mit Insulinresistenz und gestörter Glukosetoleranz, die sich einer Lebensstilintervention mit forcierter körperlicher Aktivität und Kalorienrestriktion unterzogen, nach 6 Monaten eine signifikante Reduktion der Leptin- und IL-6-Spiegel und eine tendenzielle Verbesserung von TNF α und CRP. Im Lifestyle-Interventionsarm des Diabetes Prevention Program sank das CRP innerhalb eines Jahres im Median um 29 % bzw. 33 % (Frauen/Männer), im Vergleich zu 14 % bzw. 7 % unter Metformin und 0 % bzw. +5 % in der Placebogruppe (Haffner et al., Diabetes 2005). Ähnliche Ergebnisse sind für Personen mit Adipositas und gestörter Glukosetoleranz oder Typ-2-Diabetes nach Magenbandoperation beschrieben (Viardot et al., J Clin Endocrinol Metab 2010).
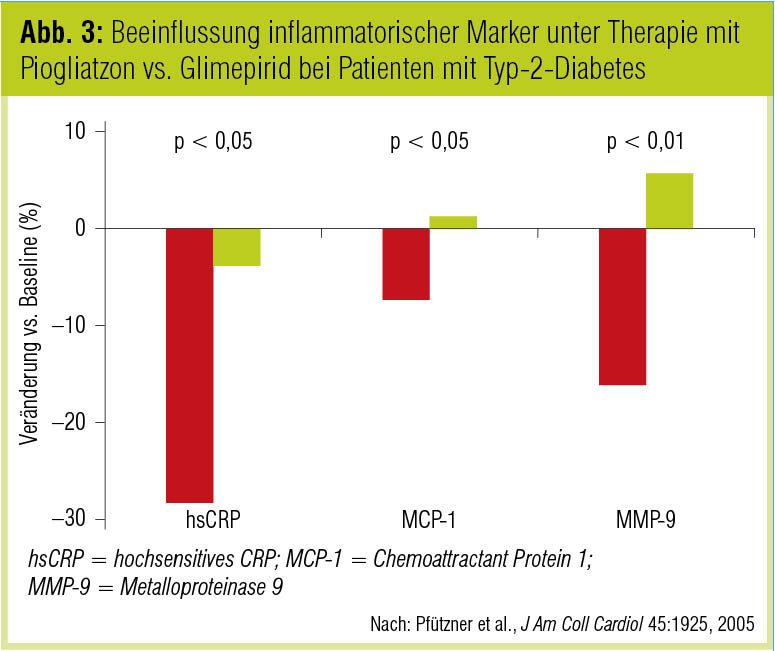
Antidiabetische Therapie. Unter den in der antidiabetischen Therapie eingesetzten Wirksubstanzen sind antiinflammatorische Effekte am überzeugendsten für die Glitazone beschrieben. Glitazone aktivieren den nukleären Transkriptionsfaktor Peroxisome proliferator-activated receptor γ (PPAR-γ) und modulieren damit die Expression verschiedener Zielgene des Glukosestoffwechsels, der Adipogenese und des inflammatorischen Geschehens. Das klinische Potenzial des Wirkprinzips zeigt sich exemplarisch in der PIONEER-Studie, in der Pioglitazon bei Patienten mit Typ-2-Diabetes innerhalb von 6 Monaten eine signifikante Absenkung von hochsensitivem CRP (hsCRP), MCP-1 und Metalloproteinase 9 (MMP-9) erreichte. Die Therapie mit Glimepirid in der Kontrollgruppe war diesbezüglich neutral, was darauf hinweist, dass der Effekt unabhängig von der glykämischen Kontrolle auftritt (Pfützner et al., J Am Coll Cardiol 2005; Abb. 3).
Insulin selber kann, wie in einigen kleineren Studien demonstriert wurde, ebenfalls antiinflammatorisch wirken. Dandona et al. (J Clin Endocrinol Metab 2001) beschreiben bei adipösen Probanden nach Infusion von Insulin einen kurzfristigen Abfall von NF-κB in mononukleären Zellen auf ein Fünftel des Ausgangswertes. In Übereinstimmung damit konnte durch eine Insulininfusion der Anstieg von hsCRP und Serumamyloid A (SAA) in der Akutphase nach Myokardinfarkt (48 h) signifikant abgemildert werden (Chaudhuri et al., Circulation 2004). Längerfristig dürften Antidiabetika (mit Ausnahme von Glitazonen und Metformin, jedoch inklusive Basalinsulin) abnorme Entzündungszeichen nicht günstig beeinflussen (Fonseca et al., J Diabetes Complications 2006).
Antiinflammatorische Effekte der Lipidsenkung. Statine als zentrale pharmakologische Option der Lipidsenkung führen nach einer Metaanalyse klinischer Studien zu einer Absenkung des CRP um 25–30 %; andere inflammatorische Marker oder die Fibrinogenkonzentration werden offenbar nicht beeinflusst. Es handelt sich dabei um einen Klasseneffekt, der dosisunabhängig auftritt und mit der erreichten Lipidsenkung nicht direkt korreliert (Balk et al., Ann Intern Med 2003).
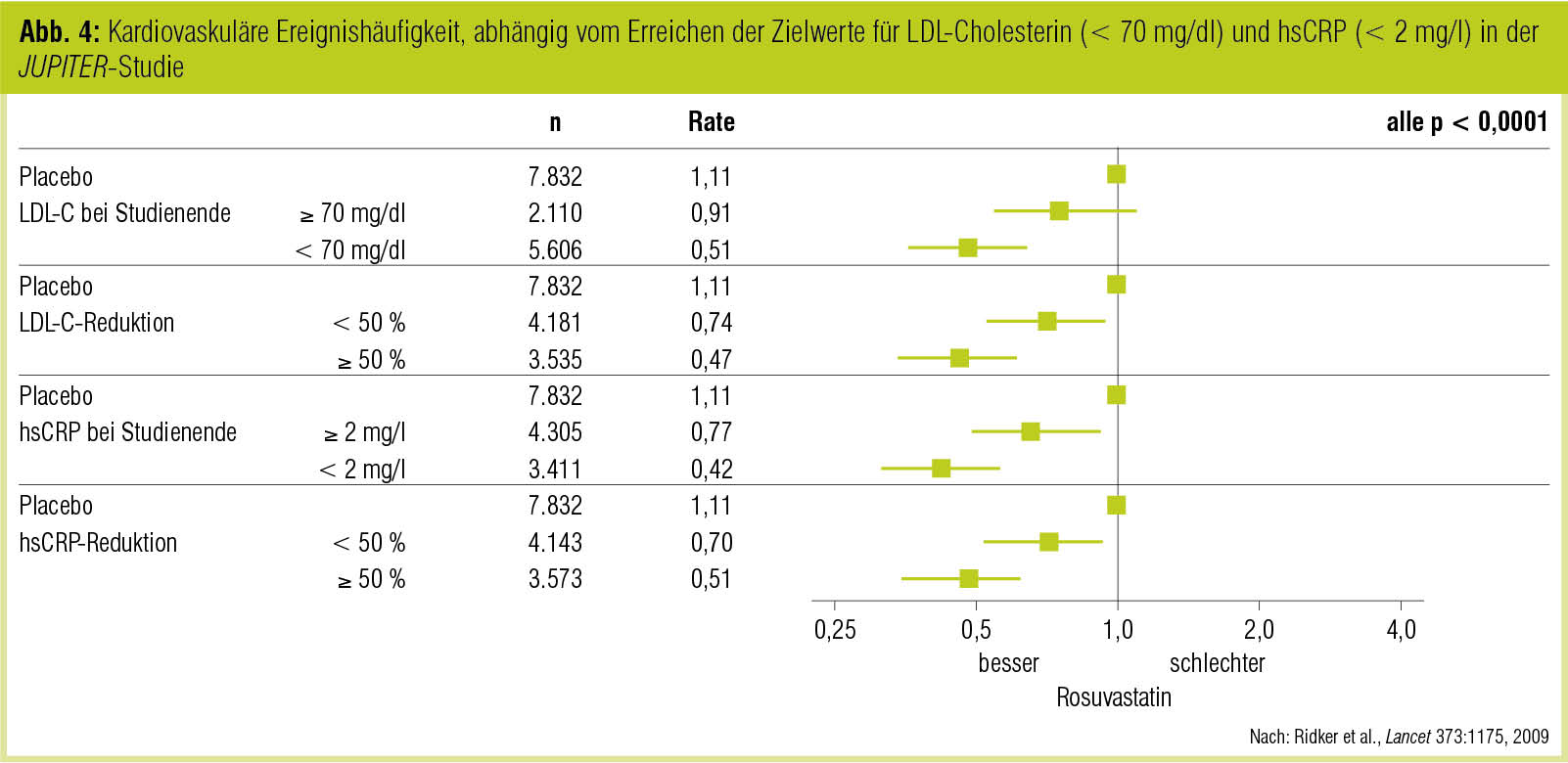
In der PROVE IT-TIMI 22-Studie und ebenso in der A to Z-Studie hatten Patienten mit akutem Koronarsyndrom dann die besten Outcomes, wenn sie unter Statintherapie nicht nur ein LDL-Cholesterin (LDL-C) von < 70 mg/dl, sondern auch ein hsCRP von < 2 mg/l erreichten (Ridker et al., N Engl J Med 2005; Morrow et al., Circulation 2006). Für Patienten mit erhöhten hsCRP-Werten bei ansonsten günstiger vaskulärer Risikokonstellation und LDL-C-Spiegeln < 130 mg/dl ergab die JUPITER-Studie unter Therapie mit Rosuvastatin vs. Placebo eine signifikante Reduktion schwerwiegender kardiovaskulärer Endpunkte (Hazard Ratio = 0,56; 95%-KI: 0,46–0,69) im Verlauf von median 1,9 Jahren; Die LDL-c-Werte waren nach dieser Zeit gegenüber der Baseline um durchschnittlich 50 %, die hsCRP-Werte um 37 % reduziert (Ridker et al., N Engl J Med 2008). Subgruppenauswertungen der JUPITER-Daten, welche die Studien-Outcomes nach LDL-C- und hsCRP-Verlauf getrennt ausweisen (Abb. 4), bestätigen, dass die unter Statintherapie erzielte CRP-Reduktion unabhängig von der Lipidsenkung für die kardiovaskuläre Prognose von Bedeutung ist (Ridker et al., Lancet 2009).
Antiinflammatorische Therapie des Diabetes mellitus
In der Literatur finden sich zahlreiche Hinweise darauf, dass die Adressierung entzündlicher Prozesse über die Gefäßprotektion hinaus für die Diabetestherapie relevant sein könnte. Wasko et al. (JAMA 2007) fanden bei Patienten mit rheumatoider Arthritis, die mit Hydroxychloroquin behandelt wurden, retrospektiv weniger Diabetesmanifestationen im Vergleich zu Patienten, die das Basistherapeutikum nicht erhielten. Vielversprechende Daten gibt es darüber hinaus zum Einsatz von IL-1-Rezeptorantagonisten und Anti-IL-1β-Antikörpern (Dinarello et al., Curr Opin Endocrinol Diabetes Obes 2010).
Azetylsalizylsäure (ASS) ist ein weiterer antiinflammatorischer Therapieansatz, der bei Diabetespatienten aber primär im Hinblick auf die erhöhte Gerinnungsneigung eingesetzt wird (Wascher, Wien Klin Wochenschr 2012). Tierexperimentelle Studien und kleinere klinische Untersuchungen bei Patienten mit Typ-2-Diabetes haben gezeigt, dass hochdosiertes ASS über die Hemmung von IKKβ (und nicht über den Zyklooxigenase-Signalweg) Insulinsensitivität und Glukosetoleranz verbessern kann (Yuan et al., Science 2001; Hundal et al., J Clin Invest 2002). Entsprechende Fallberichte über den erfolgreichen Einsatz von Natriumsalizylat bei Patienten mit diabetischer Glukosurie wurden sogar schon im 19. Jahrhundert (Ebstein, Berl Klin Wochenschr 1876) publiziert. Im Gegensatz zu ASS haben Natriumsalizylat und andere nichtazetylierte Salizylate (darunter Salsalat) keinen inhibierenden Effekt auf die Zyklooxigenasen COX1 und COX2 und die Prostaglandinsynthese (Kopp et al., Science 1994).
Vor allem das in den USA seit Jahrzehnten als Schmerzmittel verwendete, generisch verfügbare und im Vergleich zu ASS besser verträgliche bzw. blutungssicherere Salsalat (Disalcid) hat in den vergangenen Jahren zunehmend das diabetologische Interesse auf sich gezogen. In Pilotstudien wiesen Goldfine et al. (Clin Transl Sci 2008) nach, dass Salsalat in Standarddosierung in der Lage ist, den Insulinrespons und ebenso die Glukose- und Lipidhämostase (Nüchternblutzucker, postprandialer Blutzucker, freie Fettsäuren, Adiponektin) bei Patienten mit Typ-2-Diabetes zu verbessern. In einer weiteren „Proof of pinciple“-Studie bei adipösen prädiabetischen Personen verbesserte Salsalat innerhalb eines Monats die Insulinsensitivität und reduzierte die Blutzuckerwerte im Nüchternzustand und im oralen Glukosetoleranztest; inflammatorische Marker des kardiovaskulären Risikos waren unter Salsalat gegenüber Placebo abgesenkt (Fleischman et al., Diabetes Care 2008).
Salsalat in der TINSAL-T2D-Studie
Basierend auf diesen Erfahrungen wurde, finanziert von den US National Institutes of Health und dem National Institute of Diabetes and Digestive and Kidney Diseases, der Targeting Inflammation Using Salsalate in Type 2 Diabetes (TINSAL-T2D) Trial (NCT00392678) als multizentrische kombinierte Phase-II/III-Studie gestartet. Im ersten Studienteil wurden Patienten mit inadäquat kontrolliertem Typ-2-Diabetes (HbA1c: 7–9,5 %; Nüchternblutzucker ≤ 225 mg/dl) unter dietätischer oder stabiler oraler antidiabetischer Therapie 14 Wochen lang zusätzlich mit Salsalat (3 g/d; 3,5 g/d; 4 g/d) oder Placebo behandelt (jeweils n = 27). Im untersuchten Zeitraum sanken die HbA1c-Werte mit Salsalat placebobereinigt um 0,36–0,49 Prozentpunkte vs. Placebo. Nüchternblutzucker, Triglyzeride und Adiponectin waren ebenfalls signifikant verbessert, allerdings war die Albuminkonzentration im Harn in den Verumgruppen höher als in der Placebogruppe (Goldfine et al., Ann Intern Med 2010).
Die zweite Studienphase, deren Ergebnisse zur Jahrestagung der American Diabetes Association 2012 erstpräsentiert wurden, inkludierte 282 Patienten mit Typ-2-Diabetes (Body Mass Index: 33 kg/m2; HbA1c 7,7 %, Nüchternglukose: 151 mg/dl; Gesamtcholesterin: 165 mg/dl; Triglyzeride 157 mg/dl), die über einen Zeitraum von 48 Wochen mit Salsalat (3,5 g/d) oder Placebo behandelt wurden; Die Patienten waren mit bis zu 3 Antidiabetika (88 % Metformin, 52 %, Sulfonylharnstoffe, 15 % DPP-4-Hemmer, 0,3 % Alphaglukosidaseinhibitoren) vorbehandelt. Im Beobachtungszeitraum sanken Nüchternblutzucker und HbA1c jeweils moderat um durchschnittlich 11 mg/dl bzw. 0,24 Prozentpunkte vs. Placebo. Die Teilnehmer nahmen durchschnittlich um 1 kg zu, das LDL-C stieg um 8 mg/dl an, das HDL-Cholesterin blieb konstant. Wie schon in der ersten Studienphase war die Therapie mit Salsalat mit einer Erhöhung der Albuminurie verbunden, die sich nach Studienende als reversibel zeigte. Weitere potenziell sicherheitsrelevante Signale (Blutdruck, Leberfunktion, Elektrolyte, Blutungen) wurden nicht verzeichnet.
Ein Effekt der Salsalatbehandlung auf die Gefäßfunktion (bezogen auf die flussmediierte Vasodilatation) ließ sich im bisherigen Follow-up der TINSAL-T2D-Studie nicht zeigen. Im Rahmen der TINSAL-CVD-Studie (NCT00624923) wird der Effekt von Salsalat auf das Plaquevolumen bei Patienten mit koronarer Herzkrankheit untersucht; Ergebnisse sind in 1 bis 2 Jahren zu erwarten.