Diabetes und Herzinsuffizienz – Neue Therapieansätze
Es gibt bei Patienten mit Herzinsuffizienz eine hohe Prävalenz von Hyperglykämie bzw. Diabetes und es besteht eine starke Assoziation von Diabetes mit einer schlechteren funktionellen Kapazität, verstärkten Symptomen sowie von Hospitalisierungsraten und Mortalität bei Herzinsuffizienz (Romero et al., Int J Cardiol 2012).
Die Prävalenz der Herzinsuffizienz nimmt aus verschiedenen Gründen weiter zu: Es steigt das kardiovaskuläre Risiko durch fehlende körperliche Bewegung und Übergewicht und die sich daraus ergebenden Folgen Hypertonie, Diabetes mellitus und Hyperlipidämie. Da diese kardiovaskulären Risikofaktoren zu koronarer Herzkrankheit führen, steigt auch die Prävalenz der Herzinsuffizienz. Herzinsuffizienz ist eine Hauptkomplikation der koronaren Herzkrankheit; sie kann auch als Endstadium der koronaren Herzkrankheit gesehen werden. Nicht zuletzt wegen der verbesserten therapeutischen Möglichkeiten erreichen heute mehr Patienten als früher dieses Endstadium. Auch unabhängig von der Therapie der koronaren Herzerkrankung erreichen die Menschen heute ein höheres Lebensalter als früher. Da steigendes Alter ein wichtiger Risikofaktor für Herzinsuffizienz ist, steigt damit auch die Prävalenz der Herzinsuffizienz.
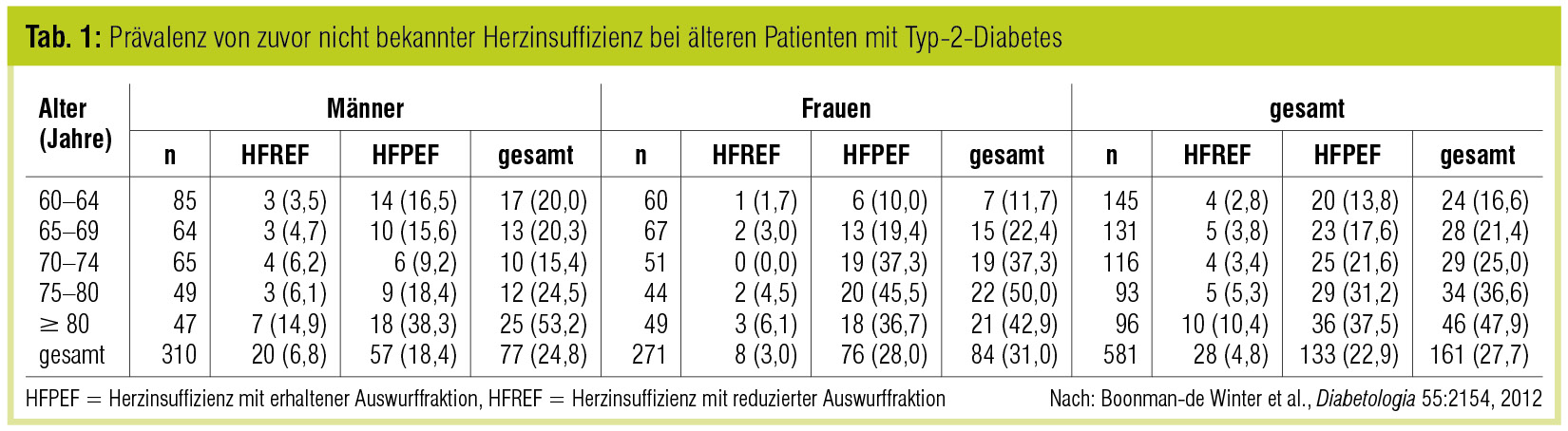
In den großen Herzinsuffizienzstudien liegt die Prävalenz von Typ-2-Diabetes bei 20–27 %: (CONSENSUS: 23 %; SOLVD: 26 %, V-HeFT II: 20 %; ATLAS: 20 %; RESOLVD: 27 %). Darüber hinaus gibt es eine hohe Dunkelziffer von nicht diagnostiziertem Diabetes und von Patienten mit Prädiabetes (gestörte Glukosetoleranz, gestörte Nüchternglukose). So hatten z. B. in der RESOLVD-Studie insgesamt 43 % der Teilnehmer einen gestörten Glukosestoffwechsel (27 % Diabetes, 16 % gestörte Nüchternglukose). In einer kürzlich publizierten Studie von Boonman-de Winter et al. (Diabetologia 2012) konnte gezeigt werden, dass umgekehrt auch eine hohe Prävalenz von bisher unbekannter Herzinsuffizienz bei über 60-jährigen Patienten mit Typ-2-Diabetes zu finden ist (Tab. 1).
Bindeglied ist die Insulinresistenz
Die atherosklerotische koronare Herzkrankheit ist die häufigste Ursache für Herzinsuffizienz (He et al., Arch Intern Med 2001) und das metabolische Syndrom ist ein Hauptprädiktor für koronare Ereignisse (Saely et al., Diabetes Care 2006). Das metabolische Syndrom und die damit eng verknüpfte Insulinresistenz konnten auch als Risikofaktoren für die Mortalität bei chronischer Herzinsuffizienz identifiziert werden (Doehner et al., J Am Coll Cardiol 2005). Außerdem ist ein hohes Proinsulin ein Prädiktor für neu auftretende linksventrikuläre systolische Dysfunktion (Arnlöv et al., Am Heart J 2001). Insulinresistenz scheint also eine wichtige Rolle als Bindeglied zwischen Diabetes und Herzinsuffizienz zu spielen.
Zwischen der Herzinsuffizienz und der Insulinresistenz gibt es in der Tat eine enge Beziehung mit gegenseitiger Verstärkung: Auf der einen Seite induziert die chronische Herzinsuffizienz eine Insulinresistenz. Es kommt zu einer neuroendokrinen Aktivierung, einer Inflammation, einer hormonellen Imbalance, einer verschlechterten Gewebeperfusion und einer endothelialen Dysfunktion sowie zu Veränderungen im Skelettmuskel, nicht zuletzt auch zu einer negativen Beeinflussung des Lebensstils: Patienten mit Herzinsuffizienz sind körperlich schlecht belastbar und deshalb körperlich wenig aktiv. Außerdem kommt es zu ungünstigen Beeinflussungen des Stoffwechsels durch Herzinsuffizienzmedikamente (v. a. durch Diuretika). Umgekehrt trägt aber die Insulinresistenz auch zur Herzinsuffizienz bei; wichtige Mechanismen dabei sind ein erhöhter Sympathikotonus, eine Aktivierung des Renin-Angiotensin-Systems, ein pro-inflammatorischer Status und die mit Insulinresistenz assoziierte Hyperglykämie, welche die diastolische Dysfunktion begünstigt. Eine beeinträchtigte energetische Effizienz begünstigt außerdem eine systolische linksventrikuläre Dysfunktion. Außerdem kommt es zu einer erhöhten Fibrose und Apoptose im Myokard, und eine Hyperinsulinämie begünstigt die linksventrikuläre Hypertrophie.
Auch die das metabolische Syndrom definierenden Stigmata sind Prädiktoren der Herzinsuffizienz. In der Framingham Heart Study konnte gezeigt werden, dass Adipositas als wichtige Komponente des metabolischen Syndroms das Risiko für das Auftreten einer Herzinsuffizienz erhöht (Kenchaiah et al., N Engl J Med 2002). Interessanterweise scheint es jedoch eine umgekehrte Beziehung zwischen der Mortalität und dem Körpergewicht diabetischer Patienten nach Hospitalisierung wegen Herzinsuffizienz zu geben: In diesem Setting ist geringeres Gewicht mit einer erhöhten Mortalität vergesellschaftet (Waring et al., Am J Med 2011). Der Grund dafür dürfte sein, dass bei den bereits Kranken die besonders Mageren schon eine kardiale Kachexie haben, die eine äußerst ungünstige Prognose anzeigt. Erhöhter Blutdruck ist ebenfalls ein Risikofaktor für das Auftreten einer Herzinsuffizienz (Haider et al., Ann Intern Med 2003).
Existiert diabetische Kardiomyopathie als eigene Entität?
Laut gängiger Definition impliziert eine Kardiomyopathie eine Herzmuskelerkrankung, bei welcher das Myokard strukturell und funktionell abnorm ist, ohne dass aber eine koronare Herzkrankheit, eine Hypertonie, eine Herzklappenerkrankung oder ein angeborener Herzfehler dafür verantwortlich gemacht werden könnte (Elliott et al., Eur Heart J 2008).
Eine hohe diastolische Steifigkeit wurde als entscheidendes frühes Stigma der diabetesinduzierten linksventrikulären Dysfunktion erkannt (Zarich et al., J Am Coll Cardiol 1988); bei erhaltener systolischer linksventrikulärer Funktion spricht man von „heart failure with normal ejection fraction“ (HFNEF). Myokardfibrose und die Ablagerung von „advanced glycation endproducts“ (AGE) sind aber auch die wichtigsten Faktoren der linksventrikulären systolischen Dysfunktion bei Diabetes (Van Heerebeek et al., Circulation 2008). Bei schwerer Hyperglykämie kann also Diabetes starke AGE-Ablagerung verursachen, außerdem zu Entzündung und Fibrose führen und letztendlich in diabetischer Kardiomyopathie vom Phänotyp der „heart failure with reduced ejection fraction» (HFREF) resultieren.
Obwohl die arterielle Hypertonie ähnliche Veränderungen induziert, wird die HFNEF-Entwicklung mehr durch Übergewicht und Diabetes vorangetrieben als durch arterielle Hypertonie. Die diabetische Kardiomyopathie des HFNEF-Phänotyps ist also eine eigene Entität und eine verbreitete kardiale Funktionsstörung.
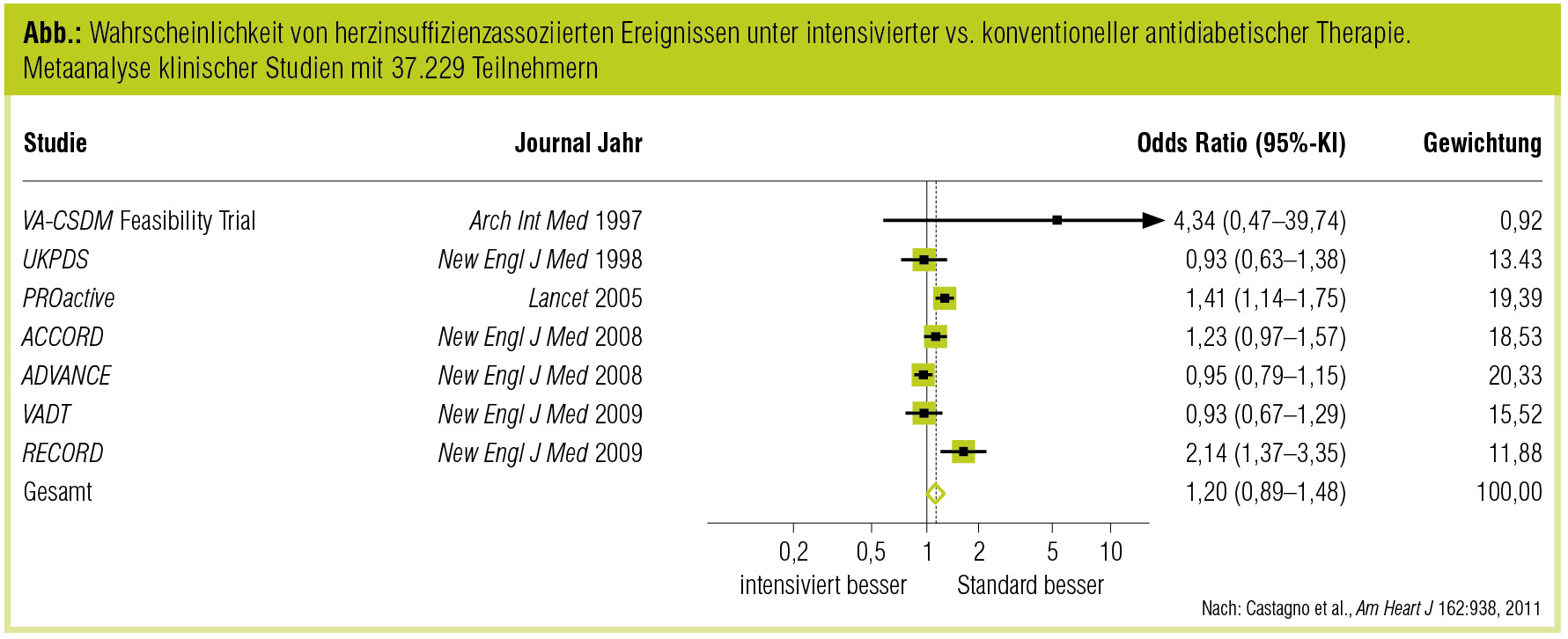
In einer 2011 publizierten Metaanalyse von 37.229 Patienten (Castagno et al., Am Heart J 2011) konnte eine intensivierte Blutzuckerkontrolle die Rate von Herzinsuffizienzereignissen bei Typ-2-Diabetikern im Vergleich zur Standardtherapie nicht senken (Abb.). Die Autoren stellten aufgrund dieses Ergebnisses das Vorhandensein einer direkten mechanistischen Verbindung zwischen Hyperglykämie und Herzinsuffizienz infrage. Andererseits konnte eine positive Assoziation zwischen HbA1c-Werten und dem Risiko für eine Herzinsuffizienz bei Patienten mit Typ-1-Diabetes gezeigt werden (Lind et al., Lancet 2011).
Proof-of-Concept-Studien mit Inkretintherapeutika
Bei Herzinsuffizienz wechselt der Metabolismus des Herzens vom Fettsäure- zum Glukosemetabolismus. Der Glukosemetabolismus hat eine bessere Energieeffizienz. Dadurch wird eine Sauerstoffersparnis von 11 % für die Produktion eines jeden ATP-Moleküls erreicht. Die Entwicklung von Insulinresistenz stört die Effizienz dieses Mechanismus. Einen potenziellen Vorteil könnten hier inkretinbasierte Therapien, einerseits mit GLP-1-Analoga, andererseits mit DPP-4-Inhibitoren, bieten.
Wie im Rahmen des „Heart Failure Congress“ der European Society of Cardiology (ESC) im Mai 2012 in Belgrad (Serbien) dargelegt, wurden „Proof of Concept“-Studien zur Inkretintherapie der Herzinsuffizienz durchgeführt. Die Therapie besteht in einer kurzzeitigen intravenösen Therapie oder einer längeren oralen oder subkutanen Therapie. Tierstudien haben auf günstige kardiovaskuläre Effekte hoffen lassen, z. B. konnte eine Verbesserung der linksventrikulären Ejektionsfraktion (LVEF) durch Inkretine bei Hunden mit Herzinsuffizienz gezeigt werden. Unkontrollierte Studien an Menschen zeigen laut John McMurray (Glasgow, Großbritannien) ebenfalls Hinweise für günstige kardiovaskuläre Effekte, z. B. eine Steigerung der LVEF bei Patienten nach akutem Myokardinfarkt und bei Patienten mit systolischer Herzinsuffizienz. Es wurde jedoch bisher nur eine placebokontrollierte randomisierte Studie an Patienten mit Herzinsuffizienz durchgeführt: 20 Patienten mit Herzinsuffizienz NYHA II oder III und einer LVEF < 40 % wurden eingeschlossen. Durch eine 48 Stunden dauernde GLP-1-Infusion kam es jedoch zu einem leichten Anstieg von Herzfrequenz und diastolischem Blutdruck, die LVEF verbesserte sich nicht (Halbirk et al., Am J Physiol Heart Circ Physiol 2010). Die Steigerung von Herzfrequenz und Blutdruck ist unerwünscht, was das Ergebnis dieser Studie ernüchternd wirken lässt. Größere Studien sind aktuell am Laufen.
Therapie der Herzinsuffizienz bei Diabetes mellitus
In den im Mai 2012 publizierten neuen ESC-Guidelines zum Management der Herzinsuffizienz (McMurray et al., Eur Heart J 2012) wird auf folgende Substanzen im Speziellen eingegangen:
Angiotensinrezeptorblocker (ARB) und möglicherweise auch ACE-Hemmer könnten einen präventiven Effekt auf die Inzidenz von Diabetes mellitus haben (NAVIGATOR-Studie; McMurray et al., N Engl J Med 2010); sie sind bei Patienten mit Diabetes ebenso indiziert wie bei Patienten ohne Diabetes.
Betablocker sind ausdrücklich nicht kontraindiziert bei Diabetes und sind bei Patienten mit Diabetes in der Verbesserung des klinischen Outcomes vergleichsweise effektiv wie bei Nichtdiabetikern. Betablocker sollten also Patienten mit Diabetes keinesfalls vorenthalten werden (GEMINI-Studie; Bakris et al., JAMA 2004).
Zusammenfassend kann folgende Empfehlung ausgesprochen werden: ACE-Hemmer, ARB und Betablocker werden zur Behandlung von Herzinsuffizienz bei Diabetikern empfohlen. Diese Medikamente reduzieren signifikant die Gesamtmortalität, die kardiovaskuläre Mortalität und die Hospitalisierungen durch Herzinsuffizienz. Zusätzlich sollen Aldosteronantagonisten, Diuretika und Ivabradin entsprechend ihrer Indikation verwendet werden.
Diabetestherapie bei Herzinsuffizienz
Pioglitazon verursacht eine Natrium- und Wasserretention und erhöht das Risiko einer Verschlechterung der Herzinsuffizienz und einer Hospitalisierung und sollte daher vermieden werden (Komajda et al., Eur Heart J 2010; Hernandez et al., Am J Cardiovasc Drugs 2011; Erdmann et al., Diabetes Care 2007). Allerdings ist die Herzinsuffizienzsterblichkeit unter Pioglitazon nicht erhöht. Die durch Pioglitazon induzierte Herzinsuffizienz scheint also besonders benigne zu sein. Die Furcht vor einer inzidenten Herzinsuffizienz sollte also nicht von einer geplanten Therapie mit Pioglitazon abhalten.
Formal besteht bei Herzinsuffizienz eine Kontraindikation gegen Metformin. Viele Diabetologen geben aber bei Patienten mit Diabetes und Herzinsuffizienz dennoch Metformin. Dies scheint sicher zu sein: In der Tat haben bei herzinsuffizienten Patienten mit Diabetes in epidemiologischen Studien jene, die Metformin erhalten, die geringste Sterblichkeit (MacDonald et al., Diabetes Care 2010; Tab. 2). Für eine definitive Beurteilung des Nutzen-Risiko-Verhältnisses von Metformin bei Herzinsuffizienz wäre natürlich eine randomisierte Studie notwendig. Wir selbst geben Metformin bei herzinsuffizienten Diabetespatienten dann, wenn keine anderen Kontraindikationen vorliegen (im Besonderen keine schwere Niereninsuffizienz) und wenn keine akute Dekompensation besteht bzw. zu befürchten ist.
Über die Sicherheit neuerer antidiabetischer Medikamente (und ihre möglichen Vorteile) gibt es noch wenige Daten.