Kardiorenoprotektion mit SGLT2i und GLP-1-RA: Bestandsaufnahme und Aufruf zur Veränderung
Kardiovaskuläre Ereignisse stellen bei Patienten mit Typ-2-Diabetes noch immer die häufigste Todesursache dar1, wobei das kardiovaskuläre Mortalitätsrisiko bei Patienten mit renalen Komorbitäten besonders ausgeprägt ist.2 Vor diesem Hintergrund zählt die Reduktion des kardiorenalen Risikos bei Patienten mit hohem kardiovaskulären und/oder renalen Risiko zu den Hauptzielen im erfolgreichen Management des Typ-2-Diabetes.3, 4
Wie kann eine Risikoreduktion gelingen?
Mit der kardiovaskulären Endpunktstudie (CVOT) EMPA-REG Outcome im Jahr 2015 konnte erstmals ein kardiovaskulärer Vorteil eines Wirkstoffs (Empagliflozin) bei Patienten mit T2D und kardiovaskulärer Erkrankung (CVD) demonstriert werden5; 2016 folgte mit LEADER eine weitere positive CVOT.6 Mittlerweile zeigten weitere Vertreter der Wirkstoffklassen SGLT-2-Inhibitoren (i) und GLP-1-Rezeptoragonisten (RA) kardiovaskuläre Vorteile,7–12 die Studienergebnisse legen zudem einen renoprotektiven Effekt beider Wirkstoffklassen nahe.3, 4, 13, 14 Dementsprechend wird der Einsatz von SGLT2i sowie GLP-1-RA in internationalen Leitlinien in der medikamentösen Zweitlinie nach Metformin bei T2D-Patienten mit manifestem bzw. hohem Risiko für kardiovaskuläre und/oder renale Erkrankungen empfohlen.3, 4
Ein Blick in die Verschreibungspraxis
Trotz der unbestrittenen und durch Evidenz belegten Vorteile der beiden Wirkstoffklassen zeigt ein Blick in die Verschreibungspraxis ein anderes Bild: Aus einer deskriptiven US-amerikanischen Analyse ging hervor, dass der Anteil der Patienten unter SGLT2i-Therapie nach Publikation der EMPA-REG-OUTCOME-Studie von 4,1 % (2015) nur auf 7,2 % (2018) anstieg. Ähnliches zeigte sich auch für den Einsatz von GLP-1-RA, wobei der Einsatz nach Publikation von LEADER auf 8,2 % zunahm (Ausgangswert 4,2 %); interessanterweise blieb die Verschreibung von DPP4-Hemmern in diesem Zeitraum konstant, obwohl für diese Substanzklasse in CVOTs neutrale Effekte auf kardiorenale Ereignisse dokumentiert wurden.15 Das bedeutet, dass ein Großteil der Patienten – auch Jahre nach Veröffentlichung der Studien – nicht von einer antidiabetischen Therapie mit belegten kardiorenalen Zusatzeffekten profitieren konnte.14 SGLT2i und GLP-1-RA dürften in Europa sogar noch seltener angewendet werden, wie eine dänische Datenbankanalyse nahelegt: nur 4 % aller erfassten T2D-Patienten wurden mit SGLT2i, 8 % mit GLP-1-RA behandelt, eine ASCVD bestand bei nur 28–29 % der Patienten. Aus diesen Ergebnissen geht hervor, dass die antidiabetische Therapie nicht optimal auf die individuellen Bedürfnisse und unter Berücksichtigung aller Komorbiditäten abgestimmt wurde.14
Eine weitere US-amerikanische Datenbankanalyse16 der Jahre 2013–2018 lässt zuletzt eine Trendwende erkennen, die unter anderem auf Indikationserweiterungen (z. B. auf Patienten mit Herzinsuffizienz mit oder ohne T2D) und die folglich gesteigerte Awareness für die positiven Effekte dieser Substanzklassen zurückzuführen sein dürfte. Empagliflozin war demzufolge der am häufigsten verschriebene SGLT2i, getrieben wurde dieser Anstieg von einem verstärkten Einsatz bei Patienten mit bestehender Herzinsuffizienz. Der Einsatz von Canagliflozin nahm in derselben Zeitspanne drastisch ab, vermutlich aufgrund einer Black-Box-Warnung der FDA für eine erhöhte Amputationsrate. In der Klasse der GLP-1-RA wurde Dulaglutid – trotz der positiven Ergebnisse der Liraglutid-Studie LEADER – am häufigsten verschrieben; dies dürfte auf einfachere/niederfrequente Anwendung und Kostengründe zurückzuführen sein. Liraglutid wurde jedoch häufiger bei Patienten mit Herzinsuffizienz eingesetzt.
Die Erstverschreibung beider Substanzklassen erfolgte überwiegend von Endokrinologen, während die Verschreibungsrate in der Kardiologie sehr gering ausfiel – auch bei Patienten mit etablierter CVD.16
Welche Faktoren beeinflussen Inertia?
Um eine Verbesserung der Verschreibungssituation zu erreichen ist es unumgänglich, die Hintergründe des bisher eher zögerlichen Einsatzes der beiden Wirkstoffklassen zu verstehen. Eine internationale Gruppe von Diabetologen*, die der Diskrepanz zwischen Studienergebnissen, potenziellem Patientennutzen und der tatsächlichen klinischen Praxis mit Besorgnis gegenübersteht, kam in Diskussionen zum Schluss, dass Inertia eine – wenn nicht die – Haupthürde für den Einsatz der neuen Substanzklassen SGLT2i und GLP-1-RA darstellt.14 Einige Faktoren, die die therapeutische Trägheit fördern (Abb. 1), werden im Folgenden kurz umrissen.
- Erfahrung, Studienwissen: Unsicherheiten aufgrund der noch geringen Erfahrung mit der Verschreibung und dem Umgang mit neuen Substanzklassen können dazu führen, dass altbekannte Medikamente bevorzugt verschrieben werden. Weiters dürften die kardiorenalen Vorteile, die in CVOTs erzielt wurden, nicht allen Kollegen, vor allem im Primärversorgungssektor, in vollem Umfang bekannt sein. In diesem Zusammenhang wurde gezeigt, dass die klinische Trägheit in Hinblick auf glykämische Kontrolle in der Primärversorgung besonders ausgeprägt ist, wobei auch im spezialisierten Bereich eine beträchtliche Inertia besteht.17, 18 Ähnliches dürfte auch auf das kardiorenale Risikomanagement zutreffen, dem vor Integration von CVOT-Ergebnissen in internationale Leitlinien insgesamt unzureichende Aufmerksamkeit zukommt.19
- Der interdisziplinäre Austausch – zwischen PCPs/Endokrinologen und Kardio- oder Nephrologen – ist in vielen Bereichen nur eingeschränkt oder nicht vorhanden. Dieser Umstand kann dazu führen, dass CVD und chronische Nierenerkrankungen (CKD) bei Patienten mit T2D noch immer unterdiagnostiziert werden. Die Vorteile einer multidisziplinären Zusammenarbeit konnten bereits in Hinblick auf Gewichtsmanagement20 und glykämische Kontrolle17 demonstriert werden, sodass ähnliche Erfolge bezüglich des kardiovaskulären Risikomanagements erwartet werden können.
- „Richtig“ priorisieren: Die Rolle der Interdisziplinarität weist bereits auf eine weitere Hürde der adäquaten Patientenversorgung hin: Typ-2-Diabetes ist mit einer Reihe von Komorbiditäten assoziiert; betreuende Ärzte stehen vor der Herausforderung, diese zu diagnostizieren, zu priorisieren und zu behandeln, wobei „offensichtlichen“ Erkrankungen (z. B. Adipositas) oder mit Symptomen assoziierten Komplikationen (Hypoglykämie) tendenziell ein höherer Stellenwert eingeräumt wird21 als symptomatisch subtileren, dennoch mit hohem Risiko assoziierten Erkrankungen (CVD, HF, CKD).
- Therapie evaluieren, anpassen: Das kardiorenale Risiko nimmt im Diabetesverlauf zu22, 23; dennoch ist es vielen Patienten nicht möglich, regelmäßige Arzttermine mit Therapiekontrollen und gegebenenfalls -anpassungen vorzunehmen. Veränderungen des kardiorenalen Status können dadurch verzögert dokumentiert, die Anpassung der Behandlung auf Wirkstoffe mit kardiovaskulären oder renalen Vorteilen erst verspätet durchgeführt werden.
Wie kann Veränderung herbeigeführt werden?
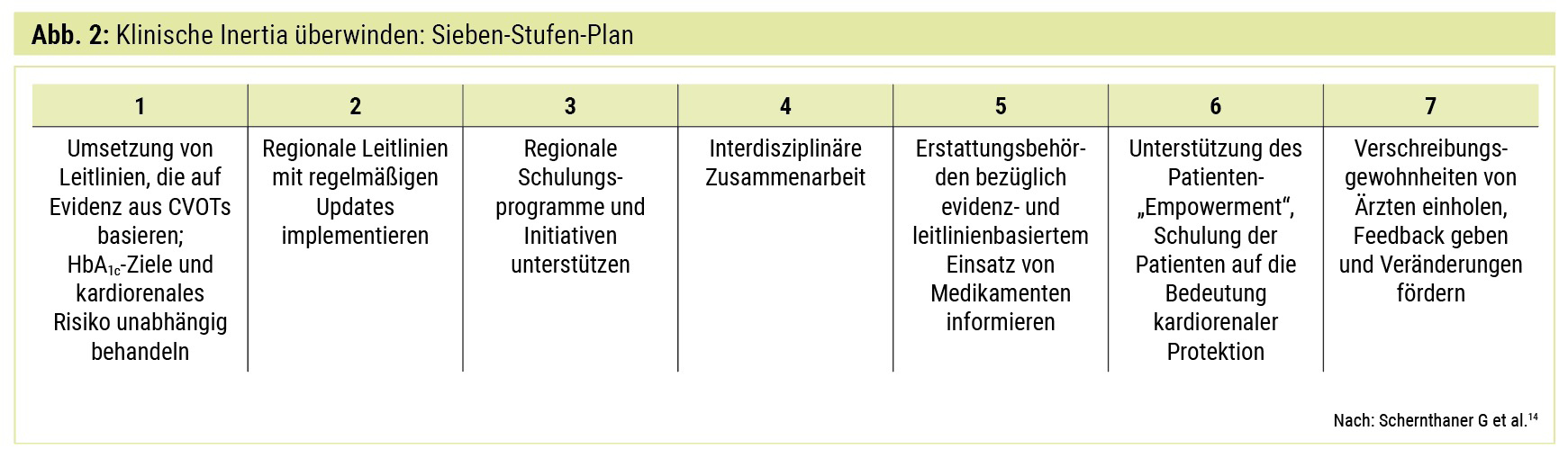
Auf Basis eigener klinischer Erfahrung und Expertise und rezenter Literatur zum Thema Inertia erstellte die internationale Diabetologengruppe um Prof. Schernthaner ein Manifest, das Lösungsvorschläge sowie eine siebenstufige Handlungsempfehlung umfasst (Abb. 2). Dieses Manifest soll behandelnde Ärzte dabei unterstützen, regionale Verschreibungsgewohnheiten zugunsten der Patienten zu verändern.
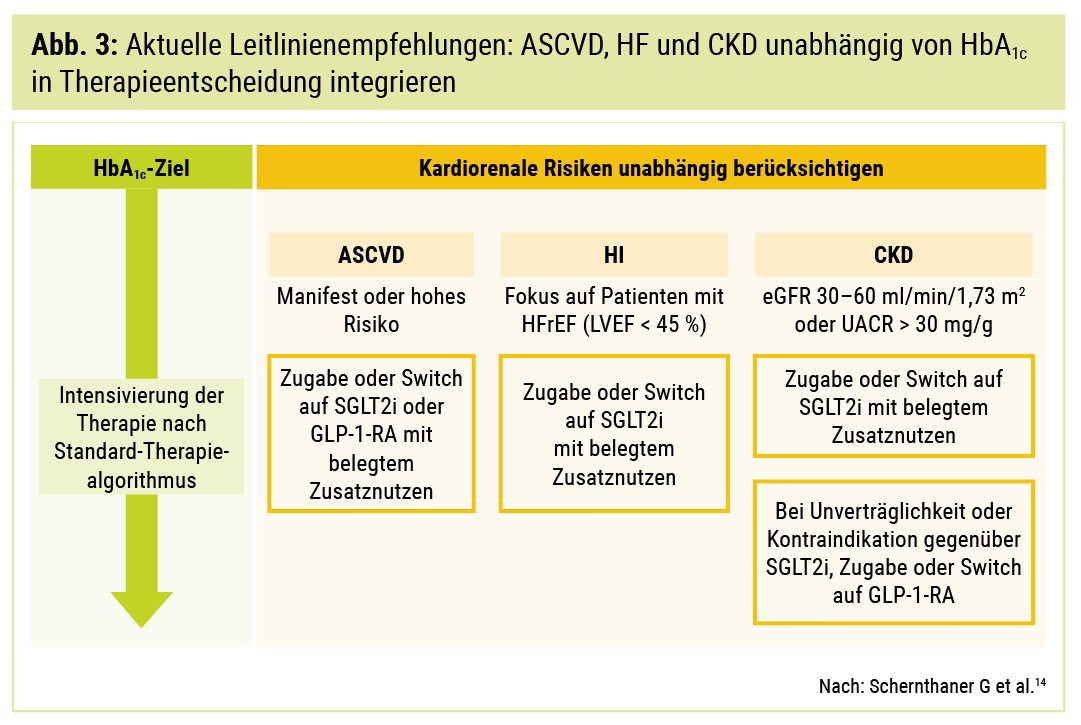
Mit aktuellen internationalen Leitlinien der Fachgesellschaften ADA, EASD und ESC wurde ein Paradigmenwechsel im Management des T2D herbeigeführt: im Gegensatz zum glukosezentrierten Ansatz – Intensivierung/Zugabe weiterer Medikamente bei unzureichender glykämsicher Kontrolle – wird nun empfohlen, dass das Risiko für atherosklerosebedingte Erkrankungen (ASCVD), Herzinsuffizienz (HI) und CKD unabhängig von der Stoffwechsellage in die Therapieentscheidung einbezogen werden soll (Abb. 3).3, 4, 24
Die breite Umsetzung dieser Empfehlungen in der klinischen Praxis stellt demnach einen zentralen und unumgänglichen Schritt für die Überwindung der klinischen Inertia dar.
|
KOMMENTAR
Adhärenz zu Lebensstilempfehlungen wäre gerade bei Menschen mit Diabetes mellitus als Teil der Krankheitstherapie, aber auch zur Prävention von Komplikationen und Folgeerkrankungen extrem wichtig, sie ist jedoch leider oft gering ausgeprägt. Ein Grund dafür ist, dass Lebensstilfaktoren und -gewohnheiten sehr häufig über viele Jahrzehnte bestehen und eventuell auch zur Entstehung der Krankheit beigetragen haben. Gründe für die fehlende Adhärenz sind meist nicht fehlendes Wissen oder mangelnde Einsicht, wie das leider viel zu oft missinterpretiert wird. Verhaltensänderungen sind komplex, schwierig, langwierig, mit Rückschlägen verbunden und erfordern das ständige Arbeiten an sich selbst sowie an der sozialen und der gebauten Umwelt. Viele Modelle wurden erprobt, evaluiert und publiziert, wie Verhaltensänderungen bei Menschen mit chronischen Erkrankungen implementiert werden können. |
|
KOMMENTAR
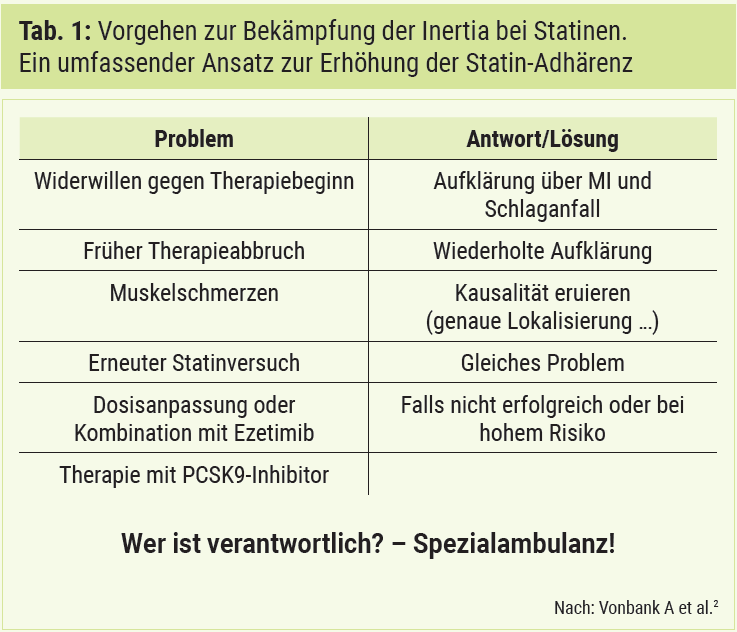
Inertia ist auch in der kardiovaskulären Pharmakotherapie ein Problem und eine Herausforderung. Passend zum Abschied von der glukozentrischen Diabetestherapie haben wir mit und ohne Diabetes die gleichen Probleme bei der lipidsenkenden Therapie und Hochdrucktherapie. In wesentlich geringerem Maße gilt dies auch für die Herzinsuffizienztherapie, weil im Gegensatz zur Lipidsenkung und Hochdrucktherapie ein Mangel an Adhärenz sehr schnell zu Symptomen führt. In der lipidsenkenden Therapie liegt die Verschreibungspraxis sowohl für Statine als auch für Ezetimib und PCSK9-Hemmung durch monoklonale Antikörper weit hinter den Erfordernissen zurück. Zum Beispiel ist sowohl in der Schweiz als auch in Österreich die Zahl der Verschreibungen von PCSK9-Antikörpern nur etwa halb so groß wie es die Erstattungsrichtlinien erlauben würden. Das grundsätzliche Problem der Statinintoleranz ist nicht rational. Stroes ES et al. haben gezeigt, dass wirklich kausale Statinmyopathie etwa um eine 10er-Potenz seltener ist als die klinisch vermutete.1 Die Arbeitsgruppe für kardiovaskuläre Pharmakotherapie der ESC hat daraufhin ein Positionspapier veröffentlicht (Vonbank A et al. 2017).2 Tabelle 1 zeigt ein Vorgehen zur Bekämpfung der Inertia bei Statinen. Bei Post-Infarkt-Patienten erwies sich zusätzlich als vorteilhaft, um multiple Barrieren zu überwinden, dass bereits auf der CCU die kombinierte Lipidtherapie durchgeführt wird.
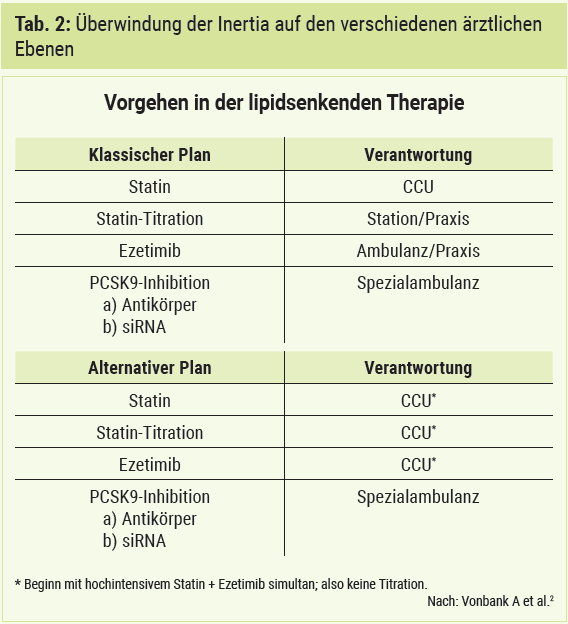
Der in Tabelle 2 gezeigte Plan B ist gegenüber dem Plan A wesentlich besser zur Überwindung der Inertia auf den verschiedenen ärztlichen Ebenen (Intensivstation, Allgemeinstation, Niederlassung, Spezialambulanz). Dieser Plan B ist auch mit den ESC/EAS-Leitlinien konform, wenngleich die direkte Empfehlung der Leitlinien eher dem Plan A entspricht (Mach F et al. 2019).3
Bei Hypertonie ist eine interessante Neuerung belegt (Kahan T 2021; Jackson R & Wells S 2021).4, 5 Hier zeigt z. B. die QUARTETT-Studie (Chow CK et al. 2021)6 einen neuen Weg, nämlich mit einer multiplen niederdosigen Therapie zu beginnen und damit von vornherein eine bessere Adhärenz zusammen mit guter Wirksamkeit zu belegen. Hier wie auch in der Lipidologie ist das Konzept der Polypill ebenso dazu angelegt, die Inertia zu minimieren. Dies ist zwar noch nicht endgültig als Empfehlung zu verstehen, könnte aber eine zusätzliche Überlegung zu der sehr schönen, im Hauptartikel dargestellten Vorgangsweise bieten. Die LDL-Zielwert-Erreichung scheint im Übrigen bei Diabetes etwas besser zu sein als ohne Diabetes, wie unlängst an einer pAVK-Population gezeigt wurde (Saely CH et al. 2020).7 Allerdings ist die Zielwerterreichung bei Diabetes zwar besser als ohne Diabetes, aber immer noch sehr schlecht. Die mangelnde Zielwerterreichung beim LDL-Cholesterin wurde durch die DA-VINCI-Studie eindrücklich aktuell bestätigt (Vrablik M et al. 2021). ResümeeZusammenfassend ist also aus der Kardiologie eine sehr ähnliche Situation der Inertia zu bestätigen, wie wir sie in der Diabetologie finden. Inertia ist einerseits mit Latenz des Wissens von der Wissenschaft bis zur Verschreibungspraxis und andererseits durch die nicht fühlbare Wirkung der LDL-Senkung überzeugend erklärt. 1 Stroes ES et al., Eur Heart J 2015; 36: 1012–22 |