Metformin bei Niereninsuffizienz: Die Zulassungsgrenzen verschieben sich
Das Biguanid Metformin ist gegenwärtig unumstritten die zentrale antidiabetische Therapieoption für Patienten mit Typ-2-Diabetes (American Diabetes Association, Diabetes Care 2012; Inzucchi et al., Diabetologia 2012; Clodi et al., Wien Klin Wochenschr 2012). Eine derartige Dominanz eines einzelnen Medikaments findet sich in wenigen anderen medizinischen Fächern und ist umso bemerkenswerter, wenn man bedenkt, dass Metformin schon 1958 erstzugelassen wurde und seitdem eine höchst wechselhafte Geschichte durchlebt hat. So stand Metformin nach der Publikation der UGDP-Studie (JAMA 1971) und den Berichten über fatale Laktazidosen im Zusammenhang mit anderen Vertretern der Substanzklasse (Buformin, Phenformin) praktisch vor dem Aus. In den meisten europäischen Ländern wurde Metformin erst 1979 zugelassen, in den USA ist die Substanz seit 1995, in Deutschland in der Monotherapie gar erst seit 1998 verfügbar.
Der Siegeszug von Metformin begann mit dem wiedererwachten Interesse für die Rolle der Insulinresistenz in der Pathophysiologie des Typ-2-Diabetes und mehr noch mit der in der UKPDS beobachteten Reduktion kardiovaskulärer Endpunkte (UKPDS Group, Lancet 1998). Und auch wenn die Evidenz dafür im Rückblick auf recht dünnen Beinen steht und die möglichen kardiovaskulären Vorteile und krebsprotektiven Eigenschaften von Metformin auch kritisch hinterfragt werden (z. B. Lamanna et al., Diabetes Obes Metab 2011; Stevens et al., Diabetologia 2012), so wird sich an der zentralen Stellung von Metformin in der antihyperglykämischen Therapie des Typ-2-Diabetes auch in den kommenden Jahren wenig ändern.
Gefährdungspotenzial von Metformin
Neben gastrointestinaler Unverträglichkeit ist Nephropathie die bedeutsamste Limitation für den Einsatz vom Metformin. Bei eingeschränkter Nierenfunktion sinkt die renale Clearance von Metformin proportional zur Kreatininclearance (Graham et al., Clin Pharmacokinet 2011). Die resultierende Akkumulation wird mit einem geringen Risiko für Laktazidosen in Zusammenhang gebracht. Literaturangaben zur Häufigkeit von Metformin-assoziierten Laktazidosen (MALA) schwanken von weniger als einem bis zu acht Fällen pro 100.000 Patienten und Jahr, die Mortalität wird mit bis zu 50 % angegeben. Ein Kausalzusammenhang mit der Akkumulation von Metformin ist allerdings nicht eindeutig belegt (Bailey et al., New Engl J Med 1996; Lipska et al., Diabetes Care 2011). Eine systematische Metaanalyse von 347 Vergleichs- und Kohortenstudien ergab für Metformin eine statistische Obergrenze der Laktazidoseinzidenz von 4,3 Fällen (Metformin) vs. 5,4 Fällen (Vergleichsgruppen) pro 100.000 Patienten und Jahr (Salpeter et al., Cochrane Database Syst Rev 2010). Die meisten der in der Literatur berichteten MALA-Fälle standen in Zusammenhang mit der Nichtbeachtung einer oder mehrerer Kontraindikationen gegenüber Metformin, darunter vor allem Niereninsuffizienz, häufig gepaart mit Zuständen, die eine reduzierte Gewebeperfusion oder Hypoxie zur Folge haben, Lebererkrankungen oder Alkoholabusus (Bailey et al., New Engl J Med 1996).
Auf Basis der Erfahrungen mit Phenformin wurde als Schwellenwert für die Metformin-Kontraindikation zunächst ein Serumkreatinin von 1,5 mg/dl (Männer) bzw. 1,4 mg/dl (Frauen) festgelegt. Nach der aktuell geltenden Fachinformation markiert eine glomeruläre Filtrationsrate (GFR) von 60 ml/min die renale Untergrenze für den Einsatz von Metformin. Bei allem Bemühen, die Patienten keinen potenziell gefährlichen Nebenwirkungen auszusetzen, muss man sich aber bewusst sein, dass diese Vorgabe in klinischen Studien ebenso wie in der therapeutischen Praxis häufig missachtet wurde und wird:
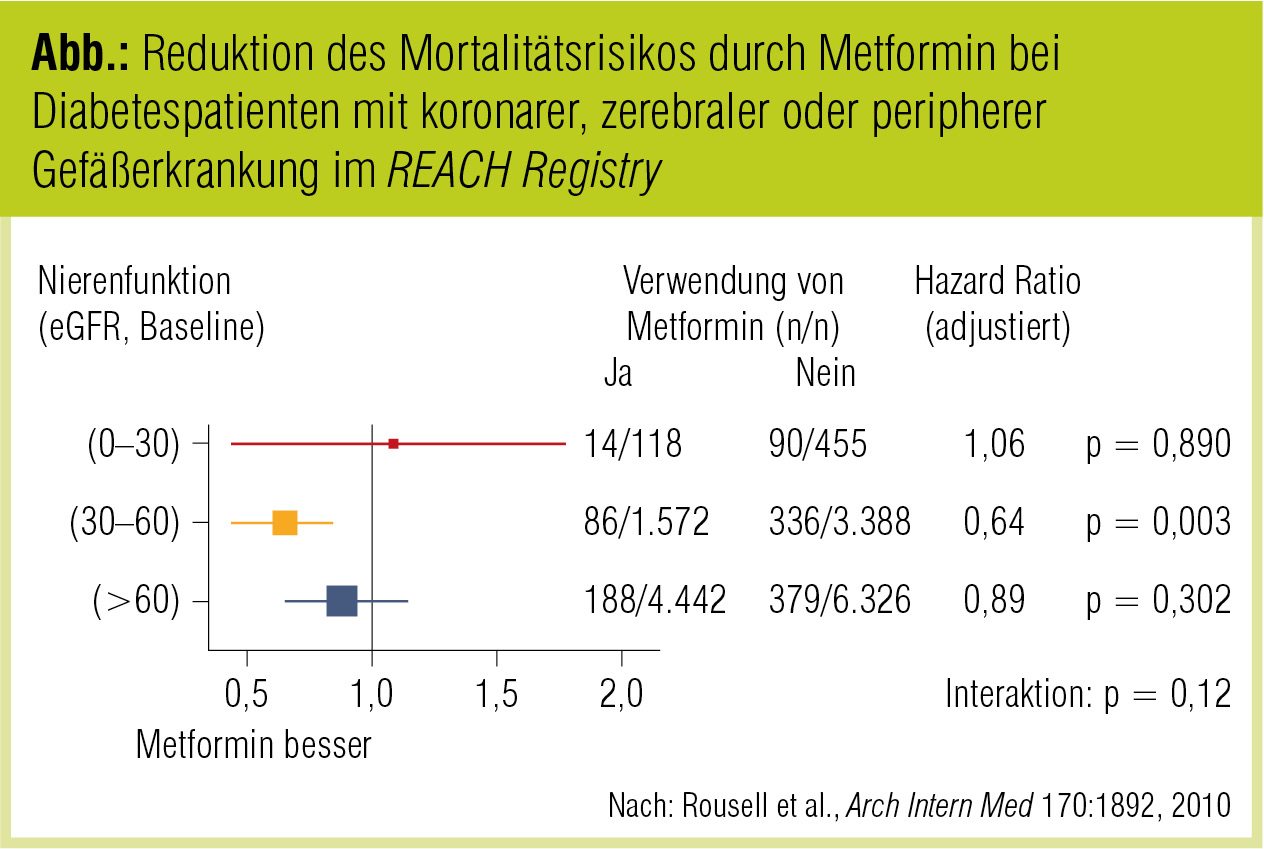
In der PROactive-Studie erhielt jeder zweite Teilnehmer mit einer mittleren errechneten glomerulären Filtrationrate (eGFR) von Metformin in Monotherapie (7,9 %), in Kombination mit einem Sulfonylharnstoff (24,3 %) oder mit Insulin (18,9 %; Schneider et al., J Am Soc Nephrol 2008). In der TREAT-Studie (Pfeffer et al., N Engl J Med 2009), die über 48 Monate Darbopoetin alpha vs. Placebo bei Patienten mit mittelgradiger Nephropathie untersuchte, erhielten 17 % der Teilnehmer mit moderater Nierenfunktionseinschränkung (mediane eGFR: 34 ml/min; Interquartilen-Range: 27–43 ml/min) Metformin. Die Auswertung des REACH Registry (Roussel et al., Arch Intern Med 2010), die den Effekt von Metformin auf die 2-Jahres-Mortalität von ca. 20.000 Diabetespatienten mit atherosklerotischen Gefäßerkrankungen korrelierte, inkludierte in der Metformingruppe 1.690 Patienten im Stadium 3–4 der chronischen Nierenerkrankung (CKD). In keiner dieser Studien ist ein Fall von Laktazidose dokumentiert. In der REACHStudie profitierten Patienten mit einer eGFR von 30–60 ml/ min/1,73 m2 sogar stärker von Metformin als jene mit einer eGFR > 60 ml/min/1,73 m2 (Abb.).
Für eine Analyse des schwedischen Nationalen Diabetesregisters inkludierten Ekström et al. (BMJ open 2012) rezent die Daten von mehr als 50.000 Patienten mit Typ-2-Diabetes und erhoben den Einfluss von Metformin auf die Inzidenz von kardiovaskulären Erkrankungen, Gesamtmortalität sowie typischen Anzeichen einer Laktazidose (Azidose, schwerwiegende Infektionen, Schock oder Nierenversagen) in Relation zum renalen Status über 3,9 Jahre. Im Vergleich zu anderen oralen Antidiabetika (zu 80 % Sulfonylharnstoffe) oder Insulin in Monotherapie oder in Kombination mit Metformin war die Metformin-Monotherapie mit einem signifikant geringeren Risiko für die untersuchten Endpunkte assoziiert; dies galt für Patienten mit einer eGFR von 45–60 ml/min/1,73 m2 in gleicher Weise wie für jene mit höherer Filtrationsraten. Außerdem fand sich in der Gruppe mit einer eGFR von 30–45 ml/min/1,73 m2 auf Basis der verwendeten Surrogatmarker kein erhöhtes Laktazidoserisiko.
Auch auf den Verlauf der diabetischen Nephropathie dürfte Metformin keinen negativen Einfluss haben, wie die retrospektive Auswertung von über 93.500 Datensätzen der National Veterans Administration Database in den USA nahelegt (Hung et al., Kidney Int 2012). Demnach kam es bei Patienten mit Typ-2-Diabetes und einer eGFR > 60 ml/min/1,73 m2, die 4 Jahr lang Metformin einnahmen, ähnlich häufig zum einem eGFR-Abfall um ≥ 25 % oder zu terminalem Nierenversagen wie bei Patienten, denen im gleichen Zeitraum Rosiglitazon verschrieben wurde, aber signifikant seltener als bei Patienten, die Glibenclamid erhielten (adjustierte Hazard Ratio = 1,20). Die Überlegenheit von Metformin gegenüber dem Sulfonylharnstoff war unabhängig von Alter, ethnischem Hintergrund, HbA1c-Einstellung oder Therapie mit ACI-Hemmern bzw. Angiotensinrezeptorblockern.
Determinanten des Laktazidoserisikos
Dass wir beim Einsatz von Metformin in der klinischen Praxis dennoch vorsichtig sein sollten, zeigt eine rezente Publikation aus einem niederländischen Krankenhaus (van Berlo-van de Laar et al., J Clin Pharm Ther 2011), die bei der Sichtung der Krankenakten von ca. 7.500 Personen mit Typ-2-Diabetes aus den Jahren 2000–2008 (davon 50 % mit Metformintherapie) immerhin 16 Fälle von MALA fanden; das entspricht einer Inzidenz von 47 pro 100.000 Patientenjahren und ist damit massiv mehr als in der Literatur angegeben. Die Autoren betonen zwar, dass in 11 Fällen Risikofaktoren für Laktazidose aus der Anamnese ersichtlich waren und 13 der betroffenen Patienten mit Nierenversagen aufgenommen wurden, dennoch bleibt anzumerken, dass vor allem in kränkeren Kollektiven, wie sie für Zentren charakteristisch sind, mit einem höheren Anteil vulnerabler Patienten gerechnet werden muss.
Ebenso wichtig erscheint der Befund der niederländischen Gruppe, dass MALA-Überlebende signifikant höhere Metformin-Serumspiegel aufwiesen als jene, die infolge der Komplikation verstarben (18,9 mg/l vs. 2,9 mg), während die Laktatspiegel zwischen den Gruppen nicht signifikant unterschiedlich waren. Dies spricht dafür, dass das Mortalitätsrisiko bei Patienten mit MALA primär nicht durch die Akkumulation von Metformin, sondern durch die allgemeine Morbidität determiniert wird.
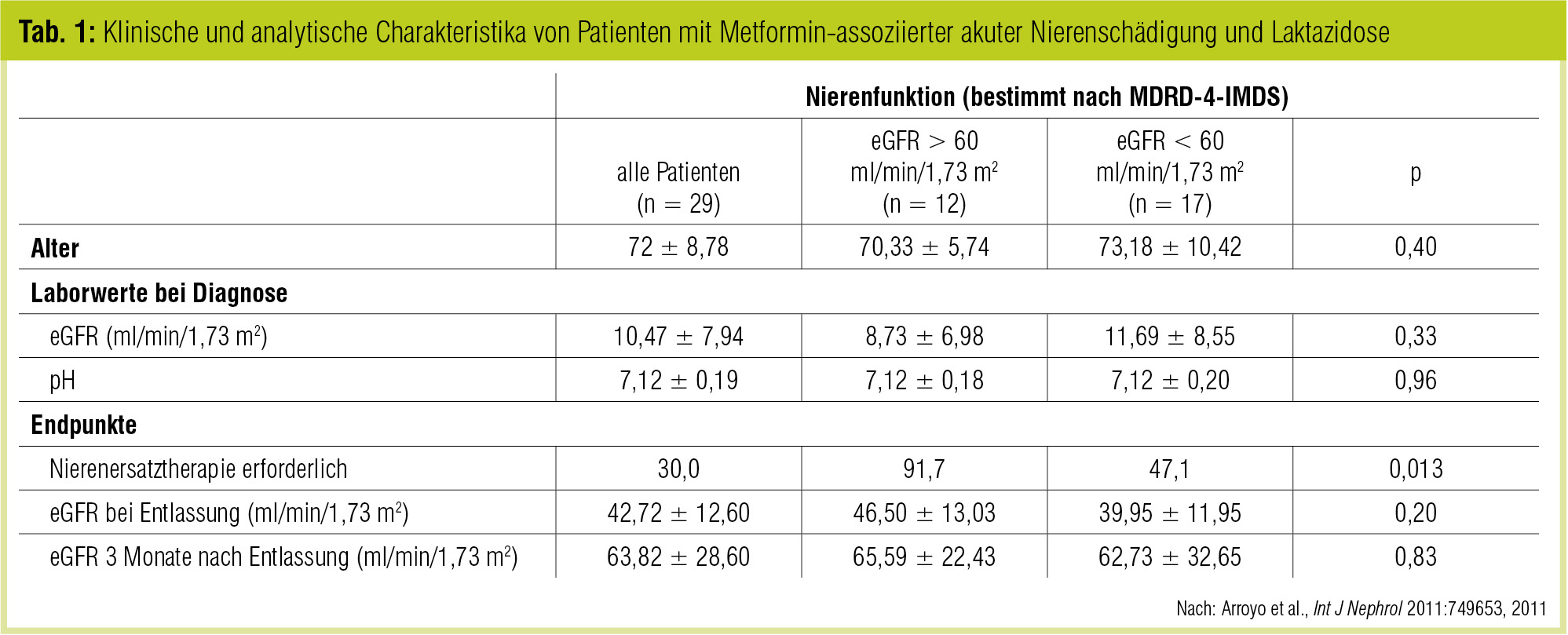
In die gleiche Richtung weist die Analyse von 29 Fällen von Metformin-assoziierter Nierenschädigung bzw. Laktazidose im Universitätshospital Madrid zwischen 2006 und 2010 (Arroyo et al., Int J Nephrol 2011), die nahelegt, dass Metformin bei Diabetespatienten mit eingeschränkter Nierenfunktion im seltensten Fall als alleiniger Verursacher schwerwiegender Komplikationen auftritt, sondern dass Begleitmedikamente, vor allem ACE-Hemmer, ARB und nichtsteroidale Antirheumatika (NSAR) oder schwerwiegenden Komorbiditäten mit eine Rolle spielen. Es zeigt sich aber auch, dass Personen mit initial schlechterer Nierenfunktion eine ungünstigere renale Prognose haben, wenn im Zusammenhang mit der Metformingabe eine solche Komplikation auftritt (Tab. 1).
Nationale und internationale Empfehlungen
In den aktualisierten Praxisleitlinien der Österreichischen Diabetes Gesellschaft (Clodi et al., Wien Klin Wochenschr 2012; Auinger et al., Wien Klin Wochenschr 2012) gilt eine eingeschränkte Nierenfunktion (GFR < 60 ml/min) weiterhin als Metformin-Kontraindikation. Es wird aber darauf verwiesen, dass immer mehr Daten für die prinzipielle Sicherheit von Metformin auch bei Patienten mit einer GFR < 60 ml/min sprechen und Metformin entsprechend den britischen NICE-Guidelines (2009) bis zu einer eGFR von 45 ml/min/1,73m2 verabreicht werden kann. Eine ähnliche Vorgehensweise propagiert auch die Schweizerische Gesellschaft für Endokrinologie und Diabetologie (Zanchi et al., Swiss Med Wkly 2012; siehe Beitrag Möglichkeiten und Grenzen der antidiabetischen Therapie). Bei schweren Infektionen, Diarrhö oder Exsikkose und ebenso perioperativ und vor Verabreichung eines Röntgenkonstrastmittels sollte Metformin jedoch vorübergehend pausiert werden.
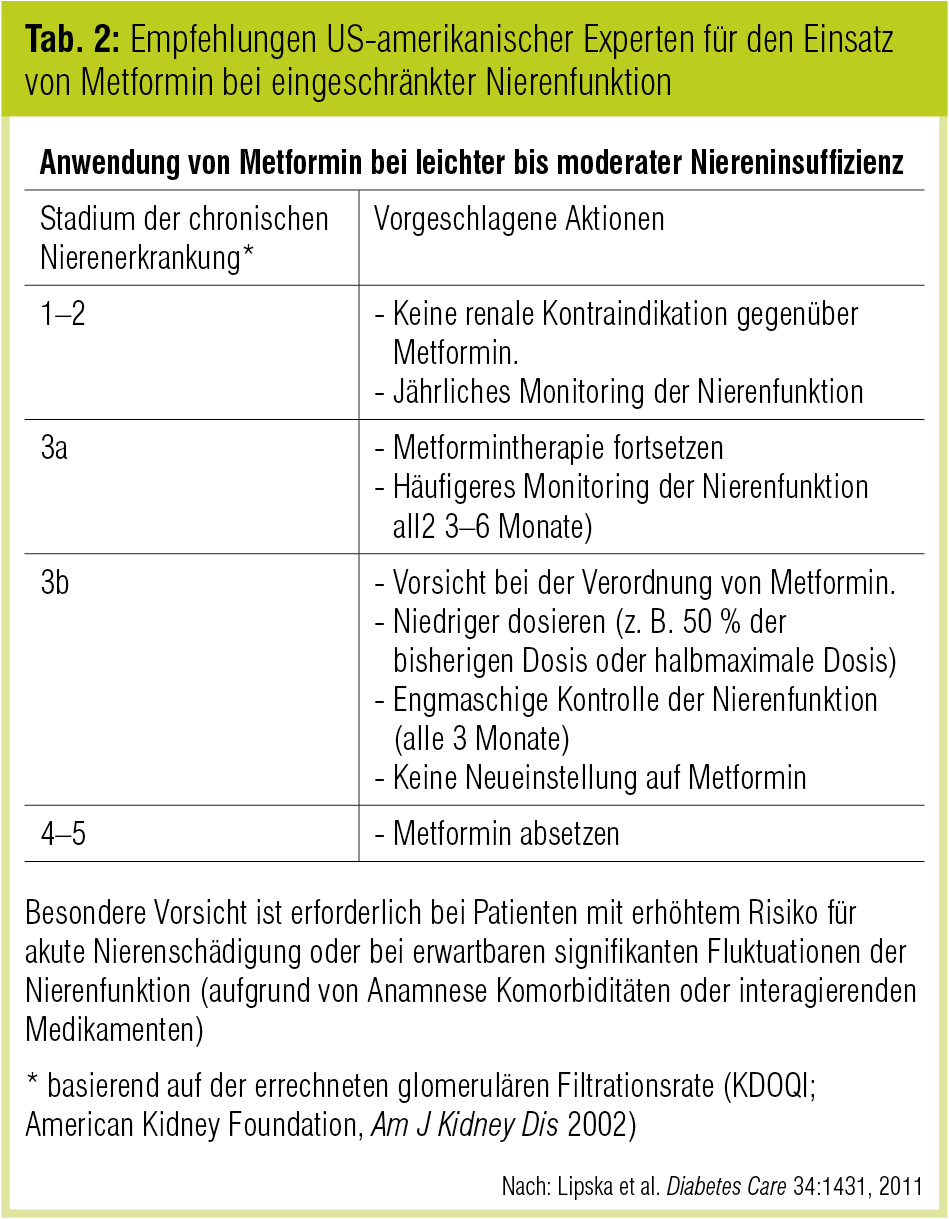
Noch einen Schritt weiter gehen Vertreter der American Diabetes Association, die im CKD-Stadium 3b (eGFR: 30–45 ml/min/1,73m2) zwar keine Neueinstellung auf Metformin empfehlen, aber die Fortführung der Metformintherapie in reduzierter Dosis und unter engmaschiger Kontrolle befürworten (Lipska et al., Diabetes Care 2011; Tab. 2).
Fazit: Vorsicht vor allem bei akuter Nierenfunktionsstörung
In der Zusammenschau dieser Überlegungen spricht Vieles dafür, dass nicht so sehr die chronische Nierenerkrankung (jedenfalls oberhalb einer glomerulären Filtrationsrate von 30 ml/min) als vielmehr die akute Verschlechterung der Filtrationsleistung das Risiko für MALA erhöht. In Anlehnung an die Empfehlungen der Kanadischen Gesellschaft für Nephrologie (Levin et al., CMAJ 2008) sollte die Metformintherapie daher immer dann ausgesetzt werden,
- wenn akute Veränderungen der Nierenfunktion sichtbar werden;
- in Situationen (z. B. gastrointestinale Störungen, Dehydratation, kardiale oder respiratorische Insuffizienz), die einen Abfall der Nierenfunktion oder Hypoxie begünstigen;
- bei Hypovolämie oder Schockzustand.
Besondere Vorsicht ist bei Patienten angebracht, die mit ACE-Hemmern, Angiotensinrezeptorblockern, NSAR oder Diuretika behandelt werden, sowie bei der Verabreichung von Kontrastmitteln ein akutes Nierenversagen erleiden können.
Die Patienten sind darüber aufzuklären, dass sie bei Dehydrierung infolge von Erbrechen oder Diarrhö die Metformintherapie zeitweilig unterbrechen und ärztliche Hilfe in Anspruch nehmen sollen. Und sie sollen darüber informiert werden, dass einige Medikamente wie Blutdrucksenker sowie Erkältungsmittel und Schmerzmittel aus der Gruppe der NSAR die Nierenfunktion kurzfristig verschlechtern können und bei gleichzeitiger Metformintherapie mit Vorsicht angewendet werden müssen.