NAFLD-Screening im klinischen Alltag – wen und wie?
Nichtalkoholische Fettlebererkrankung (NAFLD) ist ein Hauptgrund für chronisches Leberversagen, hepatozelluläres Karzinom sowie Lebertransplantation weltweit. Nichtalkoholische Steatohepatitis (NASH) und insbesondere der Grad der Fibrose haben eine große Bedeutung für die Langzeitprognose von NAFLD-Patienten. Daher ist es von besonderer Bedeutung, die Patienten mit einem erhöhten Risiko für NASH sowie fortgeschrittener Fibrose zu identifizieren. Insbesondere Leberbiopsie ist nach wie vor der Goldstandard der Diagnose. Allerdings ist sie aufgrund des nötigen invasiven Eingriffes, der hohen Kosten sowie der inter- und intraindividuellen Variabilität der Untersucher nicht praktikabel für das Screening auf breiter Ebene.
In der letzten Dekade wurden einige nichtinvasive Biomarker entwickelt und validiert. Viele Marker wurden untersucht, um die Wahrscheinlichkeit von NASH bei Patienten mit NAFLD vorherzusagen. Es handelt sich hierbei angefangen von klinischen Parametern (Alter, Geschlecht, Diabetesstatus, BMI, arterielle Hypertonie, Aminotransferasen, Bilirubin und Ferritin), metabolische Parametern (HbA1c, Insulin, HOMA-IR) und Lipiden (Triglyzeride, Cholesterin) bis hin zu Parametern, denen spezifische und komplexe molekulare Pathomechanismen der NAFLD zugrunde liegen, wie Inflammation, oxidativer Stress, Apoptose, Glukose- und Lipidmetabolismus.
Da die Pathogenese von NASH sehr komplex ist und wahrscheinlich durch multiple biologische Veränderungen entstehen kann, ist es unwahrscheinlich, dass ein einziger Biomarker oder ein einziger klinischer Parameter zwischen einer einfachen Steatose und einer NASH differenzieren kann. Daher beinhalten die meisten der folgenden nichtinvasiven Screeningmethoden zumindest zwei, aber meist mehrere Variablen, um robust sein zu können.
Screening im klinischen Alltag
Screening auf NAFLD sollte bei allen Hochrisikogruppen, also Patienten mit Typ-2-Diabetes, Adipositas oder einem metabolischen Syndrom, durchgeführt werden. Da nicht alle Patienten mit diesen Diagnosen eine Leberbiopsie erhalten können, müssen nichtinvasive, einfachere Screeningmethoden gefunden werden. Grundlage ist natürlich eine ausführliche Anamnese, in der vor allem ein alkoholischer Ursprung sowie andere sekundäre Ursachen einer Lebererkrankung (z. B. verschiedene Medikamente) ausgeschlossen werden sollten. Für ein generelles Screening Verwandter von Patienten mit NAFLD liegen derzeit nicht ausreichend Daten vor, auch wenn es zunehmend mehr Studien gibt, die über genetische Suszeptibilität berichten. Wenn Verwandte von NAFLD-Patienten allerdings auch Risikofaktoren für NAFLD haben, sollten sie auf jeden Fall gescreent werden.
Screeningmethoden – Möglichkeiten und Limitationen
Ein laborchemisches Screening mittels Bestimmung von Transaminasen ist nicht sinnvoll, da Patienten mit NAFLD überwiegend normwertige Transaminasen aufweisen. Allerdings wurden die Grenzwerte herabgesetzt (Frauen 19 U/l, Männer 30 U/l), sodass nun eine deutlich bessere Detektion möglich sein sollte.
Die Prävalenz der mittels Ultraschalls detektierten Steatose in der Allgemeinbevölkerung ist im Durchschnitt ca. 30 %, die Sensitivität des Ultraschalls für die Detektion einer Steatose ist mit ca. 60 % für ein Screeningverfahren jedoch relativ niedrig. Der Ultraschall ist und bleibt die Screeningmethode der ersten Wahl bei Patienten mit Verdacht auf NAFLD.
Eine genauere Quantifizierung des Fettgehaltes der Leber lässt sich natürlich durch ein MR der Leber bewerkstelligen. Allerdings kann und sollte dies aufgrund der hohen Kosten und der geringen Verfügbarkeit nicht routinemäßig zum Einsatz kommen.
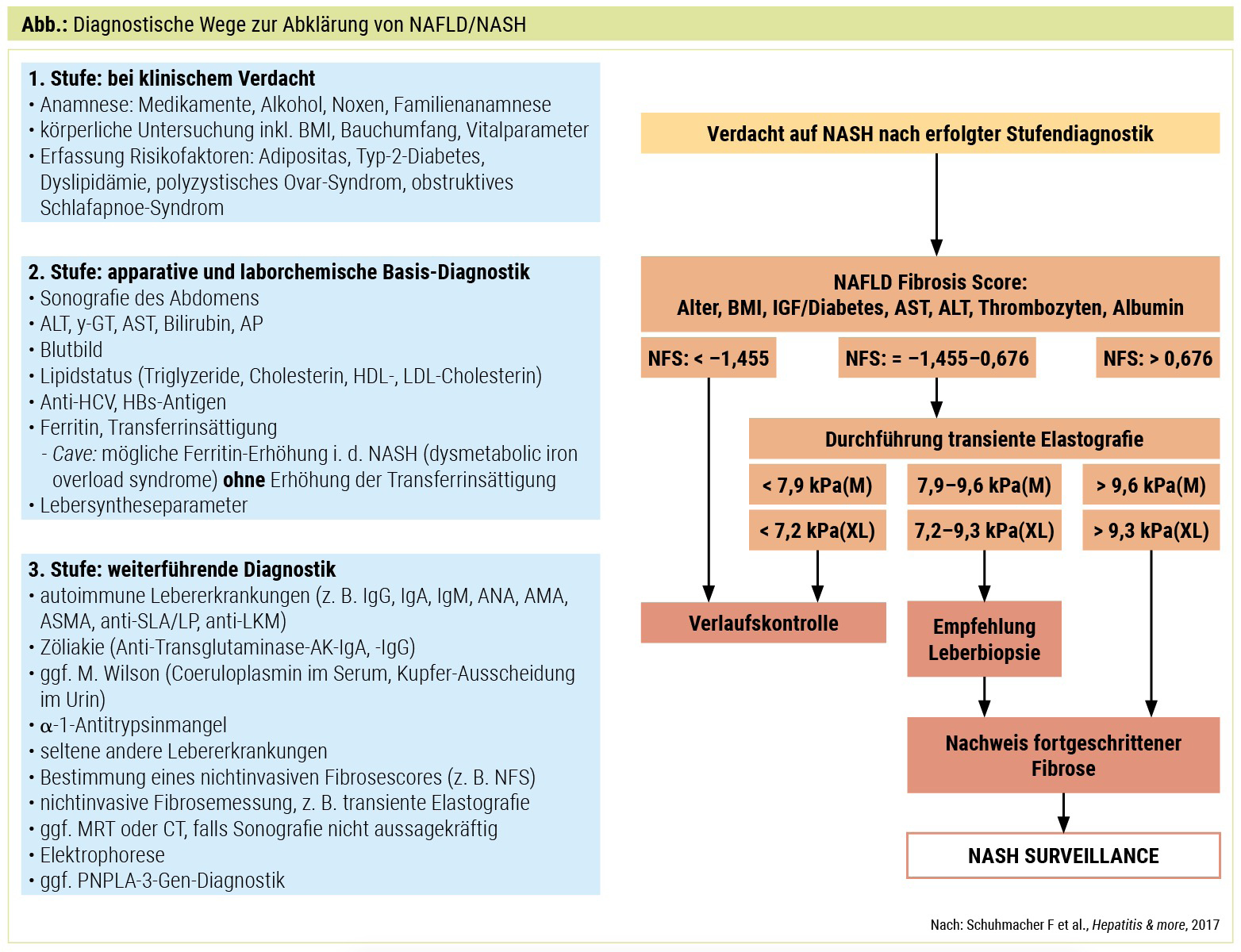
Im Jahre 2007 wurde durch die Arbeitsgruppe von Angulo et al. ein einfaches, nichtinvasives Verfahren zur Einschätzung einer Leberfibrose bei Patienten mit NAFLD vorgeschlagen. Dieser Score, der NAFLD Fibrose Score (NFS; http://nafldscore.com), setzt sich aus den Kenngrößen Alter, Hyperglykämie, Body Mass Index, Thrombozytenzahl und Albumin-Serumkonzentration sowie der AST/ALT-Ratio zusammen. Anhand des Scores lassen sich erstdiagnostizierte NAFLD-Patienten mit fortgeschrittener Leberfibrose klar von solchen ohne fortgeschrittener Fibrose unterscheiden. Im Algorithmus der deutschen Leitlinie wird auf Basis des NFS-Scores und einer Leberelastografie (FibroScan®) die Entscheidung zur Leberbiopsie getroffen (Abb.). Die europäische Leitlinie fasst die Indikation zur Leberbiopsie deutlich offener, denn zur definitiven Diagnosesicherung der NASH ist der histologische Nachweis einer Verfettung > 5 %, der Nachweis von Hepatozyten-Ballonierung („Ballooning“) und einer Entzündung in der Leberbiopsie erforderlich. Für die Erfassung dieser drei Kriterien gibt es keine Alternative zur Leberbiopsie.
Kombinierte Tests und Maker: Serummarker wie der FIB-4 oder die kommerziell erhältlichen ELF oder FibroTest können als Alternative zum NFS zum Ausschluss einer schon fortgeschrittenen Leberfibrose durchgeführt werden. FIB-4 ist ein kostenfreier, kalkulierbarer Score, bestehend aus Alter, Thrombozytenzahl, AST und ALT, mit einer diagnostischen Genauigkeit von 80 % für die Diagnose einer fortgeschrittenen Leberfibrose (http://gihep.com/calculators/hepatology/fibrosis-4-score).
Der ELF-Score ist hingegen ein kommerziell erhältlicher Marker für eine fortgeschrittene Fibrose, bestehend aus Hyaluronsäure, N-terminales Propeptid von Prokollagen III (PIIINP) und Gewebe-Metalloproteinase-1-Inhibitor (TIMP-1). Auch FibroTest ist ein kommerziell erhältlicher Fibrosemarker bestehend aus Bilirubin, γ-GT, Alpha-2-Makroglobulin, Apoprotein A1 und Haptoglobin, welcher zunächst für die virale Hepatitis entwickelt wurde, aber inzwischen auch für die NAFLD evaluiert ist.
Vielversprechende Biomarkerund andere nichtinvasive Methoden
Bei den Biomarkern sticht Keratin 18 (K18) hervor. Dies ist ein Filamentprotein in Hepatozyten und ein wichtiges Substrat der Caspase-3-Spaltung, welches im Serum mittels Immunoassays gemessen werden kann. Höhere Konzentration von K18 wurden bei Patienten mit NASH verglichen zu Patienten mit normaler Steatose gefunden. Daten von zwei Metaanalysen geben eine Sensitivität von 66–78 % und eine Spezifität von 82–87 % an, um mittels K18 eine NASH zu detektieren. Aber auch bei K18 scheint die Kombination mit den bereits genannten klinischen Kriterien eine höhere Detektionsrate zu ergeben.
Adipozytokine sind stark in die Pathogenese der NAFLD involviert, sodass auch in diesem Bereich viele Untersuchungen stattfinden, ob einer oder mehrere davon Prädiktoren für eine NASH sein könnten. Den besten Vorhersagewert hat derzeit eine Kombination aus Adiponectin, Leptin und Ghrelin zur Unterscheidung von NASH und einer simplen Steatose.
Eine weitere neue Strategie zur Differenzierung zwischen NAFLD und NASH konzentriert sich auf die Verwendung von „Omics“. „Omics“-Untersuchungen liefern eine Reihe von Molekülen, die mit der Erkrankung assoziiert sind, welche aber erst weiter untersucht und validiert werden müssen, bevor ein Einsatz im klinischen Alltag denkbar wäre.
Controlled-Attenuation-Parameter (CAP) ist eine neue, nichtinvasive Methode, welche in den FibroScan® integriert ist und während der transienten Elastografiemessung durchgeführt werden kann. CAP misst die dorsale Schallabschwächung/-dämpfung quantitativ in dB/m. In einer Metaanalyse von 7 Studien mit 9 Kohorten und insgesamt 1.471 Patienten betrugen die mittleren Sensitivitäten und Spezifitäten 73 % und 81 % für die Diagnose einer Steatose ≥ Grad 1 (11–33 %), 82 % und 79 % für ≥ Grad 2 (34–66 %) und 82 % und 80 % für ≥ Grad 3 (67–100 %).
Die Magnetresonanz-Spektroskopie (MRS) hat in der Literatur die höchste Genauigkeit für die Fettbeurteilung, ist jedoch gegenwärtig aufgrund noch fehlender Vereinheitlichung der Methodik und hohen Anforderungen an Hard- und Software auf Forschungszentren begrenzt.
Resümee
Zusammenfassend ist sicher wichtig, an die Möglichkeit einer NAFLD zu denken, vor allem in Hochrisikokohorten. Bei diesen ist ein Screening auch indiziert. Die Transaminasen sind oft falsch negativ und können daher nur eingeschränkt verwendet werden, allerdings ist durch die Senkung der Grenzwerte nun eine bessere Assoziation mit NASH möglich. Der Ultraschall ist nach wie vor die primäre Bildgebung, dieser sollte aber nach Durchführung des NFS-Scores durch eine Elastografie oder einen FibroScan® ergänzt werden. Auch der FIB-4-Score kann herangezogen werden. Erst danach entscheidet sich, ob eine Indikation für eine Leberbiopsie gestellt wird, welche allerdings nach wie vor der Goldstandard in der Diagnosesicherung ist.
– Vilar-Gomez E et al., Non-invasive assessment of non-alcoholic fatty liver disease: Clinical prediction rules and blood-based biomarkers. J Hepatol 2018; 68: 305–15
– Pimpin L et al., Burden of liver disease in Europe: Epidemiology and analysis of risk factors to identify prevention policies. J Hepatol 2018; 69: 718–35
– Roeb E et al., S2k-Leitlinie nichtalkoholische Fettlebererkrankungen AWMF Register Nr. 021-025 Version Januar 2015, Erstauflage