Übergewicht und Adipositas: Physiologie und Pathophysiologie der Appetitregulation
Das Körpergewicht wird durch eine konzertierte Regulation der Energiezufuhr und des Energieverbrauchs bestimmt. Dabei setzen kleinste Abweichungen des Körpergewichts (unter 1 %) entgegengesetzte Mechanismen in Gang, um das Körpergewicht auf dem vorgegebenen Niveau zu halten. Dies erklärt auch die Schwierigkeiten, dauerhaft Gewicht abzunehmen. Zu berücksichtigen ist weiters, dass aber schon geringste Abweichungen der Energiezufuhr, wenn sie konsequent beibehalten werden, langfristig zu bedeutenden Veränderungen des Körpergewichts führen. Eine positive Energiebilanz von nur 25 kcal/Tag, das entspricht 35 ml Vollmilch, 3 g Butter oder 10 g einer Semmel, hat im Laufe eines Jahres eine Gewichtszunahme von einem Kilogramm (1 kg Fett = 9.000 kcal) zur Folge. Dies ist insbesondere vor dem Hintergrund interessant, dass ein junger Mensch mit mäßiger körperlicher Aktivität pro Jahr etwa eine Million Kilokalorien mit der Nahrung zu sich nimmt.
Hypothalamus als Zentrale der Appetitregulation
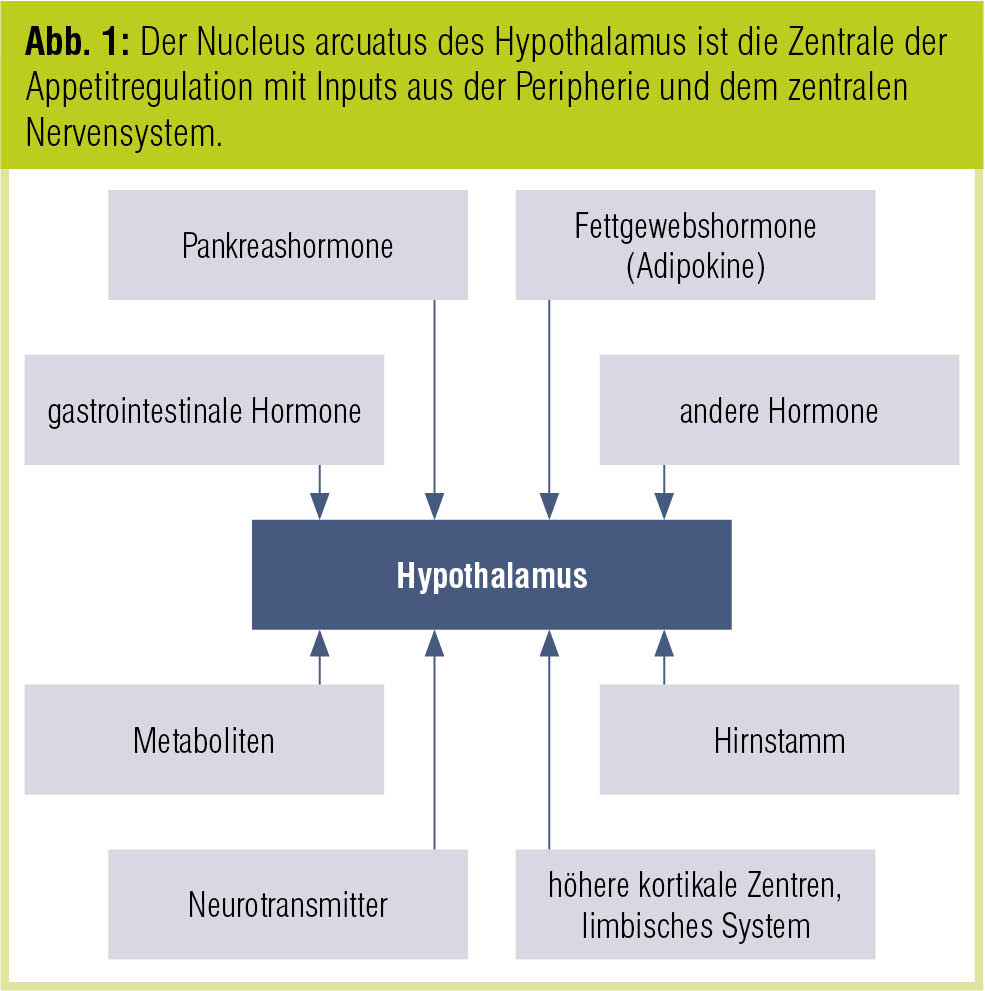
Als zentrale Stelle der Appetitregulation fungiert der Nucleus arcuatus des Hypothalamus, in dem einerseits über Neuropeptid Y/Agouti-related peptide (NPY/AgRP) der Appetit und damit die Nahrungsaufnahme angeregt werden, und andererseits über Proopiomelanocortin/Cocaine and Amphetamine Related Transcript (POMC/CART) Sättigung vermittelt und damit die Nahrungsaufnahme gedrosselt wird (Stanley et al., Physiol Rev 2005). Gleichzeitig wird über diese zentrale Schaltstelle auch der Energieverbrauch (= Energieausfuhr = körperliche Aktivität) geregelt. Der Nucleus arcuatus erhält dabei sowohl Signale aus dem zentralen Nervensystem als auch aus der Peripherie (Abb. 1). Dabei spielen zum einen Hormone aus dem Gastrointestinaltrakt, dem Fettgewebe und dem Pankreas eine Rolle, aber auch Metaboliten und Neurotransmitter sowie das vegetative Nervensystem, der Hirnstamm, höhere kortikale Zentren und das limbische System.
Appetitregulierende Hormone
Die vorliegende Zusammenstellung bezieht sich im Wesentlichen auf Hormone bzw. Peptide aus dem Magen-Darm-Trakt, dem Pankreas und dem Fettgewebe. Der Schwerpunkt wird dabei auf Ghrelin gelegt, das als orexigenes (appetitanregendes) Peptid einer Armada von anorexigen wirkenden gegenübersteht (Abb. 2). Anzumerken ist dabei, dass Hormone aus der Peripherie über die Eminentia mediana im Bereich des Hypothalamus und die Area postrema im Hirnstamm, beides Gebiete mit durchlässiger Blut-Hirn-Schranke, das zentrale Nervensystem erreichen können.
Ghrelin. Wenngleich Ghrelin erst vor 15 Jahren als lange Zeit unbekannter Ligand des neben dem Growth-Hormone-Releasing-Hormone-Rezeptor (GHRH-R) zweiten Rezeptors der somatotropen Zellen, der Somatotropinfreisetzung induziert, identifiziert worden ist, hat sich sehr bald in klinischen Studien sein orexigener Effekt gezeigt. Daneben sind stimulierende Wirkungen auf die Sekretion von adrenokortikotropem Hormon (ACTH), Prolaktin und Arginin-Vasopressin (AVP) sowie die Hemmung der Gonadotropinsekretion ebenso wie die Steigerung der Motilität des Gastrointestinaltraktes und seine positiv inotrope Wirkung gezeigt worden (van der Lely et al., Endocr Rev 2004).
Ghrelin-Konzentrationen im Plasma sind unmittelbar vor dem Essen am höchsten und sinken nach Nahrungsaufnahme innerhalb von 15–30 Minuten ab. Glukose scheint in diese Regulation nicht eingebunden zu sein und Insulin nur in hohen Konzentrationen (Schaller et al., Diabetes 2003). Des Weiteren spielt das cholinerge System eine wesentliche Rolle und die Regulation scheint bei adipösen Personen gestört zu sein (Maier et al., J Clin Endocrinol Metab 2004; Maier et al., Diabetes 2008; Maier et al., J Clin Endocrinol Metab 2010). Wir konnten auch zeigen, dass Ghrelin nach bariatrischen Eingriffen bei Sleeve-Gastrektomie wesentlich anhaltender reduziert wird als nach „gastric banding“, was einen Beitrag zur anhaltenderen Gewichtsreduktion nach Sleeve-Gastrektomie liefern könnte (Langer et al., Obes Surg 2005).
Eine interessante Verbindung zwischen Herz und Gehirn haben wir vor Kurzem beschrieben: Brain Natriuretic Peptide (BNP) hemmt das orexigene Ghrelin und könnte so zur Kachexie bei Patienten mit schwerer Herzinsuffizienz beitragen (Vila et al., Diabetes 2012). Ghrelin-Agonisten und Ghrelin-Antagonisten sind damit interessante Therapieoptionen bei Kachexie (auch Tumorkachexie) bzw. Adipositas.
Peptid YY, Cholezystokinin, GLP-1, Oxyntomodulin. Im Gegensatz zu Ghrelin hemmen Peptid YY und Cholezystokinin, deren Freisetzung ebenfalls nach Nahrungsaufnahme stimuliert wird, den Appetit (Maier et al., Diabetes 2008). Dies gilt auch für die beiden aus Proglukagon stammenden Peptide Glucagon-like peptide 1 (GLP 1) und Oxyntomodulin.
Leptin. Das vom Fettgewebe sezernierte, vor nunmehr nahezu 20 Jahren identifizierte Leptin (Zhang et al., Nature 1994) stimuliert die Expression von POMC im Nucleus arcuatus und hemmt die orexigenen Pathways (NPY/AgRP). Im Gegensatz zu Ghrelin wird es nicht essensabhängig, sondern kontinuierlich freigesetzt. Die ursprünglich in Leptin gesetzten Erwartungen bei der Behandlung von Adipositas haben sich mit Ausnahme der Wirkung bei den wenigen auf der Welt bekannten leptindefizienten Patienten, die jede Art von Essen schätzen, Unmengen davon unkontrolliert zu sich nehmen und schon im frühen Kindesalter eine massive Adipositas entwickeln, leider nicht bestätigt. Leptingabe führt nur bei leptindefizienten Kindern, wie zuvor bei den leptindefizienten Mäusen bereits gezeigt wurde, zu einer drastischen Reduktion der Kalorienaufnahme und damit des Körpergewichts (Farooqi et al., N Engl J Med 1999).
Im Gegensatz zu der ursprünglichen Annahme weisen adipöse Personen nicht niedrige, sondern hohe Leptin-Plasmakonzentrationen und somit eine Leptinresistenz auf. Diese kann auch durch Verabreichung hoher Leptindosen nur gering beeinflusst werden. Allerdings wird zurzeit eine mögliche Anwendung von Leptin bei Diabetes untersucht (Cummings, Diabetes Obes Metab 2012). Darüber hinaus stimuliert Leptin das Immunsystem und ist für eine normale Funktion der Hypothalamus-Hypophysen-Gonaden-Achse von Bedeutung (Mantzoros et al., Am J Physiol Endocrinol Metab 2011). Die mit Anorexie einhergehende Amenorrhö scheint durch niedrige Leptinkonzentrationen (bedingt durch eine niedrige Fettmasse) verursacht zu sein.
Andere Hormone. Es ist auch bekannt, dass Trijodthyronin (T3) neben einer Steigerung der metabolischen Rate und Thermogenese den Appetit und damit die Nahrungsaufnahme stimuliert, insgesamt jedoch eine negative Energiebilanz begünstigt. Östrogene führen zu Anorexie und Abnahme der Fettmasse, was die Zunahme der zentralen Fettspeicherung in der Menopause erklärt, die durch Hormonersatztherapie reversibel ist. Auch Kortisol wirkt appetitanregend.
Resümee
Der Hypothalamus (Nucleus arcuatus) ist die zentrale Stelle der Appetitregulation. In ihm werden unzählige Signale aus der Peripherie und dem Zentralen Nervensystem verarbeitet und dadurch die Energiezufuhr (Nahrungsaufnahme) und Energieausfuhr (körperliche Aktivität) geregelt. Schon kleinste Veränderungen an einem der beiden Schenkel bewirken das Ingangsetzen von entgegengesetzten Regulationsmechanismen, die danach trachten, das Körpergewicht auf dem vorgegebenen Niveau zu halten.