Künstliche Intelligenz in der Uroradiologie
Zuletzt sind die Anwendungen der künstlichen Intelligenz (KI) ein wesentlicher Bestandteil der Diskussion in den Medien gewesen, wie es beispielsweise am Programm ChatGPT zu sehen war. Bedingt durch die in den letzten Jahren gestiegenen Rechenkapazitäten sowie maßgeblichen Fortschritte im Bereich der Programmierung konnten in einigen Teilbereichen der Medizin erste KI-Anwendungen im Rahmen von Forschungsprojekten sowie als klinisch anwendbare Assistenzsysteme verwendet werden.1,2 Mit Hilfe von künstlicher Intelligenz lassen sich kognitive menschliche Teilaufgaben durch gezielte Rechenprogramme ersetzen.Hierzu werden üblicherweise Techniken wie das so genannte Machine Learning bzw. Deep Learning verwendet. Beides sind unterschiedliche technische Ansätze, die das Ziel haben, aus vorhandenen Daten bestimmte Muster zu erkennen, aus den Daten zu lernen und hierauf basierend Entscheidungen zu treffen. Das Machine Learning verwendet einen Algorithmus zur Datenanalyse, lernt aus den Daten und trifft basierend hierauf Entscheidungen.3 Bei Deep Learning werden künstliche neuronale Netzwerke (englisch Artificial neuronal Network) verwendet, wobei das System selbstständig dazulernt und den jeweiligen Ebenen (Layer) Algorithmen zuweist (Abb.). Hierbei werden mehrere Ebenen hintereinander bzw. parallel verwendet, um verschiedene Aspekte eines Bildes zu analysieren (beispielsweise eine Ebene zur Identifikation der Form, eine Ebene für Grauwerte usw.).4
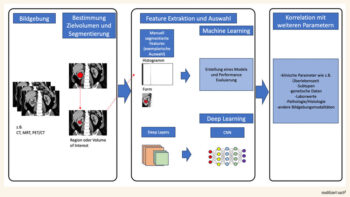
Abb.: Beispielhafte Darstellung eines Arbeitsablaufes bei der Bilddaten-Analyse mit Machine Learning und Deep Learning
Blickpunkt Uro(onko)logie
Mit Bezug auf den Fachbereich der Urologie ergeben sich verschiedene Teilbereiche, die prädestiniert für KI-Anwendungen wie beispielsweise uroonkologische Erkrankungen und die Klassifizierung von Nierensteinen sind. Im Rahmen dieses Artikels sollen insbesondere die Applikationsmöglichkeiten in der uroonkologischen Bildgebung eingehender betrachtet werden. Die hierbei von verschiedenen Arbeitsgruppen genauer untersuchten Tumorentitäten sind unter anderem das Prostatakarzinom sowie das Nierenzellkarzinom.
Prostatakarzinom
KI-Anwendungen mit Bezug zum Prostatakarzinom umfassen solche, welche die Diagnostik und die Detektion von Rezidiven adressieren,sowie auch jene, die das Therapieansprechen und das Gesamtüberleben vorhersagen. Beispielhaft sollen einzelne ausgewählte Anwendungsbeispiele aufgeführt werden.
Die Diagnosestellung anhand einer multiparametrischen MRT kann im Einzelfall schwierig sein und stellt insbesondere für unerfahrene Radiolog:innen eine Herausforderung dar. In einer retrospektiven, Multi-Reader-, Multi-Case-Studie wurden insgesamt 184 Patienten mit einer multiparametrischen MRT eingeschlossen und unerfahrene und erfahrene Radiolog:innen gebeten, einmal mit und einmal ohne Zuhilfenahme einer Deep-Learning-KI eine Diagnose zu stellen.5 Bei den Patienten lagen zudem Ergebnisse einer transrektalen ultraschallgesteuerten Biopsie vor. Bei den unerfahrenen Radiolog:innen stieg die diagnostische Performance – hier ausgedrückt als Area under the Curve (AUC) – von 0,66 bzw. 0,68 auf 0,80 und bei den erfahrenen Radiolog:innen von 0,81 auf 0,84 bzw. 0,865. In einer weiteren Studie konnte durch KI-unterstütze Abläufe die Genauigkeit der Befundung mittels PI-RADS (Prostate Imaging-Reporting and Data System) von 84% auf 88% verbessert und eine Inter-Reader-Variabilität reduziert werden.6
Nierenzellkarzinom
Die bildmorphologische Differenzierung von Nierenzellkarzinomen, fettarmen Angiomyolipomen und Onkozytomen kann im klinischen Alltag auf Grund von überlappenden Bildgebungseigenschaften eine besondere Herausforderung darstellen.7 Mit Hilfe von KI sind zusätzliche Informationen, die in den Bildgebungsdaten enthalten sind, evaluierbar und können dazu verwendet werden, die Diagnostik zu verbessern und benigne von malignen Tumoren zu unterscheiden.8 Basierend auf Daten von 20.000 CT- Bilddatensätzen konstruierten Pedersen et al. ein neuronales Netzwerk, das eine Unterscheidung von Onkozytomen und Nierenzellkarzinomen mit einer Genauigkeit von 93,3% und einer Spezifität von 93,5% erreichte.9 Baghdadi et al. berichten in einer kleinen Kohorte von 20 Patient:innen, dass eine KI-basierte Software unter anderem anhand der Eigenschaften des Kontrastmittels Onkozytome von chromophoben Nierenzellkarzinomen mit einer Sensitivität von 100% und eine Spezifität von 89% unterscheiden kann.10 In einer Studie mit CT von 41 fettarmen Angiomyolipomen und 130 Nierenzellkarzinomen war ein texturbasierter Machine-Learning-Algorithmus besser als Radiolog:innen in der Differenzierung von fettarmen Angiomyolipomen, Nierenzellkarzinomen, klarzelligen Nierenzellkarzinomen und nichtklarzelligen Nierenzellkarzinomen mit AUC von 0,96, 0,97 und 0,89 vs. 0,67, 0,68, und 0,64.11 Insgesamt müssen die Ergebnisse der KI in Bezug auf Nierenzellkarzinome jedoch aufgrund der teils kleinen Kohorten mit Vorsicht betrachtet werden und können eine sichere Diagnosestellung, wie sie mittels Histopathologie erreicht werden kann, derzeit nicht ersetzen.
Ausblick
Die vielversprechenden Ergebnisse aus einzelnen Studien lassen das Potenzial von KI-Anwendungen in der urologischen Bildgebung erahnen und könnten eine zusätzliche Hilfestellung bei der radiologischen Bildinterpretation und der automatisierten Befunderstellung darstellen. Es sind weitere größere randomisierte Studien wünschenswert, um in diesem Bereich auch Limitationen von KI genauer zu bestimmen. So wird KI hier perspektivisch die Radiolog:innen nicht ersetzen, sondern eher als Co-Pilot für den Radiolog:innen und Urolog:innen eingesetzt werden.12 In der Zukunft erscheint ein Einsatz von KI zum Beispiel bei Fusionsbiopsien oder fokalen Therapien für Prostatakarzinompatienten vielversprechend.13 Die direkte Integration in bestehende Hardware könnte so zu einer Verbesserung der medizinischen Versorgung durch genauere Lokalisierung von Tumorgrenzen führen und vor allem die Lernkurve von unerfahreneren Urolog:innen bei Biopsie oder fokaler Therapie verbessern.























































































