COVID-Impfung bei rheumatischen Erkrankungen
Im Dezember 2019 trat erstmals das „neue“ Coronavirus SARS-CoV-2 als Erreger der in Folge pandemisch gewordenen COVID-19-Erkrankung auf. Das Krankheitsbild von COVID-19 und die Risikofaktoren für einen schwereren Verlauf sind mittlerweile gut bekannt. Zu Beginn der Pandemie waren Patient*innen mit entzündlich rheumatischen Erkrankungen in mehrfacher Hinsicht verunsichert. Einerseits wurden essenzielle „Rheuma“-Medikamente wie z. B. Hydroxychloroquin und Tocilizumab als potenzielle COVID-19-Therapeutika in Beschlag genommen und waren in der Folge für ihre ursprünglichen Indikationen schwer verfügbar. Andererseits war eine erhöhte Anfälligkeit für die SARS-CoV-2-Infektion ebenso wie auch eine für schwerere Verläufe unter einer bestehenden immunsuppressiven Therapie gefürchtet. Letzteres konnte für die Patient*innen-Population mit rheumatischen Erkrankungen nicht bestätigt werden. Es dominieren auch hier Faktoren wie höheres Alter, männliches Geschlecht und Komorbiditäten wie schlecht eingestellter Hypertonus, Diabetes, schwere Herz-Kreislauf- und Lungenvorerkrankungen das Risiko für Hospitalisierung, Notwendigkeit einer intensivmedizinischen Betreuung und Versterben durch COVID-19. Insbesondere wurde offensichtlich, dass die immunsuppressiven und immunmodulierenden Therapien mit Ausnahme einer bestehenden Kortison-Therapie (> 10 mg Aprednislon-Äquivalent/Tag) keinen negativen Einfluss auf die Infektion und ihren Verlauf zeigten und somit eindringlich von selbständigem Absetzen oder Pausieren der bestehenden Therapie mit DMARDs jeglicher Substanzklasse abgeraten wurde. Für einzelne Biologika-Klassen wie z. B. die TNF-α-Blocker waren in einigen Untersuchungen sogar benefizielle Trends bei COVID-19 zu verzeichnen. Interessanterweise sind es gerade diese klassischen „Rheuma“-Medikamente, die nach wie vor für die Therapie der Hyperinflammation im Rahmen der COVID-19-Erkrankung untersucht werden.
Aus therapeutischer Sicht ist auch nach einem Jahr Pandemie das Armamentarium trotzdem überaus bescheiden. Lediglich die Gabe von Dexamethason bei schwereren Verläufen konnte sich bis jetzt als Standardtherapie etablieren. Dementsprechend liegen alle Hoffnungen auf präventiven Maßnahmen. Diese sind zum einen nichtpharmakologisch wie das Tragen von Masken, die Reduktion sozialer Kontakte bzw. das Einhalten von Distanzregeln, zum andern wurden in sehr kurzer Zeit Impfstoffe entwickelt, die sich bereits in breiter Anwendung befinden.
Impfstoffe in Österreich
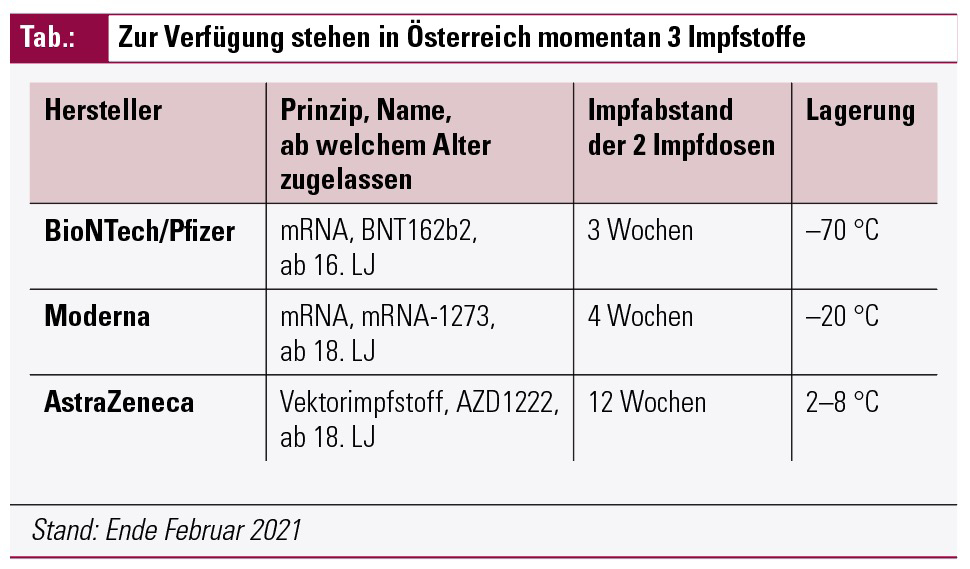
In Österreich stehen derzeit – mit Stand Ende Februar 2021 – drei Impfstoffe zur Verfügung (Tab.).
Alle drei Impfstoffe werden als Totimpfstoffe angesehen und für Patient*innen mit entzündlich rheumatischen Erkrankungen unter immunsuppressiver/immunmodulierender Therapie jedenfalls empfohlen, wobei für sogenannte Hochrisikopatient*innen die mRNA-Impfstoffe zu bevorzugen sind. Daten zur Effektivität und zur Sicherheit der Impfungen liegen allerdings für alle 3 Impfstoffe noch nicht in ausreichendem Maße vor. Somit können auch die sonst verbreitet diskutierten Unterschiede im Impfansprechen zwischen den mRNA-Impfstoffen und dem Vektorimpfstoff nicht auf das rheumatische Patient*innen-Kollektiv übertragen werden.
Die initiale Beschränkung der Impfempfehlung des nationalen Impfgremiums für die Vektorimpfung von AstraZeneca auf Unter-65-Jährige wurde nach Vorliegen von aktuellen Daten besonders aus England aufgehoben, womit alle verfügbaren Impfstoffe nunmehr auch in höherem Alter einsetzbar sind. Bei fehlenden Informationen zur Wirksamkeit der COVID-19-Impfungen bei Immunsuppression/Immunmodulation erscheint eine „Titer“-Kontrolle nach erfolgter Impfung sinnvoll, wobei hier einschränkend das Korrelat der Protektion erst einmal definiert werden muss. Eine COVID-19-Antikörper-Bestimmung im Vorfeld der Impfung ist allerdings nicht notwendig, da unabhängig vom Vorliegen eines etwaigen positiven Antikörper-Nachweises eine Impfung erfolgen sollte.
Zeitpunkt der COVID-19-Impfung
Zum Zeitpunkt der COVID-19-Impfung sollten die Patient*innen eine möglichst geringe Krankheitsaktivität aufweisen. Idealerweise sollte die Impfung 2 Wochen vor dem Therapie-Start mit einer immunsuppressiven/immunmodulierenden Therapie abgeschlossen sein. Ein Absetzen oder Pausieren der bestehenden immunsuppressiven/immunmodulierenden Therapie ist nicht notwendig bzw. wird sogar dezidiert davon abgeraten, da dies ein Risiko für die Reaktivierung der entzündlich rheumatischen Erkrankung darstellt. Für alle verfügbaren Impfungen gilt, dass es bis dato keine Hinweise gibt, dass es zu einer Verschlechterung der entzündlich rheumatischen Grunderkrankung kommt. Hier ist aber – ähnlich wie beim Impfansprechen – ein entsprechendes Monitoring angezeigt.
Um ein optimales Ansprechen der Impfung zu erreichen, sollte in der Mitte des Therapieintervalls geimpft werden. Analog zur Influenza-Impfung kann ein zweimaliges Aussetzen der Methotrexat-Gabe nach der Impfung diskutiert werden. Zusätzlich sollte ein Abstand von 2 Wochen zur Applikation von anderen Totimpfstoffen (z. B. FSME) bzw. 4 Wochen zur Gabe von Lebendimpfstoffen (z. B. MMR) eingehalten werden. Bei ehemals an COVID-19 erkrankten Patient*innen wird von der deutschen ständigen Impfkommission (STIKO) ein Abstand von ca. 6 Monaten zur Impfung empfohlen, wobei es hier erste Hinweise gibt, dass lediglich eine Impfung zur Auffrischung der Immunantwort ausreichen könnte, was bei Impfstoffknappheit und auch hinsichtlich des Nebenwirkungsprofils einen Vorteil bedeutet.
Spezialfall B-Zell-Depletion (z. B. mit Rituximab, RTX)
Patient*innen unter B-Zell-depletierender Therapie weisen ein erhöhtes Risiko für eine Viruspersistenz mit verlängerter Infektiosität sowie einen prolongierten und unter Umständen undulierenden Verlauf einer COVID-19-Erkrankung auf.
Idealerweise sollen alle Patient*innen vor Beginn einer B-Zell-depletierenden Therapie geimpft werden, hier jedenfalls mit einem mRNA-Impfstoff. Die Wirksamkeit der Impfung unter der B-Zell-depletierenden Therapie kann beeinträchtigt sein, wobei hier besonders der Zeitpunkt der letzten Gabe von Bedeutung ist. Der Impfzeitpunkt sollte in enger Absprache mit dem betreuenden Arzt/der betreuenden Ärztin terminisiert werden. Im Falle von RTX wohl ca. 4,5 Monate nach der letzten Gabe, um spätestens 2 Wochen vor der neuerlichen RTX-Administration die Impfung abgeschlossen zu haben. Allein aufgrund des langen Impfintervalls von 3 Monaten beim Vektorimpfstoff von AstraZeneca sind hier ausschließlich mRNA-Impfstoffe sinnvoll. Das Impfansprechen bzw. die Impftauglichkeit anhand der Quantität der in der Lymphozyten-Typisierung vorhandenen B-Zellen zu beurteilen erscheint einerseits aufwendig und daher unpraktikabel, andererseits wird die (eventuell auch wichtige) zelluläre Immunantwort damit völlig ausgeblendet.
Nebenwirkungen der COVID-19-Impfung
Sowohl bei den mRNA-Impfstoffen als auch beim Vektorimpfstoff können lokale (Rötung, Schwellung, Schmerzen) und systemische Nebenwirkungen (Fieber, Schüttelfrost, Kopfschmerzen, Müdigkeit, Muskel-/Glieder-/Gelenkschmerzen …) auftreten. Diese Nebenwirkungen sind beim Vektorimpfstoff häufiger nach der ersten Impfung, bei den mRNA-Impfungen nach der zweiten Gabe zu verzeichnen. Die Schwere der Nebenwirkungen ist altersabhängig, d. h., jüngere Geimpfte sind stärker davon betroffen. Soweit bekannt, gibt es für Patient*innen mit entzündlich rheumatischen Erkrankungen kein erhöhtes Risiko für unerwünschte Nebenwirkungen der Impfung. Auch gibt es zum jetzigen Zeitpunkt keine Hinweise für ein vermehrtes Auftreten von autoimmunen/autoinflammatorischen Erkrankungen im Anschluss an die Impfung. Anaphylaktische Reaktionen treten nach US-amerikanischen Erhebungen in etwa bei 4,7 Fällen/1 Mio. Impfungen mit BioNTech/Pfizer und 2,5 Fällen/1 Mio. Impfungen mit Moderna auf (bei > 17 Mio. Geimpften). Die anaphylaktischen Reaktionen traten im Median 10 Minuten nach Verabreichung auf und sprachen sehr gut auf Epinephrin-Gabe
an. Todesfälle waren nicht zu verzeichnen.
Welche Patient*innen mit einer entzündlich rheumatischen Erkrankung sollten nicht geimpft werden?
Wie bereits zuvor erwähnt, sollten Patient*innen mit entzündlich rheumatischen Erkrankungen bei möglichst geringer Krankheitsaktivität geimpft werden. Das heißt, ein etwaiger Schub der Grunderkrankung sollte zuerst unter Kontrolle gebracht werden.
Eine klassische Kontraindikation ist eine schwere allergische Impfreaktion in der Vorgeschichte sowie Allergien gegen Impfinhaltsstoffe.
Impfung in der Schwangerschaft, Stillzeit und bei Kinderwunsch
Keine Impfung ist in der Schwangerschaft oder Stillzeit zugelassen, somit kann es hier lediglich eine strenge Nutzen-Risiko-Abwägung in Rücksprache mit dem betreuenden Arzt/der betreuenden Ärztin geben. Patientinnen mit entzündlich rheumatischen Erkrankungen und immunsuppressiver/immunmodulierender Therapie und aktuellem Kinderwunsch wird die SARS-CoV-2-Impfung jedenfalls empfohlen. Gerüchte über eine Beeinflussung der Fruchtbarkeit durch eine COVID-19-Impfung entbehren jeglicher Grundlage.
Resümee
Alle bis dato vorliegenden Daten zur COVID-19-Impfung zeigen eine hohe Schutzrate sowohl für das geimpfte Individuum als auch für die Gemeinschaft. Die derzeit verfügbaren Impfstoffe scheinen nicht nur effektiv zu sein, sondern weisen auch ein hohes Sicherheitsprofil auf. Obwohl diesbezüglich Daten bei Patient*innen mit entzündlich rheumatischen Erkrankungen noch weitgehend fehlen, ist die COVID-19-Impfung gerade in dieser verletzlichen Population dringend zu empfehlen. Inwieweit nach einer Grundimmunisierung auf die vermehrt zirkulierenden Virusvarianten durch flexibleren Einsatz der Impfstoffe reagiert werden muss, wird sich wie viele andere offene Fragen in naher Zukunft weisen.