Neues zur Polyarthritis vom EULAR 2012 in Berlin
Biologikatherapie
Bereits die Zulassungsstudien für TNF-Hemmer zeigten, dass TNF-Inhibitoren in Kombination mit MTX eine überlegene Wirksamkeit gegenüber Monotherapien aufweisen.1 Außerdem deuten die meisten Daten darauf hin, dass eine TNF-Monotherapie keine bessere Wirkung als eine MTX-Monotherapie hat. Die klassischen Basismedikamente (als Standardtherapie MTX) stellen also eine etablierte und wirksame Therapieoption dar. Aus unterschiedlichen Gründen wie Unverträglichkeit, mangelnder Information und schlechter Adhärenz ist allerdings die Kombinationstherapie von DMARD und TNF-Blockern nicht immer möglich. Die bisherige Datenlage belegt, dass 20–60 % der RA-Patienten eine Biologikatherapie ohne begleitende DMARD erhalten.
Tocilizumab-Monotherapie
ACT-RAY-Studie. Bei diesem EULAR-Kongress wurde die Studie ACT-RAY (Phase IIIb) präsentiert, in der die Wirksamkeit der Tocilizumab-Monotherapie (TCZ) gegenüber der Kombinationstherapie mit MTX verglichen wurde.2 In diese Studie wurden Patienten mit aktiver RA (DAS28 > 4,4) eingeschlossen, die davor ungenügend auf die MTX-Monotherapie angesprochen hatten. Sowohl bei primären Endpunkten (Remissionsrate nach DAS28) als auch bei sekundären fanden sich keine signifikanten Unterschiede. Das bedeutet für RA-Patienten, dass die Tocilizumab-Monotherapie eine valide Behandlungsoption darstellt.
ADACTA-Studie. Die Ergebnisse der Phase IV der ADACTA-Studie, in der die Wirksamkeit und Sicherheit von TCZ vs. TNF-Blocker (Adalimumab) als Monotherapie bei RA-Patienten mit hoher Krankheitsaktivität bewertet wurde, wurden präsentiert. 3 Die Monotherapie mit TCZ war einer Monotherapie mit Adalimumab bei RA-Patienten, die eine MTX-Unverträglichkeit oder MTX-Unwirksamkeit hatten, hinsichtlich der Verringerung der Symptome der RA überlegen. Das allgemeine Sicherheitsprofil beider Medikamente war ähnlich den zuvor veröffentlichten Daten.
Subkutane Applikation. Zu Tocilizumab wurden auch Studien zur subkutanen Applikation vorgestellt. In der MUSASHI-Studie wurde die Wirksamkeit der intravenösen gegenüber der subkutanen Tocilizumab-Monotherapie verglichen, welche beinahe identische Ergebnisse in beiden Behandlungsgruppen zeigte.
Fragen für die Zukunft
Alle neuen Erkenntnissen bringen auch neue Fragen mit sich, daher wurden auch die Fragestellungen für die Zukunft ausgearbeitet:
- Wirksamkeit bei Dosisreduktion oder Intervallverlängerung
- Wirksamkeit nach Versagen der Non-TNF-Biologika
- Prädiktoren für das Ansprechen oder die Notwendigkeit einer Dosissteigerung
- Systemische Studien möglicher Kombinationstherapien mit anderen DMARD
- Andere Indikationen, z. B. der Effekt auf systemische Osteoporose
- Sicherheit in der Schwangerschaft oder bei chirurgischen Interventionen Neue IL-6-Inhibitoren Tocilizumab wird bald nicht mehr der einzige IL-6-Inhibitor bleiben.
Sirukumab. Das zeigten uns die Ergebnisse der Phase-II-Studie mit Sirukumab, einem humanen anti-IL-6-monoklonalen Antikörper. Sirukumab in Kombination mit MTX verbesserte die körperliche Funktion und reduzierte andere Zeichen und Symptome der RA.4
Sarilumab. In der Phase II der MOBILITY-Studie mit Sarilumab, dem ersten vollständig humanen monoklonalen Antikörper gegen IL-6Rα, wurde die Wirksamkeit und Sicherheit von 5 verschiedenen Dosierungen von subkutanem Sarilumab plus Methotrexat (MTX) im Vergleich zu Placebo plus MTX evaluiert.5 Das ACR20-Ansprechen in Woche 12 war aber statistisch nur in der 150-mg-Dosisgruppe signifikant besser. Art und Häufigkeit von Nebenwirkungen waren vergleichbar mit jenen, die zuvor bei IL-6-Inhibitoren beobachtet wurden. Beim Vortrag wurden die Phase-III-Studien angekündigt, bei der die langfristige Wirksamkeit von Sarilumab beurteilt werden soll.
Neue Anti-IL-20-Therapeutika
NNC0109-0012 ist ein neuer humaner monoklonaler IgG4-Antikörper, der die Aktivität des proinflammatorischen Zytokins Interleukin-20 neutralisiert. In der Phase-II-Studien wurden die Wirksamkeit und Sicherheit von NNC0109-0012 (Anti-IL-20-MAB) bei Patienten mit rheumatoider Arthritis überprüft6. NNC0109-0012 wurde über einen Zeitraum von 12 Wochen in der Dosierung von 3 mg/kg einmal wöchentlich s. c. in Kombination mit MTX verabreicht, dabei konnte eine deutliche Reduktion der Aktivität der Erkrankung gezeigt werden. Die neue Substanz zeigte ein günstiges Sicherheits- und Verträglichkeitsprofil.
Small modular immunopharmaceuticals (SMIP) sind von Antikörpern abgeleitete Proteine. Ihre therapeutische Anwendung wurde in der Studie mit SBI-087 (humanisiertes, gegen CD20 gerichtetes SMIP) geprüft. SBI-087 wurde subkutan verabreicht und allgemein gut vertragen.7 In der Dosierung von 200 mg erreichte SBI-087 eine signifikante Verbesserung der RA im Vergleich mit Placebo.
Zukünftige Therapie-Targets – neue Zytokine IL 17, Gm-CSF
Target: Gm-CSF. Die Ergebnisse der Phase-II-Studie Mavrilimumab (CAM-3001), einem humanen Antikörper gegen GMCSFRα, zeigten eine schnelle (innerhalb von 2 Wochen) und klinisch signifikante Wirkung vs. Placebo, vor allem in den höheren Dosen (100 mg)8.Die beobachteten Nebenwirkungen waren im Allgemeinen leicht bis mittelschwer; die häufigsten Ereignisse waren ein Rückgang der CO2-Diffusionskapazität, Nasopharyngitis oder Infektionen der oberen Atemwege. Auf weitere klinische Daten dieser neuen Anti-GM-CSFRα-mAk darf man gespannt sein.
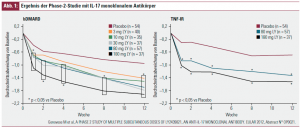
IL-17 (oder IL-17A) ist ein proinflammatorisches Zytokin, das primär von einer Subgruppe von CD4 + T-Zellen, genannt Th17-Zellen, produziert wird, die eine zusätzliche Untergruppe von CD4 + „Helfer“-Lymphozyten neben den klassischen Th1- und Th2-Populationen darstellt. Bisher konnte nachgewiesen werden, dass aberrante Th17-Antwort und inadäquate IL- 17-Produktion mit einer Vielzahl von Autoimmunerkrankungen, einschließlich der RA, in Verbindung stehen.
In der 2. Phase einer Studie mit dem Anti-IL-17-monoklonalen Antikörper LY2439821 (LY) wurde die Sicherheit und Wirksamkeit in einer DMARD-naiven Gruppe und einer, die unzureichend auf TNF-Blocker-Therapie angesprochen hatte, überprüft. LY verbesserte deutlich die Anzeichen und Symptome der RA im Vergleich zu Placebo (Abb. 1)9.
Neue Behandlungsstrategie
In der IDEA-Studie konnte gezeigt werden, dass eine frühzeitige intensive Behandlung mit Infliximab (IFX) in gleichem Ausmaß wie ein einmaliger Steroidpuls nur zu minimaler radiologischer Progression innerhalb des Beobachtungszeitraums einer zielangepassten Kombinationstherapie von 78 Wochen führte. 10
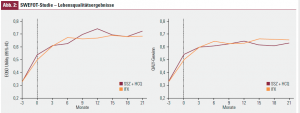
Aus der SWEFOT-Studie wurde der Effekt zweier unterschiedlicher Therapiemodalitäten auf die Lebensqualität untersucht.11 Über einen Zeitraum von 21 Monaten wurden bei Patienten mit aktiver RA im Frühstadium unter laufender Therapie mit Methotrexat (MTX) und Zugabe von entweder Infliximab (IFX) oder Sulfasalazin und Hydroxychloroquin (SSZ + HCQ) die Lebensqualität anhand des EuroQol-5-Scores (EQ-5D) gemessen. Es konnten keine statistisch signifikanten Unterschiede nachgewiesen werden (Abb. 2).
Neue synthetische kleine Moleküle in der RA-Therapie
CCX354-C ist ein spezifischer Antagonist des CC-Chemokin-Rezeptor-1, der die Migration von Monozyten und Makrophagen in das Synovialgewebe regelt. CCR1 ist auch an der Osteoklastenreifung, Mobilität und Aktivierung beteiligt. In einer Phase- II-Studie wurde die Sicherheit und Verträglichkeit von CCX354-C als primärer und die Wirksamkeit als sekundärer Endpunkt in der Therapie der RA evaluiert. CCX354-C scheint sicher und gut verträglich sowie klinisch wirksam zu sein.12
Auch im Bereich der Kinaseinhibitoren gibt es Neues: In einer Metaanalyse zeigte der JAK-Hemmer Tofacitinib in 2 verschiedenen Dosierungen vergleichbare Ergebnisse wie TNF-Blocker und andere Biologika, was den ACR-20-, -50- und -70-Respons angeht.13 Auch GLPG0634, ein oraler JAK-1-Inhibitor konnte in einer Phase-II-Studie14 vielversprechende Ergebnisse vorweisen.
Insgesamt gab es also eine Fülle von neuen Daten, die unseren klinischen Alltag in den nächsten Jahren beeinflussen werden, um die Therapie der Patienten mit rheumatoider Arthritis zu verbessern.
1 Breedveld FC, Arthritis & Rheumatism 2006
2 Abstract N° THU0093
3 Abstract N° LB0003
4 Abstract N° THU0100
5 Abstract N° OP0023
6 Abstract N° LB0004
7 Abstract N° OP0024
8 Abstract N° FRI0182
9 Abstract N° OP0021
10 Abstract N° OP0156
11 Abstract N° OP0155
12 Abstract N° OP0203
13 Abstract N° THU0151
14 Abstract N° OP0263