Teil 7: JAK-Inhibitoren – ein neues Therapiekonzept
Es ist unbestritten, dass proinflammatorische Zytokine, wie z. B. Interleukin-6 (IL-6), einen nicht unwichtigen Beitrag zur Aufrechterhaltung chronischer Entzündungen wie der chronischen Polyarthritis (CP) leisten. Diese Zytokine mögen zwar nicht ursächlich für diese Erkrankungen sein, doch reicht es oft aus, nur einen dieser Faktoren zu blockieren, um die Entzündung in den Griff zu bekommen. Dieses Wissen findet tagtäglich sehr erfolgreich durch den Einsatz neutralisierender, monoklonaler Antikörper, wie z. B. gegen TNF oder IL-6, Anwendung.
Anforderungsprofil für neue Biologika
Trotz der bekannten vorzüglichen Eigenschaften dieser Therapieformen gibt es aber auch einige Nachteile. Da diese monoklonalen Antikörper selbst Proteine sind, ist nur eine parenterale oder subkutane Applikation möglich. Dies ist oft für die PatientInnen nicht nur unangenehm, sondern kann, je nach Applikationsart, auch zu lokalen oder systemischen Nebenwirkungen führen. Außerdem stellen diese Antikörper selbst potenzielle Antigene dar. Ein Wirkungsverlust durch induzierte neutralisierende Antikörper gegen den therapeutischen monoklonalen Antikörper ist dann die Folge. Dass diese Antikörper sehr spezifisch nur auf ein Zytokin wirken, mag auch nicht immer von Vorteil sein. Man spricht nicht umsonst vom „inflammatorischen Netzwerk“, und die Neutralisation „nur eines“ dieser proinflammatorischen Faktoren ist manchmal nicht ausreichend. Zusätzlich sollen natürlich die hohen Kosten von monoklonalen Antikörper nicht unerwähnt bleiben.
Im Sinne eines Fortschritts sollten neue Therapieformen daher zusätzlich zu den Eigenschaften von monoklonalen Antikörpern folgende Anforderungen erfüllen: 1. orale Verfügbarkeit, 2. gleichzeitige Neutralisation mehrerer proinflammatorischer Zytokine oder deren Signaltransduktion, 3. keine Toleranzentwicklung, 4. kostengünstiger bei gleicher Wirksamkeit.
In den letzten Jahren gewonnene Erkenntnisse, wie Zytokinsignaltransduktion von der Zellmembran in den Zellkern genau funktioniert, haben nun zu neuen Therapiekonzepten wie den JAK-Inhibitoren (JAKinibs) geführt. Diese werden den oben beschriebenen Anforderungen durchwegs gerecht. Deren Wirkungsweise und Studienergebnisse zu Tofacitinib, der bisher am besten untersuchten Substanz dieser Medikamentenklasse, sollen im nachfolgenden Teil kurz beschrieben werden.
Konzept der Signaltransduktion durch Januskinasen (JAK)
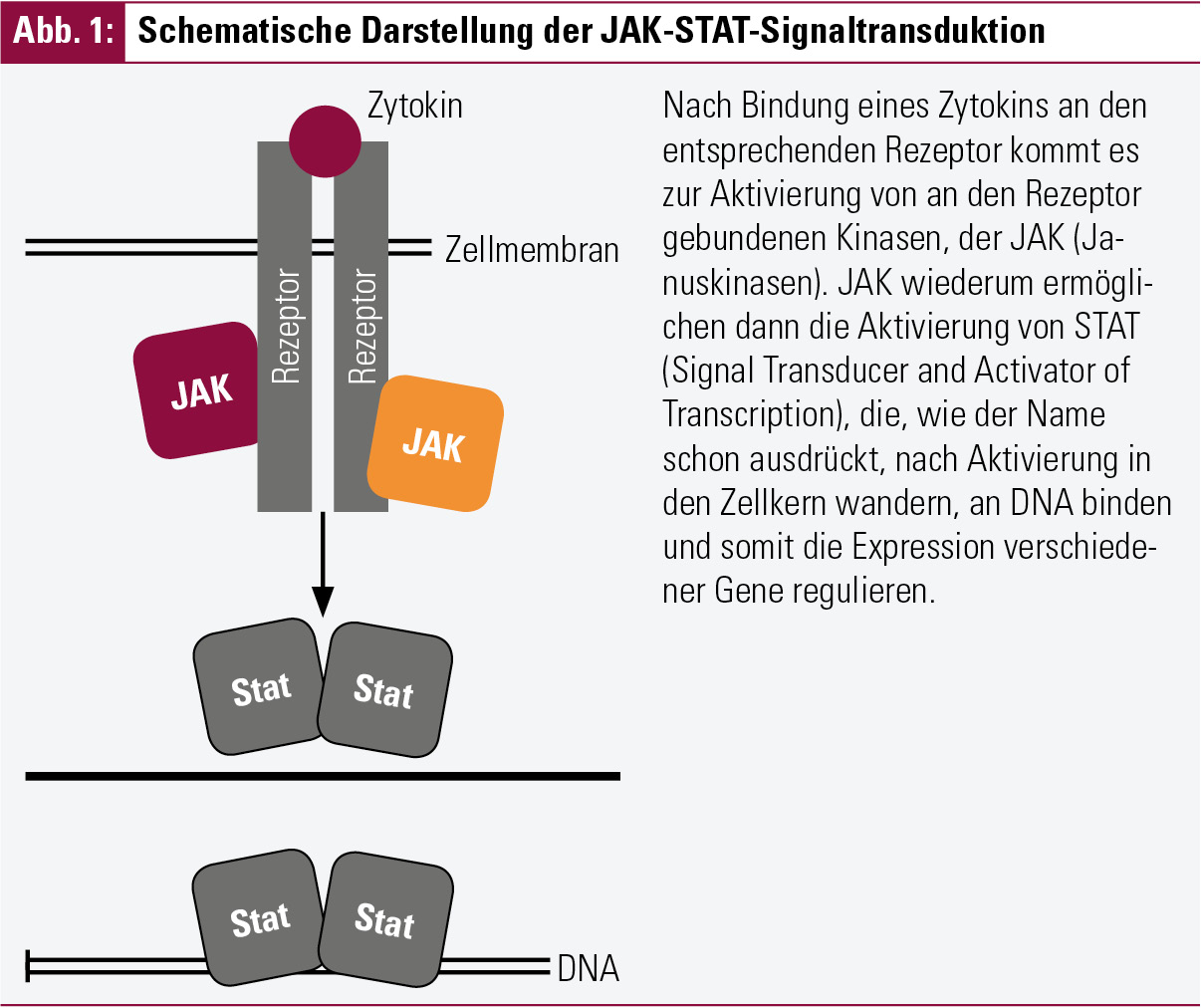
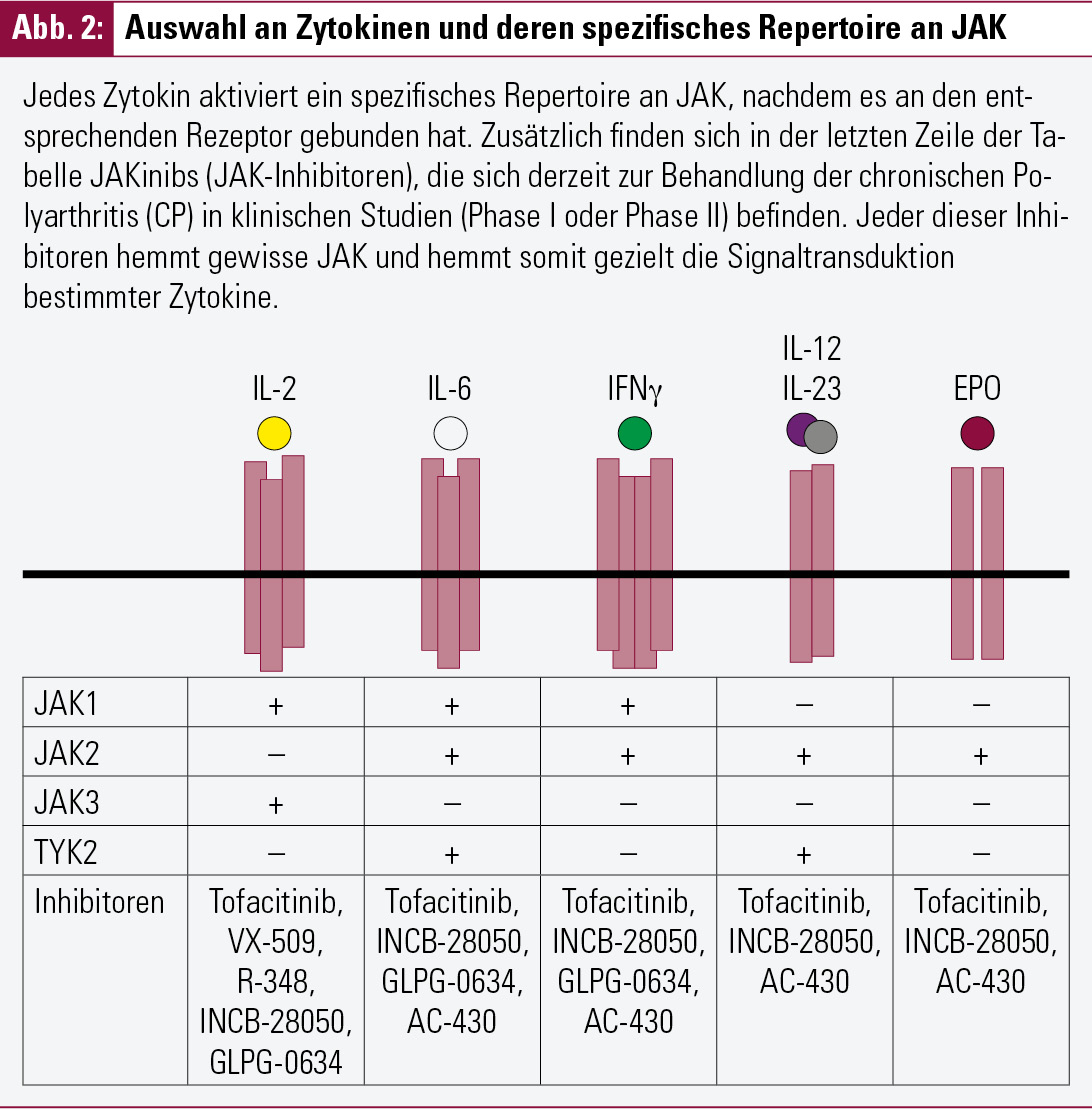
Viele bekannte Zytokine (z. B. IL-2, IL-6, IL-12) und auch Interferone binden an so genannte Zytokinrezeptoren der Klasse I oder Klasse II. Gemeinsam ist diesen Rezeptoren, dass nach Bindung des Zytokins an den spezifischen Rezeptor der so genannte JAK-STAT-Signaltransduktionsweg (JAK = Januskinase; STAT = Signal Transducer and Activator of Transcription) aktiviert wird. Das bedeutet, die Information, dass ein Zytokin an seinen spezifischen Rezeptor an der Zellmembran gebunden hat, wird über JAK und STAT in den Zellkern transportiert (Abb. 1). Während JAK nach Aktivierung am Rezeptor gebunden bleiben, bilden STAT nach ihrer Aktivierung durch JAK Dimere aus, wechseln in den Zellkern und regulieren durch Bindung an die DNA die Expression von Genen, z. B. von weiteren Zytokinen oder Chemokinen. Es sind vier JAKs (JAK1, JAK2, JAK3, TYK2) bekannt, von denen JAK1, JAK2 und TYK2 in den meisten Zellen zu finden sind. JAK3 wiederum ist primär in hämatopoetischen Zellen, wie z. B. B- und T-Zellen, exprimiert. Wichtig für das Verständnis der Wirkung von JAKinibs ist auch, dass, wie in Abbildung 2 ersichtlich, jeder Zytokinrezeptor sein spezifisches JAK-Repertoire aufweist. Somit ist es mit selektiven Inhibitoren möglich, gezielt Signaltransduktionswege auszuschalten. Ein spezifischer Inhibitor für JAK3 ermöglicht somit gezielt die Unterbindung der Signaltransduktion von IL-2, IL-4, IL-7, IL-9, IL-15 und IL-21. Dieses Wissen und das Faktum, dass JAK3 nur in hämatopoetischen Zellen zu finden ist, führte zur Entwicklung des bisher am besten untersuchten JAKinibs, nämlich Tofacitinib (früher: CP-690,550).
Prinzipiell, aufgrund der Vielzahl an Zytokinen, für die eine Rolle in der Immunpathogenese der CP gezeigt wurde, ist es aber durchwegs plausibel, dass auch die Inhibition anderer JAKs zur Therapie der CP genutzt werden kann. Deshalb laufen, wie in Abbildung 2 gezeigt, derzeit mehrere Studien mit JAKinibs, die jeweils ein spezifisches Muster hinsichtlich der Hemmung von JAK aufweisen.
Januskinase-Inhibitor Tofacitinib bei chronischer Polyarthritis
Im Folgenden soll kurz auf die Erfahrungen mit Tofacitinib, dem bisher am besten untersuchten JAKinib, auf Basis der bisher vorliegenden Phase-II-Studien eingegangen werden. Tofacitinib wurde zur spezifischen Hemmung von JAK3 konzipiert. Es handelt sich bei diesem Medikament um einen oral verfügbaren ATP-kompetitiven JAKinib.
In den bisherigen Studien konnte eine Wirksamkeit von Tofacitinib sowohl als Monotherapie als auch in Kombination mit Methotrexat (MTX) gezeigt werden. Unabhängig ob als Monotherapie oder in Kombination mit MTX, zeigten circa 2 Drittel der PatientInnen eine ACR20-, die Hälfte eine ACR50- und ein Viertel eine ACR70-Response in diesen Studien, die 12–24 Wochen liefen. Generell wurde Tofacitinib gut vertragen, wenige PatientInnen berichteten von Übelkeit oder Kopfschmerzen. Es zeigte sich aber, wie bei anderen Immunsuppressiva, eine erhöhte, aber tolerable Anfälligkeit für Infektionen, wie Harnweginfekte oder Pneumonien. Weiters kam es bei PatientInnen, die mit Tofacitinib behandelt wurden, zu einem leichten Anstieg von Kreatinin, HDL- und LDL-Cholesterin. Es soll aber auch angemerkt werden, dass Tofacitinib nicht so spezifisch wirkt, wie anfänglich angenommen, da es auch JAK1 und JAK2 hemmt. Dies sollte einerseits kein Nachteil sein, da Tofacitinib dadurch zusätzlich die Signaltransduktion von IL-6 und Interferon g (IFN-g) blockiert. Andererseits wurden leichte Anämien als eine weitere Nebenwirkung beschrieben, was darauf zurückgeführt wurde, dass Erythropoetin (EPO) JAK2 zur adäquaten Signaltransduktion benötigt.
Derzeit laufen mehrere Phase-III-Studien mit Tofacitinib.
Zusammenfassung
Mit den oral verfügbaren JAKinibs wird sich das therapeutische Spektrum zur Behandlung chronisch-entzündlicher Erkrankungen, vor allem der CP, deutlich erweitern. Die bisher dazu vorliegenden Studien sind sehr viel versprechend. Wo sich diese Inhibitoren jedoch im Spektrum zwischen DMARD und Biologika genau einordnen werden, können erst die laufenden Phase-III-Studien zeigen.