Vitamin D und Fertilität

Vitamin D ist ein Steroidhormon. Ungefähr 80–90 % des sich im Körper befindlichen Vitamin D entstehen durch Sonnenlicht-induzierte Produktion in der Haut. Ein sehr viel kleinerer Teil, nämlich 10–20 %, stammt aus der Nahrung. Das durch die Nahrung aufgenommene oder durch Sonnenlicht synthetisierte Vitamin D wird in weiterer Folge in der Leber durch das Enzym 25-Hydroxylase zu 25-Hydroxyvitamin D3 (25[OH]D) umgewandelt, welches gemessen wird, um den Vitamin-D-Status eines Patienten zu bestimmen.
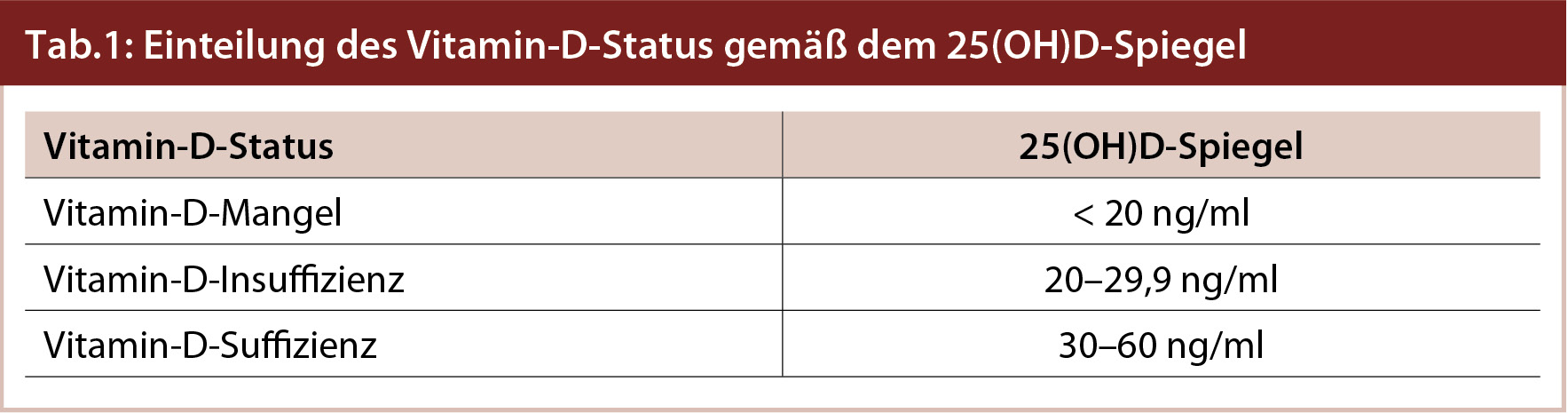
Als Vitamin-D-suffizient wird ein 25(OH)D-Serumspiegel von 30–60 ng/ml erachtet, liegt der Spiegel zwischen 20 und 29 ng/ml, spricht man von Vitamin-D-Insuffizienz, bei einem 25(OH)D-Spiegel von < 20 ng/ml liegt eine Vitamin-D-Defizienz vor (Tab. 1).
In weiterer Folge wird 25(OH)D in der Niere oder auch in anderen Geweben durch das Enzym 1α-Hydroxylase zu seiner aktiven Form, dem 1,25-Dihydroxyvitamin D3 (1,25[OH]2D3), umgewandelt. Die Vitamin-D-Wirkung entfaltet sich u. a. über den Vitamin-D-Rezeptor (VDR), der sich neben den klassischen Vitamin-D-Zielgeweben, wie Knochen, Darm und Epithelkörperchen, auch in Herzmuskelzellen findet.
Über die klassische Rolle von Vitamin D im Kalzium- und Knochenstoffwechsel hinaus haben jüngste Forschungsergebnisse das öffentliche Interesse an Vitamin D bzw. Vitamin-D-Mangel geweckt. So wurde der VDR in nahezu allen Zellen und Geweben des menschlichen Körpers gefunden, darunter auch Eierstöcken, Gebärmutter und Hoden, was darauf schließen lässt, dass Vitamin D auch eine mögliche Wirkung in diesen Zellen entfaltet. Ein Vitamin-D-Mangel ist in der Bevölkerung sehr häufig und mit verschiedenen chronischen Erkrankungen, wie z. B. Autoimmunerkrankungen, Typ-2-Diabetes, Bluthochdruck, Herz-Kreislauf-Erkrankungen sowie Infertilität verbunden.
Besonders häufig ist ein Vitamin-D-Mangel in Österreich einerseits bei älteren und adipösen Menschen und andererseits bei Personen mit dunklerem Hauttyp/einer stark pigmentierten Haut. In Österreich ist nur in den Monaten Mai bis September die Sonneneinstrahlung intensiv genug, um eine ausreichende Vitamin-D-Synthese in der Haut zu ermöglichen. Man geht davon aus, dass 3-mal wöchentlich 15–30 Minuten Sonneneinstrahlung (Gesicht, Arme und Beine) ausreichen, um einen adäquaten Vitamin-D-Spiegel (30–40 ng/ml) zu erreichen, wobei die exakte Dauer und Häufigkeit natürlich vom Hauttyp abhängig ist. Anzumerken ist, dass ein UV-Schutz in Form von Sonnencremes oder auch Hautcremes mit integriertem Lichtschutzfaktor eine Vitamin-D-Synthese in der Haut vermindert.
Vitamin D und Fertilität bei Frauen
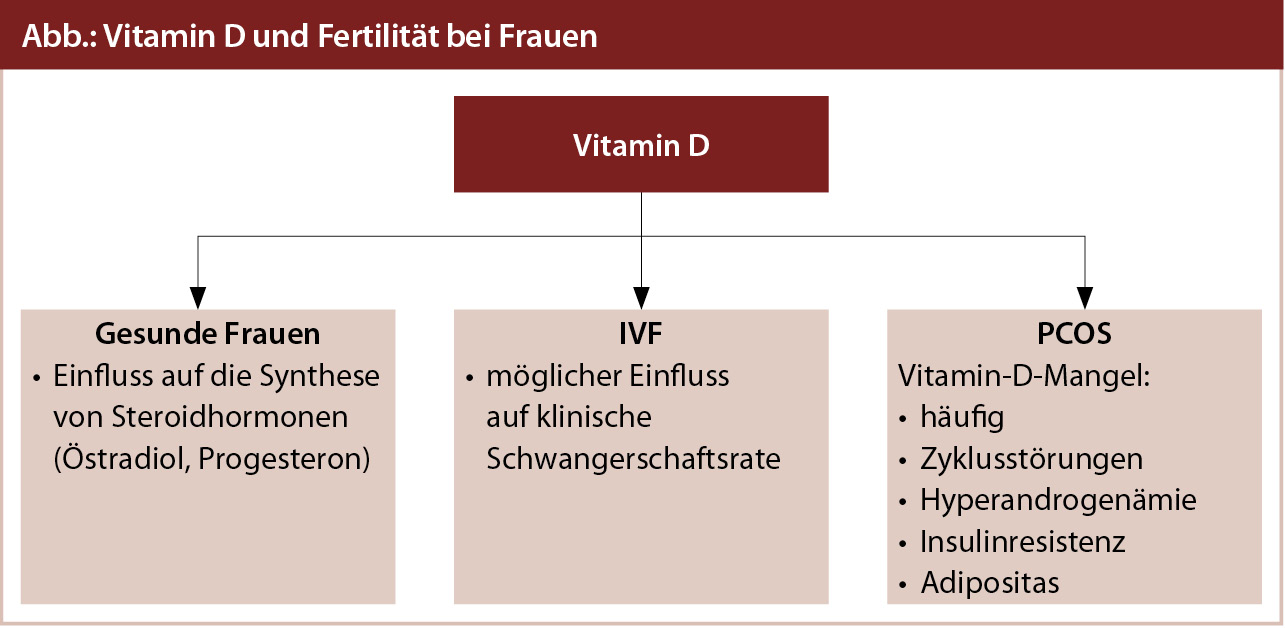
Neben der klassischen Rolle von Vitamin D im Kalzium- und Knochenstoffwechsel legen Studien eine wichtige Rolle von Vitamin D in der Fertilität der Frau nahe (Abb.). So konnte gezeigt werden, dass Vitamin D bzw. der Vitamin-D-Mangel die Steroidhormonsynthese bei gesunden Frauen beeinflusst, bei Frauen mit polyzystischem Ovar-Syndrom (PCOS) hinsichtlich Stoffwechselfunktion und hormonellen Faktoren wichtig ist und dass Vitamin D auch eine Rolle bei In-vitro-Fertilisationen (IVF) spielt.1
In-vitro-Fertilisation (IVF): Schon im Jahr 2000 konnte gezeigt werden, dass die Schwangerschaftsrate nach IVF im Herbst am höchsten und im Frühjahr am niedrigsten ist.2 Interessanterweise sind aufgrund der wechselnden Sonneneinstrahlung auch die 25(OH)D-Spiegel im Herbst am höchsten und im Frühjahr am niedrigsten. In einer weiteren Studie im Jahr 2010 wurde beobachtet, dass bei Frauen mit einem hohen 25(OH)D-Spiegel in der Follikelflüssigkeit, welcher eng mit dem Serum-25(OH)D korreliert ist, sowohl die Implantations- als auch die klinischen Schwangerschaftsraten nach IVF deutlich höher sind als bei Frauen mit niedrigeren 25(OH)D-Spiegeln.3 In einer kürzlich publizierten Studie bei 91 Frauen mit PCOS wurde festgestellt, dass ein niedriger Vitamin-D-Spiegel mit einer deutlich schlechteren Schwangerschaftsrate nach Clomiphen-Behandlung (zur Auslösung des Eisprunges) verbunden ist als ein hoher Vitamin-D-Spiegel.4
Polyzystisches Ovar-Syndrom (PCOS): Frauen mit PCOS haben u. a. einen hohen Spiegel an männlichen Hormonen (Hyperandrogenämie) und/oder einen nur selten auftretenden oder gänzlich ausbleibenden Eisprung (Oligo- oder Anovulation) und/oder Eierstockbläschen. Zusätzlich sind betroffene Frauen häufig übergewichtig oder adipös und haben einen gestörten Glukosestoffwechsel oder eine Insulinresistenz und leiden häufiger an unerfülltem Kinderwunsch. In der Grazer PCOS-Kohorte konnte gezeigt werden, dass der Vitamin-D-Mangel bei PCOS-Frauen mit Adipositas, Glukosetoleranzstörung, Insulinresistenz und dem metabolischen Syndrom assoziiert ist.5 Weiters konnten wir zeigen, dass es bestimmte, mit dem Vitamin-D-Status assoziierte genetische Veränderungen (Polymorphismen) gibt, die einerseits zu einem Vitamin-D-Mangel prädisponieren und andererseits auch mit Stoffwechselveränderungen wie Insulinresistenz verbunden sind.6 Daraus ergibt sich die Forschungsfrage, ob die Vitamin-D-Supplementierung auch zu einer Verbesserung von Stoffwechsel und hormonellen Parametern führen kann. Bereits 1999 wurde in einer Pilotstudie bei 13 Frauen mit PCOS und Zyklusstörungen gezeigt, dass eine Kombination aus Kalzium- und Vitamin-D-Supplementierung zu einer deutlichen Verbesserung der Zyklusunregelmäßigkeiten führen kann.7 Diese Ergebnisse konnten wir bei 57 Frauen mit PCOS bestätigen und um detaillierte Stoffwechseldaten erweitern.8 So führte die Einnahme von 20.000 Internationalen Einheiten (IE) Vitamin D wöchentlich über 24 Wochen sowohl zu einer deutlichen Verbesserung des Glukosestoffwechsels als auch zu einer Normalisierung initial bestehender Zyklusstörungen.
Vitamin D und Schwangerschaft: Neben der oben beschriebenen Vitamin-D-Wirkung hinsichtlich Zyklus, Konzeption und IVF-Erfolg spielt Vitamin D auch in der Schwangerschaft eine entscheidende Rolle. So wurde gezeigt, dass ein Vitamin-D-Mangel zwischen der 15. und 20. Schwangerschaftswoche das Risiko für eine Präeklampsie (erhöhter Blutdruck und Eiweiß im Harn) deutlich erhöht.9 Auch das Risiko für einen Schwangerschaftsdiabetes war bei Frauen mit Vitamin-D-Mangel signifikant höher als bei Frauen mit suffizientem Vitamin-D-Status. Frauen mit Schwangerschaftsdiabetes hatten einen deutlich niedrigeren 25(OH)D-Spiegel als Frauen ohne Schwangerschaftsdiabetes.10 Weiters erhöht ein Vitamin-D-Mangel das Risiko für einen Kaiserschnitt anstelle einer normalen Geburt11, was einerseits durch eine potenzielle Muskelschwäche als auch durch mögliche rachitische Beckendeformierungen infolge des Vitamin-D-Mangels zu erklären sein könnte. In einer randomisierten kontrollierten Studie, in der schwangere Frauen entweder 400 oder 4.000 IE Vitamin D täglich erhielten, wurde gezeigt, dass die Vitamin-D-Supplementierung absolut sicher und nebenwirkungsfrei ist und zu einer signifikanten Reduktion von Frühgeburten, Infektionen der Mutter und Komorbiditäten (Schwangerschaftsdiabetes, Bluthochdruck, Präeklampsie) führt (Tab. 2).12 Die Schlussfolgerung der Autoren dieser Studie war, dass jeder Schwangeren täglich 4.000 IE Vitamin D täglich und jeder stillenden Frau 6.400 IE einzunehmen empfohlen wurde.
Vitamin D und Fertilität bei Männern
Auch bei der männlichen Fertilität spielt Vitamin D eine wichtige Rolle. So gibt es Hinweise, dass Vitamin D die Androgensynthese beeinflusst, für die Samenqualität wichtig ist und auch einige Testikulopathien (Erkrankungen des Hodens) mit Veränderungen des Vitamin-D-Spiegels einhergehen.1
Vitamin D und Testosteron: Während die individuelle Rolle von Vitamin D einerseits und Testosteron andererseits in der Knochen- und metabolischen Gesundheit des Mannes seit Langem bekannt sind, war lange
Zeit unklar, ob es einen Zusammenhang zwischen den beiden Hormonen selbst gibt. In unserer Grazer Forschungsgruppe konnten wir erstmals zeigen, dass ein Vitamin-D-Mangel mit einem 2,5-fach erhöhten Risiko für einen Testosteronmangel verbunden ist.13 Der Testosteronmangel per se ist mit negativen Auswirkungen auf die kardiovaskuläre Gesundheit bis hin zu einer deutlich erhöhten Mortalität verbunden.14, 15 Weiters konnten wir zeigen, dass nicht nur der 25(OH)D-Spiegel, sondern auch die Androgene beim Mann eine ausgeprägte saisonale Schwankung zeigen, mit den höchsten Spiegeln von Vitamin D und Testosteron im August und den niedrigsten Spiegeln im März.13 Der Zusammenhang von Testosteron und Vitamin D wurde kürzlich in zwei weiteren Studien bestätigt.16, 17 Weiters gibt es erste Hinweise zu Interventionsstudien, dass eine Vitamin-D-Supplementierung zu einem Anstieg des Testosteronspiegels bei Männern führt.18
Neue Forschungsergebnisse aus Graz legen nahe, dass das gleichzeitige Bestehen eines Vitamin-D- und Testosteronmangels bei Männern mit besonders ungünstigen Konsequenzen verbunden ist.19 Während das Vorhandensein entweder eines Vitamin-D-Mangels oder eines Testosteronmangels mit einem ca. 1,5-fach erhöhten Mortalitätsrisiko einhergeht, ist das gleichzeitige Vorliegen eines Mangels beider Hormone mit einem 2,5-fach erhöhten Risiko zu sterben verbunden, im Vergleich zu Männern mit einem suffizienten Vitamin-D- und Testosteronspiegel. Weiters war der Testosteronmangel nur bei jenen Männern mit einer erhöhten Sterblichkeit verbunden, die einen Vitamin-D-Mangel hatten, wohingegen bei Männern mit einem suffizienten Vitamin-D-Spiegel kein signifikanter Zusammenhang zwischen Androgenmangel und einer erhöhten Mortalität vorhanden war.
Vitamin D und Samenqualität bei Männern: Neben der Rolle von Vitamin D im Androgenstoffwechsel des Mannes ist Vitamin D auch in der Spermatogenese bedeutsam. Studien aus Dänemark zeigen, dass ein hoher Vitamin-D-Spiegel mit einer guten Samenqualität verbunden ist.20 Sowohl die Beweglichkeit als auch die Morphologie der Spermien waren bei jenen Männern deutlich besser, welche einen hohen normalen Vitamin-D-Spiegel hatten. Erste Ergebnisse aus Graz zeigen, dass Männer mit einem pathologischen Samenbefund einen signifikant niedrigeren 25(OH)D-Spiegel haben als Männer mit einem normalen Spermiogramm.21
Vitamin-D-Messung und Supplementierung
Es gibt unterschiedliche Empfehlungen, wann der Vitamin-D-Spiegel gemessen werden sollte. So gibt es die Empfehlung eines internationalen Experten-Komitees, 25(OH)D bei allen Personen zu messen, bei denen muskuloskelettale Probleme (z. B. Osteoporose), kardiovaskuläre Erkrankungen, Diabetes, ein arterieller Hypertonus, Autoimmunerkrankungen oder Karzinome bestehen oder die ein hohes Risiko haben, an den angeführten Leiden zu erkranken, sowie bei institutionalisierten Menschen (Krankenhaus, Alten- bzw. Pflegeheim).22 Aufgrund der bestehenden Datenlage kommen viele Experten zu dem Schluss, dass auch bei Personen mit hormonellen Störungen und/oder Infertilität der 25(OH)D-Spiegel gemessen werden sollte.
Die genauen Referenzwerte eines „optimalen“ Vitamin-D-Status sind ein viel und kontrovers diskutiertes Thema. Die momentan verfügbare Evidenz aus Studien legt nahe, dass ein 25(OH)D-Spiegel zwischen 30 und 40 ng/ml optimal sei. Wenn der Vitamin-D-Spiegel unter 30 ng/ml liegt, steigt konsekutiv PTH an, was neben einem ungünstigen Effekt auf Knochenmineralisation und -morphologie auch ungünstigen Effekte auf das Herz-Kreislauf-System hat.
In zwei großen Metaanalysen konnte gezeigt werden, dass die Vitamin-D-Supplementierung in der Bevölkerung die Sterblichkeit um 6 % bzw. 7 % zu senken vermag.23, 24 Wenn man sich nun bei einem 25(OH)D-Spiegel < 30 ng/ml zur Vitamin-D-Supplementierung entschließt, gilt die Faustregel, dass 1.000 IE Vitamin D den 25(OH)D-Serumspiegel um 10 ng/ml erhöhen können (siehe Tab. 3). Es kann entweder eine tägliche oder wöchentliche Supplementierung erfolgen, auch sehr hohe Dosen mit 10.000 IE täglich und 25(OH)D-Spiegeln bis 150 ng/ml blieben ohne Nebenwirkungen wie z. B. Hyperkalzämie oder Nephrolithiasis. Das heißt, die Vitamin-D-Supplementierung ist eine sehr sichere Therapie. Eine Wiederholung der 25(OH)D-Messung ist 3 Monate nach Therapiebeginn empfehlenswert, um zu evaluieren, ob die Dosis adäquat ist und um einen 25(OH)D-Spiegel zwischen 30 und 40 ng/ml das ganze Jahre über sicherzustellen.