Expression von p16, p16/Ki-67 und L1 zur Verlaufsprognose – Biomarker in der Diagnostik von Zervixdysplasien
Unter den verschiedenen zellulären Proteinen, die bisher als potenzielle Biomarker evaluiert wurden, sind der Nachweis der Überexpression des p16INK4a- Proteins bzw. der Expression des viralen L1-Proteins für die Praxis relevant geworden.
p16-Nachweis
Monoklonaler p16-Antikörper für die Detektion des Biomarkers p16INK4a (p16) (Fa. mtm): Der Zyklin-abhängige Kinaseinhibitor p16 ist ein den Zellzyklus regulierendes Protein, welches bei durch High-Risk-HPV (HPV-HR) induzierter, durch das virale E7-Onkoprotein vermittelter Inaktivierung des Retinoblastomgens überexprimiert wird. Dieses Epiphänomen der durch HPV induzierten Karzinogenese wird derzeit in der Histopathologie zunehmend genutzt. Auch in der Zytopathologie beginnt der Einsatz des Nachweises der Überexpression von p16, zunehmend auch in Kombination mit dem Nachweis des proliferationsassoziierten Antigens Ki-67.
p16-Nachweis in der Histopathologie der Zervix: Bei zervikalen intraepithelialen Neoplasien (CIN), die durch transformierende HPV-HR-Infektionen verursacht wurden, und beim Adenocarcinoma in situ der Zervix ist die p16-Immunhistochemie positiv. Ein negatives Färbeergebnis zeigt sich hingegen bei unreifer und tubarer Metaplasie, bei reaktiven Läsionen, mikroglandulärer Hyperplasie und bei CIN auf dem Boden von Low-Risk-HPV-Infektionen (HPV-LR).
Durch den immunhistochemischen Nachweis einer Überexpression von p16 kann die histologische Diagnostik von Portiobiopsien und Konisaten signifikant verbesserte werden (Bergeron C., Am J Clin Pathol 2010; 133:395). Dies ist in erster Linie für CIN-2-Läsionen mit einer bekannt hohen Rate von Meinungsverschiedenheiten zwischen verschiedenen Diagnostikern und insbesondere in der Abgrenzung zu unreifen Metaplasien relevant. Auch kann auf die Klassifikation von so genannten atypischen Metaplasien verzichtet werden, da solche Veränderungen bei p16-Positivität den Dysplasien zuzurechnen sind (Regauer S., Histopathology 2007;50:629).Neben diesem wichtigen Aspekt der Diagnostik, der einen objektiven Standard in der Beurteilung von Zervixbiopsien und Konisaten erlaubt, kann mit der p16-Immunhistochemie der Verlauf von CIN-1-Läsionen prognostiziert werden. Während CIN-1-Läsionen mit negativem Färbeergebnis mit einer hohen Rate von Regressionen assoziiert sind, zeigen p16-positive CIN-1-Läsionen vergleichsweise ein signifikant erhöhtes Risiko für eine Progression (Del Pino M., Am J Obstet Gynecol 2009; 201:488).
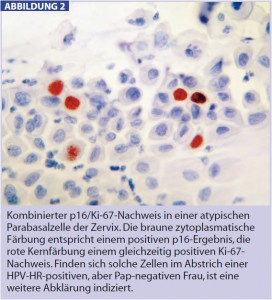
p16-Nachweis in der Zytopathologie der Zervix: Es konnte gezeigt werden, dass der immunzytochemische Nachweis von p16 eine signifikante Verbesserung der zytologischen Erkennbarkeit von höhergradigen Dysplasien im Vergleich zur herkömmlichen Pap-Zytologie erlaubt (Denton K. J., Am J Clin Pathol 2010; 134:12). In der Zytopathologie wird jedoch der alleinige Nachweis einer Überexpression von p16 zunehmend von einem kombinierten Nachweis von p16 und dem proliferationsassoziierten Antigen Ki-67 abgelöst (Abb. 1). Dieser p16/Ki-67-Doppelnachweis in Einzelzellen könnte zukünftig für die weitere Abklärung Pap-negativer, aber HPV-HR-positiver Frauen ab dem 30. Lebensjahr interessant werden, da sich in diesem Kollektiv bei positivem Färbeergebnis ein signifikanter Anteil behandlungswürdiger CIN-2+-Läsionen nachweisen lässt (Petry K. U., Gynecol Oncol 2011; 121:505). Eigene, bisher nicht publizierte Erfahrungen mit auffälligen Pap-Test-Ergebnissen in der Schwangerschaft zeigen, dass p16/Ki-67-positive Befunde mit einer Persistenz post partum assoziiert sind, während ein negatives Färbeergebnis eine Regression erwarten lässt.
L1-Nachweis
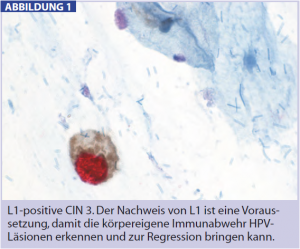
Nachweis des HPV-L1-Kapsidproteins (Fa. Cytoimmun): Als L1 wird eines von 8 spezifischen HPV-Proteinen bezeichnet. Der Nachweis dieses Proteins ist deshalb interessant, da L1 ein wesentliches Ziel für die Antwort des Immunsystems auf HPVInfektionen darstellt. Während L1-positive, z. T. auch höhergradige Dysplasien mit einem signifikanten Anteil von Regressionen assoziiert sind (Abb. 2), bleibt die Regression in der Gruppe L1-negativer Dysplasien weitgehend aus (Griesser H., Am J Clin Pathol 2009; 132:840).
Transportmedien
Der Nachweis von p16, p16/Ki-67 und L1 ist an Formalin-fixierten und in Paraffin eingebetteten Gewebeproben sowie mit konventionell fixiertem zytologischen Material möglich. Für Reflextestungen ist von der amerikanischen Gesundheitsbehörde FDA derzeit nur die PreservCyt®-Lösung, die in der Dünnschichtzytologie verwendet wird (ThinPrep® Pap Test/Cervista® HPV HR, Fa. Hologic) als Universalmedium für die weiterführende Diagnostik mittels molekularer Marker zugelassen. Hierbei handelt es sich um ein formaldehydfreies Methanol- basiertes Fixationsmedium, in das die beim Abstrich entnommenen Zellen direkt überführt werden. Reflextestungen mit Biomarkern haben den Vorteil, dass Frauen mit entsprechender Indikation für die weitere Diagnostik mit einem Biomarker oder HPV-Test nicht neuerlich einbestellt werden müssen, sondern die Analyse am gleichen Probenmaterial durchgeführt werden kann. Die immunzytochemischen Marker p16 und L1 können sowohl aus der ThinPrep®-Pap-Test-Lösung als auch aus anderen Dünnschichtzytologiemedien durchgeführt werden.
Zukunftsaspekte
Ein noch nicht gefundener idealer Biomarker würde einen „point of no return“ der Karzinogenese an der Zervix markieren. Möglicherweise ist dafür ein kombinierter Nachweis verschiedener Proteine sinnvoll (Kaskimaa H. M., Cancer Epidemiol Biomarkers 2010; 19:203). Auch könnte zukünftig der Nachweis von integrierten Papillomvirussequenzen einen weiteren inte – ressanten Biomarker darstellen, der es erlaubt, das Progressionsrisiko von Läsionen des Zervixepithels besser abzuschätzen. Ferner könnte der Nachweis von Zellen mit integrierten viralen Genomkopien die Rezidivdiagnostik verbessern helfen. Derzeit erscheinen insbesondere die Biomarker, die ihre klinische Relevanz in großen Studien wiederholt belegen können, für die klinische Praxis geeignet. Festzuhalten bleibt dabei, dass das Ergebnis der Testung von Biomarkern wie auch andere Faktoren, z. B. Alter oder HPV-Status der Patientinnen, mit in die Entscheidung zur Therapie einbezogen werden sollen. Es dürfen jedoch bis auf Weiteres die klassischen, dem Standard entsprechenden histo- und zytomorphologischen Befunde kein „Upgrading“ oder „Downgrading“ erfahren.