Brustkrebsscreening mit Mammografie und Ultraschall
Brustkrebs ist weltweit die führende Karzinomtodesursache bei Frauen. In Österreich erkranken jährlich etwa 5.000 Frauen an einem Mammakarzinom, etwa 1.600 sterben daran.1 Angesichts des Fehlens breit anwendbarer primärpräventiver Ansätze ist die Sekundärprävention in Form des populationsbasierten Screenings von entscheidender Bedeutung für die Senkung der Mortalität. Die Effizienz und Effektivität des organisierten Brustkrebsscreenings wurde in großen randomisierten Studien und mittlerweile auch in regulären Screeningprogrammen in mehreren europäischen Ländern nachgewiesen.2, 3
Mammografie als Screeningtest
Die Mammografie gilt als der einzige diagnostische Test mit nachgewiesener Effektivität im Screening. Die Methode hat allerdings entscheidende Nachteile: Im Strahlengang hintereinander gelegene Objekte werden aufeinander projiziert und können so dem Nachweis entgehen, andererseits können Läsionen durch Superpositionseffekte auch vorgetäuscht werden. Die geringen Unterschiede zwischen Tumor- und Drüsen- oder Bindegewebe in Bezug auf die Absorption von Röntgenstrahlen erschweren die Karzinomdetektion insbesondere in dichtem Mammaparenchym. Neue Verfahren, wie die digitale Mammografie und die Tomosynthese können diese Limitationen nicht vollständig kompensieren.
Während die Sensitivität der Mammografie in der Karzinomdiagnose in fettgewebsreichen Brüsten (Dichtegrad 1) bei bis zu 98 % liegt, sinkt sie mit zunehmender Parenchymdichte fast linear und beträgt bei dichten Brüsten mit einem Parenchymanteil von über 50 % (Dichtegrad 3 und 4) nur mehr 65 % bzw. 48 %.4 Diese hohen Brustdichtegrade finden sich bei über 50 % der Frauen unter 50 Jahren und bei 30–40 % der Frauen über 50 Jahre.5, 6 Auf Grund der limitierten Sensitivität der Screeningmammografie haben Frauen mit dichtem Mammaparenchym ein bis zu 6-fach höheres Risiko, zwischen den Screeningrunden ein Intervallkarzinom mit entsprechend schlechterer Prognose zu entwickeln.7 Die Brustparenchymdichte ist jedoch auch ein unabhängiger Risikofaktor: Frauen mit hoher Parenchymdichte haben ein 4- bis 6-fach höheres Risiko, an einem Mammakarzinom zu erkranken.8
Sonografie als additive Untersuchungsmethode
Die Sonografie wird seit Jahrzehnten als additives Verfahren in der Mammadiagnostik eingesetzt. Ihre Stärken liegen neben der breiten Verfügbarkeit in der Schnittbilddarstellung, der Real-Time-Fähigkeit („Durchleuchtungseffekt“), der fehlenden Strahlenbelastung und dem im Vergleich zur Mammografie erheblich besseren Kontrast in dichtem Gewebe.
Technische Entwicklungen, wie hochauflösende Sonden, die 3-D-Sonografie, farbkodierte Duplexsonografie und Elastografie, haben in den letzten Jahren die Sensitivität und Spezifität der Mammasonografie deutlich verbessert. Die Einführung standardisierter Befundkriterien (US-BIRADS bzw. US-BIRADS-Äqivalent der DEGUM/ÖGUM) hat die Untersucherabhängigkeit reduziert und die Validität der Sonografie als diagnostischem Test erhöht.9
Mehrere prospektive Studien haben gezeigt, dass die additive Sonografie bei Frauen mit dichtem Brustparenchym zu einer signifikanten Steigerung der Sensitivität führt. Die inkrementalen Karzinom-Detektionsraten lagen zwischen 2,3–4,6 Karzinomen pro 1.000 untersuchten Frauen.10–15 In der Innsbrucker Studie mit über 8.100 Frauen wurden 22 % aller Karzinome lediglich mit der Sonografie entdeckt.10 Allerdings handelte es sich durchwegs um selektionierte Patientinnengruppen mit einem im Vergleich zu einer typischen Screeningpopulation größeren Anteil an Frauen mit erhöhtem Brustkrebsrisiko. Als wesentliche Limitationen der additiven Sonografie zeigte sich in allen Studien eine niedrige Spezifität in der Karzinomdiagnose mit einem positiven prädiktiven Wert zwischen 3 % und maximal 25 %.
Die Screeningsituation in Österreich
Die Europäische Union hat im Jahr 2003 die Mitgliedsstaaten zur Implementierung von organisierten populationsbasierten Screeningprogrammen für alle Frauen zwischen 50 und 69 Jahren aufgerufen. Bereits seit dem Jahr 1993 existieren Umsetzungsleitlinien in Form der „European Guidelines for Quality Assurance in Breast Cancer Screening and Diagnosis“, welche derzeit in der 4. Auflage aus dem Jahre 2006 vorliegen.16
In Österreich ist die Mammografie als von den Krankenversicherungen bezahlte Vorsorgeuntersuchung breit verfügbar. In einer Mikrozensuserhebung aus dem den Jahren 2006–2007 gaben mehr als 80 % der Frauen zwischen 40 und 59 Jahren an, sich im vergangenen Jahr zumindest einer Mammografie unterzogen zu haben.17 Im Gegensatz zu einem organisierten populationsbasierten Screening werden die Frauen bei diesem „opportunistischen“ Screening nicht persönlich eingeladen, das Qualitätsmanagement ist rudimentär und eine Datenbasis für die Beurteilung der Screeningergebnisse existiert nicht. Die Effektivität dieser Vorsorgeuntersuchung kann daher nur geschätzt werden. Der seit Mitte der 1990er-Jahre auch in Österreich zu beobachtende Rückgang der Brustkrebsmortalität dürfte auf einen kombinierten Effekt von opportunistischem Screening und Fortschritten in der Brustkrebsbehandlung zurückzuführen sein.
Angesichts eines derart etablierten opportunistischen Screenings stellt sich für ein Gesundheitssystem die Frage der Transition in ein organisiertes Screening, ohne durch den Systemwechsel organisatorische Bruchstellen und einen Verlust an Akzeptanz in der Bevölkerung hinnehmen zu müssen. Als erster Schritt zur Implementierung eines nationalen Mammografie-Screeningprogramms in Österreich wurde daher von der Bundesgesundheitskommission im Jahr 2005 die Förderung von Pilotprojekten beschlossen. Das Programm „MammographieScreening Tirol“ wurde als Referenzprojekt konzipiert und unterscheidet sich daher von den anderen österreichischen Pilotprojekten in wesentlichen Punkten.6, 18–20
Das Tiroler Referenzprojekt
Das Programm startete im Mai 2007 in den Bezirken Innsbruck-Stadt und Innsbruck-Land und im Mai 2008 in allen Tiroler Bezirken. Die Screeningpopulation umfasst 123.000 Frauen zwischen 40 und 70 Jahren, das Einladungsintervall beträgt 12 Monate (40–59) bzw. 24 Monate (60–69). Die Frauen in der Zielgruppe werden persönlich eingeladen, es besteht jedoch freie Wahl der Screeningeinrichtung und des Termins. Die Screenings werden in 22 Screeningeinheiten (Radiologenpraxen und Krankenhausabteilungen) durchgeführt, die Abklärung erfolgt in definierten Assessmentzentren.
Durch den Aufbau einer Screeningdatenbank und durch Abgleich mit dem Tiroler Tumorregister können jährliche Evaluierungsberichte entsprechend den Vorgaben der „European Guidelines for Quality Assurance in Breast Cancer Screening and Diagnosis“ erstellt und publiziert werden.6, 20
Die 1-Jahres-Teilnahmerate lag bei 37,9 %, im Zeitraum von bis zu 2 Jahren nach der Einladung ergab sich eine Teilnahmerate von 58,9 %. Die Karzinomdetektionsrate lag nach Altersgruppen bei 0,25 % für die 40- bis 49-jährigen, bei 0,30 % für die 50- bis 59-jährigen und bei 0,59 % für die 60- bis 69-jährigen Frauen.
Die in den „European Guidelines“ angegebenen Performanceparameter wurden während der gesamten bisherigen Laufzeit des Programms erreicht und zum Teil deutlich übertroffen. So betrug der Anteil der Karzinome bis 10 mm Durchmesser 31,6 %, der Anteil der Tumoren mit einem Durchmesser von unter 15 mm lag bei 62,2 % und der Anteil an lymphknotennegativen Tumoren bei 75,7 %.
Mammasonografie im Screening
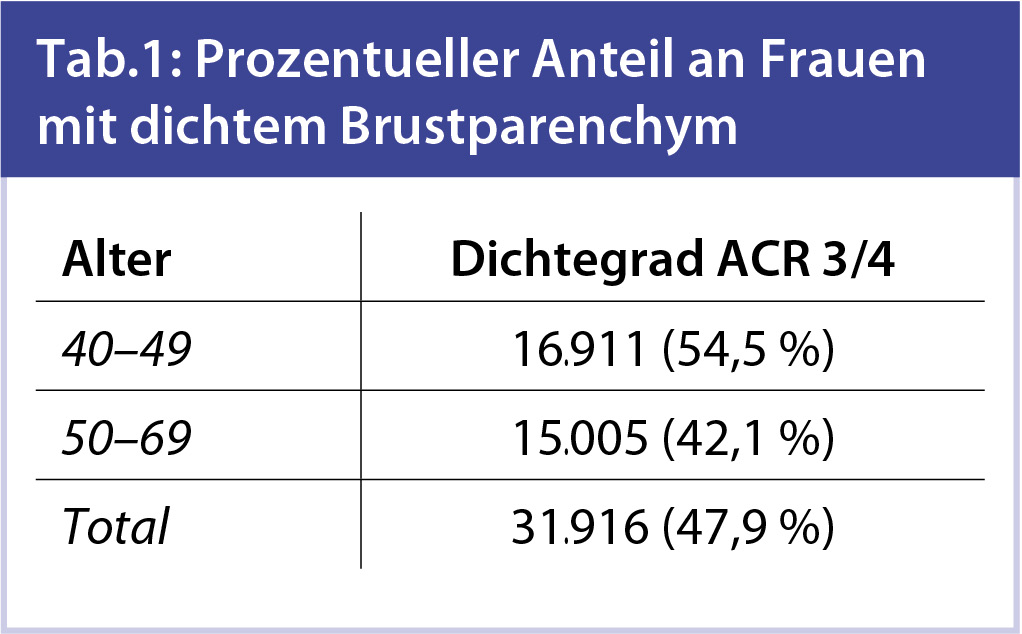
Im 2. und 3. Projektjahr des „Mammographie Screening Tirol“ (Juni 2008 – Mai 2010) wurden über 66.000 Mammasonografien im Rahmen des Screenings durchgeführt. Die Sonografierate wegen dichtem Mammaparenchym (Dichtegrad 3 oder 4) betrug 47,9 % mit deutlichen Unterschieden zwischen den Altersgruppen (Tab. 1).
Die Intervallkarzinomrate bezogen auf die Hintergrundinzidenz betrug für die Altersgruppe 50–69 Jahre im Zeitraum bis zu 12 Monaten 19,7 % und im Zeitraum bis zu 24 Monaten 37,5 %. Sie lag damit deutlich unter den in den europäischen Leitlinien geforderten 30 % bzw. 50 %. Besonders auffällig ist, dass die Intervallkarzinomrate in der Altersgruppe 40–49 Jahre – somit in der Altersgruppe mit der höchsten Brustgewebsdichte – mit 24,9 % der Hintergrundinzidenz nicht höher als in der Altersgruppe 50 bis 69 Jahre war. Diese Ergebnisse zeigen, dass mit dem kombinierten Einsatz von Mammografie und Sonografie auch in den jüngeren Altersgruppen eine annähernd gleich hohe Sensitivität wie in der klassischen Screeningpopulation zwischen 50 und 69 Jahren erreicht werden kann.
Trotz des umfassenden Einsatzes der Sonografie waren die negativen Effekte der Sonografie deutlich geringer als erwartet. So betrug der positive Vorhersagewert (PPV) für das Assessment, d .h. der Anteil der Karzinome unter den durchgeführten Assessments, immerhin 24,7 %. Der positive Vorhersagewert der Stanzbiopsie lag bei 43,9 %, d. h. über 40 % der gestanzten verdächtigen Läsionen waren tatsächlich Karzinome (Tab. 2).
Die Gründe für dieses deutlich bessere Abschneiden der Sonografie im Vergleich zu den früheren klinischen Studien liegen vermutlich in inzwischen verfügbaren technischen Verbesserungen, vor allem aber in der größeren Erfahrung der Untersucher mit der Mammasonografie und in der Standardisierung der Beurteilung und Befundung. Eine detaillierte Analyse von Nutzen, Risiken und Kosten der additiven Sonografie im Screening auf Basis der ab dem zweiten Pilotjahr erfolgten getrennten Erfassung der Mammografie- und Ultraschallergebnisse wird in Kürze vorliegen.
Das nationale Brustkrebs-Früherkennungsprogramm
Ab dem Jahr 2013 soll ein österreichweites, bevölkerungsbezogenes, systematisches und qualitätsgesichertes Screeningprogramm zur Früherkennung des Mammakarzinoms implementiert werden. Die Eckpunkte des Programms sind:
- persönliche Einladung aller Frauen zwischen 45 und 69 Jahren in 24-monatigen Intervallen
- 40- bis 44-Jährige und 70- bis 75-Jährige werden nicht aktiv eingeladen, können jedoch teilnehmen
- ausschließliche Verwendung von digitalen Mammografiegeräten, technische Qualitätssicherung nach EUREF-Ö
- obligatorische Doppelbefundung der Mammografieaufnahmen
- obligatorische Qualifikationsmaßnahmen für alle beteiligten Berufsgruppen, Mindestfallzahlen für die Mammografiebefundung (2.000 Screeningmammografien pro Jahr)
- additive Sonografie bei dichtem Brustgewebe (Dichtegrad 3 bis 4) und unklarem Befund in der Mammografie
Im nationalen österreichischen Screeningprogramm wird die Sonografie somit erstmals routinemäßig und unter kontrollierten Bedingungen im Screening eingesetzt. Die gewonnen Erfahrungen sollen die Evidenzbasis dieses Vorgehens weiter ausbauen und könnten zu einer Adaptierung der Screeningpolitik in zahlreichen anderen Ländern führen, für die Österreich eine Vorreiterrolle einnimmt.