Zielgerichtete Therapie bei endokriner Resistenz
Bei vielen Krebserkrankungen ist das mTOR-Signaling-System, dessen Name von Mammalian Target of Rapamycin (mTOR) abgeleitet wird, ein wichtiger Mediator der Zellproliferation. mTOR ist ein zentraler Regulator für Wachstum und Metabolismus und wird über verschiedene „Upstream“-Signalwege (z. B. Wachstumsrezeptoren wie HER2) reguliert bzw. aktiviert. „Downstream“ reguliert die mTOR-Aktivierung Zellproliferation, Angiogenese und Metabolismus sowohl in normalen als auch in malignen Zellen. Als erster Inhibitor von mTOR wurde Rapamycin (Sirolimus) entwickelt, das 1972 aus einer Bodenprobe der Insel Rapa Nui (Osterinsel) im Südpazifik isoliert wurde. Es handelt sich dabei um ein Produkt des Bakteriums Streptomyces hygroscopicus. Rapamycin hat potente antimykotische und auch immunsuppressive Eigenschaften, weshalb es auch in der Transplantationsmedizin eingesetzt wird. Daneben hat die Substanz aber auch eine starke antitumorale Wirkung.
Everolimus (RAD001) ist eines der seit den 1990er-Jahren entwickelten Rapamycin-Analoga („Rapalogs“). Everolimus hat ebenfalls eine immunosuppressive Wirkung, die unter anderem auf einer Hemmung der durch Zytokine induzierten Lymphozytenproliferation beruht. Darüber hinaus zeigt die Substanz bei verschiedenen Krebserkrankungen klinische Wirksamkeit und wird in klinischen Studien als zielgerichtete Therapie erprobt. Everolimus ist in seiner klinischen Entwicklung von allen mTOR-Inhibitoren am weitesten fortgeschritten.
Rolle des mTOR -Signalings bei Krebs
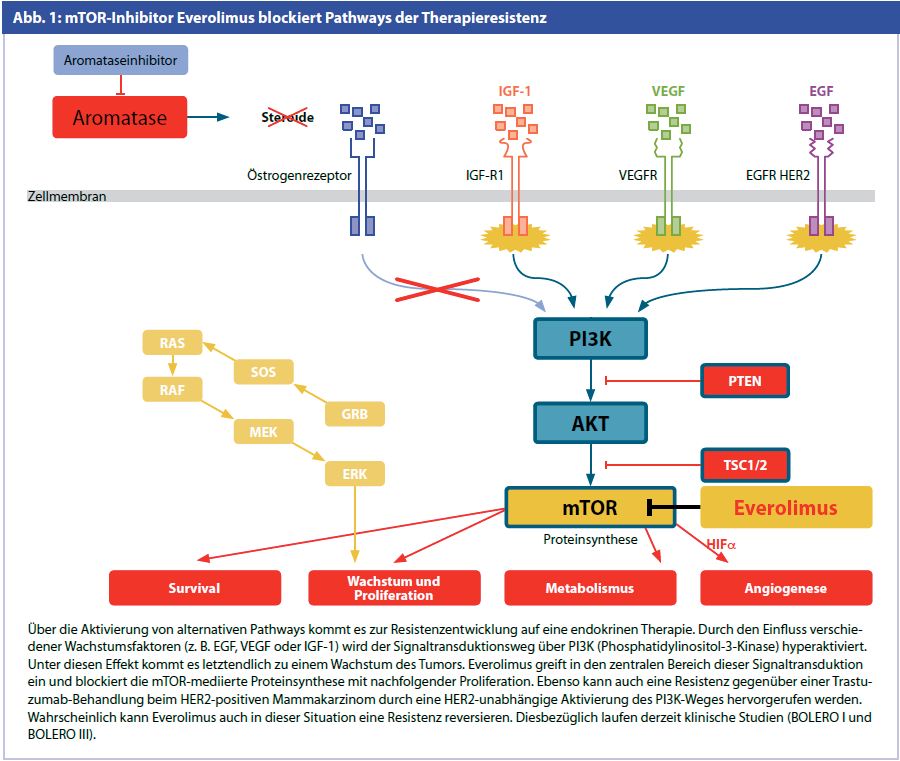
Komponenten der davor liegenden Signaltransduktionswege von mTOR sind in malignen Zellen häufig dereguliert. Im Gegensatz dazu ist das mTOR-Protein selbst selten verändert. Aus diesem Grund stellt dieses Molekül ein stabiles Ziel zur Beeinflussung von wichtigen und unterschiedlichen Signalwegen bei Krebs dar. Verschiedene Mutationen und/oder Genamplifikationen verursachen in der malignen Zelle Signale, die den wachstums- und proliferationsstimulierenden Hebel im mTOR-Signalweg umlegen. Gesteigerte mTOR-Aktivität führt zu einer vermehrten Proteinsynthese durch Gene, die Wachstum, Zellmetabolismus und Überleben von Krebszellen vermitteln. Das mTOR-System steht in direkter und indirekter Verbindung mit Rezeptoren für Wachstumsfaktoren an der Oberfläche von Krebszellen wie EGFR, HER2 und IGF-1R, die beim Mammakarzinom eine wesentliche Rolle spielen (Abb. 1). Ebenso sind Rezeptoren innerhalb der Tumorzelle sowie Steroidrezeptoren (z. B. Östrogenrezeptoren) in die Aktivierung von mTOR involviert („intracellular signaling“). Aktivierende Mutationen in Onkogenen wie z. B. Ras („gain of function“) oder funktionsvermindernde Mutationen in Tumorsuppressorgenen wie PTEN („loss of function“) können zur Aktivierung von mTOR führen. Die drei in Krebszellen am häufigsten hyperaktivierten oder hyperaktiven „upstream“ von mTOR gelegenen Signalwege sind der PI3K/Akt-, der Proteinkinase-C-(PKC)- und der Mitogen-aktivierte-Proteinkinase-(MAPK)/Ras-Signalweg. Die durch Wachstumsfaktoren und Rezeptoren regulierten Signalwege führen zur Aktivierung von mTOR und nachfolgend zur Produktion einer Reihe von Schlüsselproteinen: So hat mTOR erstens einen Einfluss auf die Translation der mRNA für Cycline (Cyclin D), wodurch die Aktivität der Cyclin-abhängigen Kinasen (CDKs) beeinflusst wird, die den Zellzyklus steuern. mTOR fungiert daher sozusagen als „Kontrollorgan“ für den Zellzyklus. Zweitens ist mTOR in den Aminosäure- bzw. Glukosetransport involviert. Krebszellen haben teilweise durch einen erhöhten Metabolismus einen vermehrten Bedarf an Energie. Und zum Dritten induziert mTOR die Angiogenese, die besonders über die Produktion von HIF-1a und in der Folge von Vascular Endothelial Growth Factor (VEGF) durch Krebszellen gesteuert wird. Gefäßbildung ist für die Ernährung, das Wachstum und die Metastasierung von Krebszellen eine wesentliche Voraussetzung (siehe Abb. 1).
Klinischer Einsatz von Everolimus
Inhibition von mTOR bei endokriner Resistenz des Mammakarzinoms: Ungefähr 30–40 % der Östrogenrezeptor-positiven Brustkrebserkrankungen weisen eine primäre (intrinsische) Resistenz gegen Tamoxifen auf und können überhaupt nicht von diesem Medikament profitieren. Entweder besteht eine intrinsische (primäre) Resistenz gegen die endokrine Therapie (Tamoxifen, Fulvestrant oder Aromataseinhibitoren) oder es kommt im Laufe der Zeit zu einem Versagen der endokrinen Therapie (sekundäre oder erworbene Resistenz). Ein gemeinsames Merkmal von Brustkrebszellen, die auf endokrine Therapien resistent sind, ist die Überaktivierung von Signaltransduktionskaskaden, die es den Tumorzellen offenbar ermöglicht, der Wirkung der endokrinen Therapie zu entgehen. Typisch hierbei ist vor allem die Aktivierung des PI3-Kinase-AktmTOR- Signalwegs (siehe Abb. 1). Daraus ergibt sich die Hypothese, dass mTOR-Inhibition ein sinnvoller Ansatz in der Therapie des Hormonrezeptor-positiven Mammakarzinoms ist und eine Möglichkeit darstellt, endokrine Resistenzen zu überwinden. Somit stellt die Kombination einer endokrinen Therapie (z. B. Aromataseinhibitor) mit dem mTOR-Inhibitor Everolimus eine sinnvolle Option für diese Situation dar.
Die Kombination aus Letrozol und Everolimus wurde erstmals im Rahmen einer Phase-II-Studie im neoadjuvanten Setting untersucht. 270 Patientinnen wurden randomisiert und erhielten entweder Letrozol + Placebo oder Letrozol + Everolimus als neoadjuvante Therapie. Die Ansprechrate wurde mittels klinischer Palpation beurteilt und war im Everolimus- Arm signifikant besser. Ebenso war eine deutlichere Abnahme der Tumorzellproliferation (ki67) unter Everolimus zu beobachten.
Die ersten Ergebnisse in Bezug auf Verbesserung des progressionsfreien Überlebens durch die Überwindung der endokrinen Resistenz lieferte dann die TAMRAD-Studie. In der Phase- II-Studie verbesserte Everolimus/Tamoxifen die Clinical-Benefit- Rate gegenüber Tamoxifen allein (61,1 vs. 42,1 %) und verlängerte das progressionsfreie Überleben signifikant. Dabei war das Ergebnis bei sekundärer (erworbener) Resistenz auf Aromatasehemmer deutlich besser als bei primärer (intrinsischer) Resistenz. Im Kombinationsarm konnte eine 61%ige Rate mit klinischem Benefit erzielt werden im Vergleich zu 42 % im Tamoxifen-Monotherapiearm. Die Everolimus-Kombination zeigte sich auch hinsichtlich der Zeit bis zur Progression (p = 0,0026) sowie der Gesamtüberlebenszeit (p = 0,0019) signifikant überlegen. Durch die gute Verträglichkeit von Everolimus kann diese Kombination als wesentlicher Fortschritt in der Therapie des endokrin resistenten Mammakarzinoms betrachtet werden.
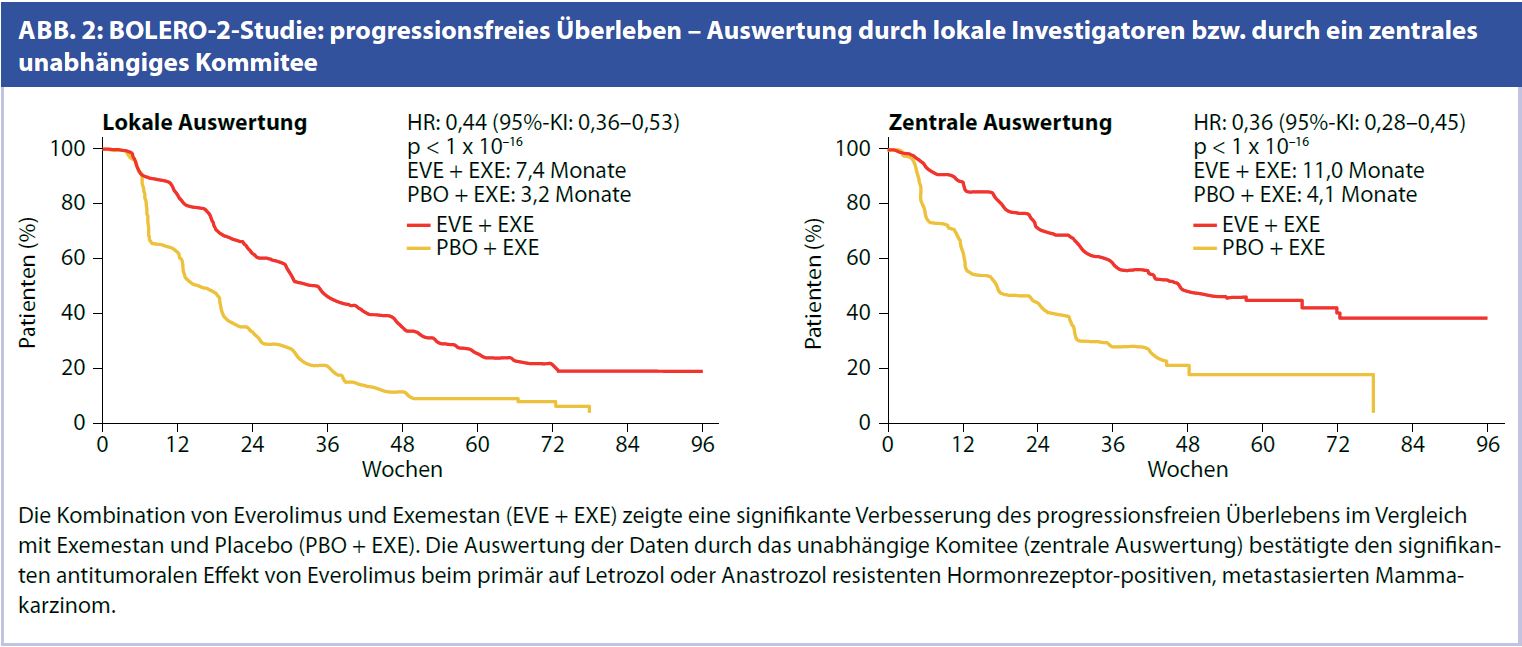
Im Dezember 2011 wurden dann die Ergebnisse der BOLERO-2-Studie in San Antonio präsentiert und gleichzeitig im „New England Journal of Medicine“ publiziert. Die Phase-IIIStudie BOLERO 2, die Exemestan plus Everolimus oder Placebo bei postmenopausalen Frauen mit Resistenz gegen Anastrozol oder Letrozol untersuchte, konnte frühzeitig abgebrochen werden, weil der primäre Endpunkt erreicht war. In der Auswertung durch die Studienärzte war das progressionsfreie Überleben (PFS) im Kombinationsarm mehr als verdoppelt gegenüber Exemestan allein (7,4 vs. 3,2 Monate). Die unabhängige zentrale Auswertung bestätigte den signifikanten progressionsverzögernden Effekt des mTOR-Inhibitors (PFS 11 vs. 4,1 Monate) (siehe Abb. 2). Everolimus reduziert das Progressions- und Sterberisiko um 57 %. Es wurden in BOLERO 2 keine anderen Nebenwirkungen als in anderen Indikationen beobachtet. Die am häufigsten aufgetretenen Nebenwirkungen Grad 3/4 waren Stomatitis (7,7 %), Anämie (5,8 %), Dyspnoe (3,9 %), Hyperglykämie (4,3 %), Müdigkeit (3,7 %), nicht-infektiöse Pneumonitis (3,1 %) und eine Erhöhung von Leberenzymen (3,1 %).
Inhibition von mTOR bei Resistenz gegenüber Trastuzumab: Ähnlich wie bei der Resistenzdurchbrechung bei endokriner Therapie und Everolimus wurde versucht, mittels Everolimus die Resistenz bei Patienten mit metastasiertem Mammakarzinom auf eine Trastuzumab-basierte Therapie zu durchbrechen. Rationale hierfür ist, dass es durch den Verlust des Tumorsuppressorgens PTEN zu einer Aktivierung von Akt/mTOR kommt, was eine Resistenz auf Trastuzumab mediiert. Diese Hypothese wurde bereits im Rahmen einer klinischen Phase-I/II-Studie überprüft. In dieser Studie wurde die Kombination von Everolimus und Trastuzumab bei HER-positiven Patientinnen, welche auf Trastuzumab resistent geworden sind, untersucht. Durch die gemeinsame Gabe von Trastuzumab und Everolimus (47 Pat.) konnte ein deutlicher klinischer Benefit erreicht werden.
Derzeit wird diese Kombination im Rahmen der Phase-III-BOLERO-1-Studie (Everolimus in Kombination mit Trastuzumab und Paclitaxel) beim metastasierten Mammakarzinom untersucht. Die BOLERO-3-Studie rekrutiert derzeit Patientinnen mit HER2-positiven Mammakarzinom, um die Wirksamkeit von Everolimus in Kombination mit Trastuzumab und Vinorelbin zu beurteilen.
ZUSAMMENFASSUNG: Seit Einführung der HER2-gerichteten Therapie mit Trastuzumab oder Lapatinib bzw. deren Weiterentwicklung in Form von Pertuzumab ist die Inhibition des mTOR-Signalwegs ein neuer Meilenstein in der Therapie des Mammakarzinoms. Everolimus ist eine relativ gut verträgliche orale Therapie, welche erwiesenermaßen die Resistenz gegenüber endokrine Therapie beim metastasierten Mammakarzinom umkehren kann. Die große Herausforderung in der Zukunft wird sicherlich die Etablierung von Studien sein, die das Potenzial einer mTOR-Inhibition in der adjuvanten Situation untersuchen sollten.