Mangel als kausaler Faktor, Substitution als präventive und therapeutische Chance – Sexualhormone und Osteoporose
Perimenopausales “Prophylaxe-Fenster”
Tatsächlich wird das Thema Knochengesundheit sowohl von den internistischen OsteologInnen als auch von den GynäkologInnen in der täglichen Praxis aufgegriffen. Allerdings herrscht Dissens zwischen diesen beiden Fachrichtungen. Während nämlich von Seiten der Gynäkologie traditionell, und insbesondere auch in Bezug auf die Knochengesundheit, präventivmedizinische Überlegungen im Vordergrund stehen, wird es von den internistischen Osteologen als ausreichend angesehen, bei Nicht-Risikopatientinnen erst ab dem 65. Lebensjahr mit Knochendichtemessungen zu beginnen, also in einem Lebensalter, in dem manche Frauen bereits Frakturen erlitten haben. Dabei liegt der viel interessantere Lebensabschnitt zwischen etwa dem 50. und dem 60. Lebensjahr, da im Laufe dieser 10 Jahre nachweislich die meiste Knochenmasse verloren geht. Deshalb sollten wir FrauenärztInnen die Vorsorgemaßnahmen in Bezug auf Knochengesundheit, insbesondere auf dieses zeitliche “Window of Opportunity” fokussieren. Denn hat sich einmal die Osteoporose etabliert, so ist sie nicht nur mit erhöhter Frakturgefahr assoziiert, sondern es werden viele andere Körperfunktionen, von denen man gar nicht annehmen würde, dass der Knochen an deren Aufrechterhaltung maßgeblich beteiligt ist, beeinträchtigt.
Konsequenzen über die Frakturgefahr hinaus
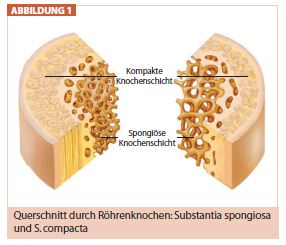
Der Knochen besteht aus dem Kortex (dieser macht in etwa 20% der Knochenmasse aus) und aus der Spongiosa, wo sich die Osteoporose zuerst manifestiert (Abb. 1).
Schwindende Stammzellreserve: Ein Verlust der Spongiosa in der zweiten Lebenshälfte geht im Übrigen mit Verlust von Immunität einher, weil sich durch die Abnahme des Knochenmarks, der Sitz der Hämatopoese, auch die Anzahl der natürlichen Killerzellen, der Neutrophilen und naiven B-Zellen reduziert.
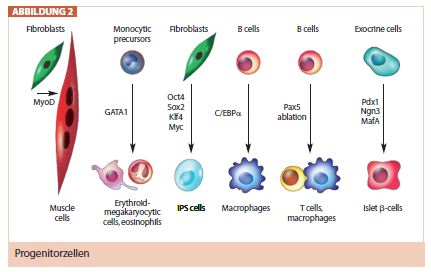
Im Knochenmark sind mononukleäre Stammzellen beheimatet, die auf Lockruf von Zytokinen (z. B. VEGF) mobilisiert werden, um nach einem akuten Herzinfarkt oder bei chronisch-ischämischer Herzmuskelschwäche die Herzleistung zu verbessern. Diese Progenitorzellen bewirken ein Remodelling der Herzmuskelzellen, können sich aber auch zu Gefäßzellen (Endothelzellen) differenzieren und unterstützen auf diese Weise dank der Neubildung von Blutgefäßen die kardiale Regeneration (Abb. 2). Mit Reduktion der Spongiosa bei Osteoporose schwindet die Zahl der Stammzellen und somit nimmt diese regenerative Funktion ab.
Metabolische Destabilisierung: Wie in einer Publikation in “Cell” 2007 nachgewiesen wurde, ist der Knochen weiters ein Produzent des Blutzucker-regulierenden Hormons Osteokalzin, das die Zahl der Betazellen im Pankreas erhöht und somit für die Erhöhung des Insulins und des Adiponektins verantwortlich ist. Frauen, bei denen in jungen Jahren, z. B. aufgrund von Anorexie, Knochenmasse (insb. Spongiosa) verloren gegangen ist, haben somit nachweislich mehr metabolische Probleme, z. B. mit Entgleisung des Kohlenhydratstoffwechsels in späteren Jahren.
Sexualhormonschutz für den Knochen
Nun ist der Knochen nicht nur selbst ein Hormonbildner, wir wissen aus der klinischen Praxis, dass der Knochen auch sehr empfindlich auf Hormonmangel reagiert; in diesem Zusammenhang seien die Östrogene und Testosteron angeführt, denen beiden eine zentrale Rolle im Knochenstoffwechsel zukommt:
Östrogene
-
bewirken die Differenzierung von Osteoblasten aus Knochenmarkstromazellen
-
hemmen die Apoptose von Osteoblasten und Osteozyten
-
steigern die Bildung osteoblastischer Wachstumsfaktoren (IGF-1, TGF-β)
-
und die Synthese von Prokollagen
Die Östrogene spielen weiters eine essenzielle Rolle in der Regulation der Osteoklasten: Sie unterdrücken die RANKL-Bildung und stimulieren die Osteoprotegerin-(OPG)-Produktion, womit ihnen eine Hemmung der Osteoklastenaktivität zukommt. Auch verschiedene Knochen-resorbierende Zytokine stehen unter dem hemmenden Einfluss der Östrogene. Und nicht zuletzt bewirken die Östrogene eine vermehrte Apoptose der Osteoklasten. Der Wegfall der Östrogene in der Postmenopause ist Ursache für das Auftreten der postmenopausalen Osteoporose.
Testosteron spielt eine Rolle in der Knochenneubildung und hat außerdem einen antiresorptiven Effekt. Im Übrigen kommt der Aromatase im Rahmen der Umwandlung von Testosteron in Östrogene eine wichtige Rolle in Bezug auf die Aufrechterhaltung der Knochendichte zu.
Ätiologische Paradigmen der Östrogenmangel-Osteoporose
Hypogonadismus der Frau: Prämenopausale Frauen mit Östrogenmangel haben eine signifikant niedrigere Knochendichte als Frauen mit normaler Ovarialfunktion, als Folge von Hypogonadismus entwickelt sich eine sekundäre Osteoporose. In diesen Fällen besteht dringend die Indikation zur Östrogensubstitution.
Nach der Menopause ist der Östrogenmangel hauptverantwortlich für die Abnahme der Knochendichte und somit für die erhöhte postmenopausale Frakturinzidenz. Der positive Effekt einer Hormonersatztherapie auf den Surrogatparameter Knochendichte und zur Primärprophylaxe osteoporotischer Frakturen ist durch eine Vielzahl randomisierter Studien belegt. Nicht zuletzt hat auch die WHI-Studie eine signifikante Senkung des Frakturrisikos (Oberschenkelhals- und Wirbelkörperfrakturen) bei substituierten Frauen gezeigt. Aus diesen Gründen ist eine peri- und frühe postmenopausale Östrogensubstitution nach wie vor zur Prävention (und gegebenenfalls auch Therapie) einer Osteoporose indiziert.
Aromatasehemmer-Therapie: Besondere Bedeutung kommt der adjuvanten, antihormonellen Behandlung des Hormonrezeptor- positiven Mammakarzinoms mit Aromatasehemmern (AI) bei der postmenopausalen Frau zu. Die Aromatasehemmer der 3. Generation (Anastrozol, Exemestan, Letrozol) bewirken eine fast vollständige Suppression der endogenen Östrogen- Bildung und führen durch Aktivierung der Knochenresorption zu einer Abnahme der Knochendichte mit konsekutiv erhöhter Frakturgefahr. Insbesondere in Abhängigkeit von weiteren Risikofaktoren ist bei diesen Patientinnen eine antiresorptive Therapie mit Bisphosphonaten bzw. aktuell auch mit Denosumab indiziert.
Zusammenfassend ist festzustellen, dass Osteoporose in jedem Lebensalter eine Behandlungsindikation darstellt, da sie mit hoher Morbidität verbunden ist. Den Sexualsteroiden kommt eine zentrale Rolle in Bezug auf die Knochengesundheit zu, ein Hormonmangel kann Ursache für das Auftreten einer Osteoporose sein. Insbesondere bei Fällen von Hypogonadismus in der Prämenopause sollte, wenn keine Kontraindikation vorliegt, eine Hormon-Substitution zur Prävention der Osteoporose durchgeführt werden.