Konservative Myomtherapie
Bei Ulipristalacetat (UPA; Esmya®) handelt es sich um einen sog. selektiven Progesteron-Rezeptor-Modulator (SPRM). Diese Substanzgruppe, deren bekanntester Vertreter Mifepriston ist, weist sowohl agonistische als auch antagonistische Eigenschaften am Progesteronrezeptor auf und wurde in verschiedenen klinischen Studien bei dysfunktionellen Blutungen, Endometriose und in der Notfallkontrazeption untersucht. Die Rolle des Progesterons bei Myomen hat auch dazu geführt, dass UPA zur Behandlung bei Uterus myomatosus eingesetzt wurde und mittlerweile die Zulassung zur präoperativen Therapie erhalten hat.
PEARL I
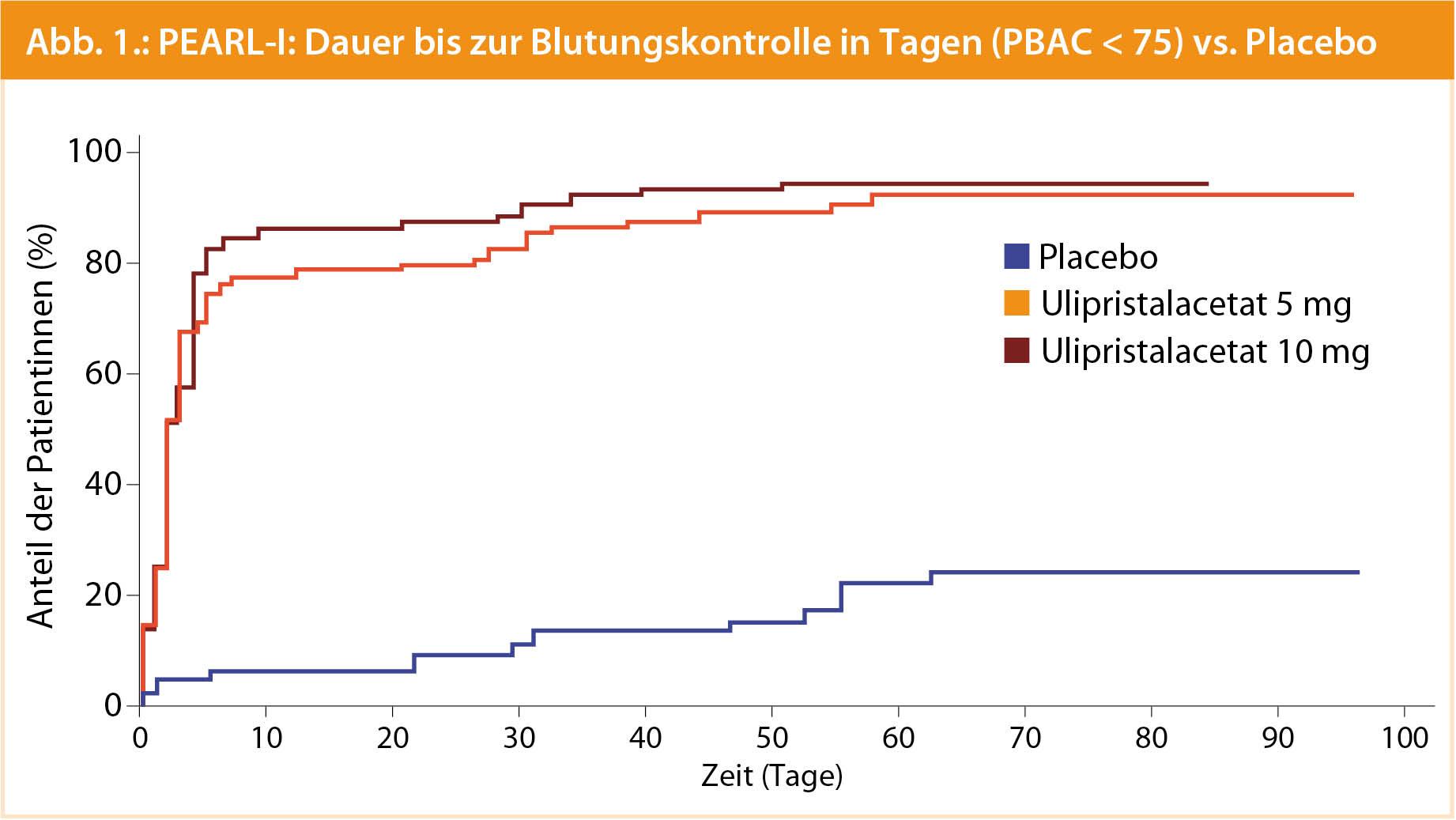
In zwei multizentrischen, randomisierten und doppelblinden Studien1,2, an denen auch unsere Abteilung beteiligt war, wurde zunächst die Wirksamkeit von UPA gegenüber Placebo (PEARL-I-Studie) untersucht. Diese Studie sollte die Wirksamkeit in der Behandlung von symptomatischen Myomen bei Frauen mit starken, zur Anämie führenden Menstruationsblutungen belegen. Über einen Zeitraum von 3 Monaten wurden täglich 5 mg oder 10 mg UPA mit Placebo – bei gleichzeitiger Gabe von Eisen in allen drei Gruppen – verglichen.
Starke Blutungen normalisierten sich in mehr als 90 % aller Patientinnen unter UPA statistisch signifikant häufiger als unter Placebo (Abb. 1) und die Mehrzahl der Patientinnen entwickelte eine Amenorrhö. Im Vergleich dazu konnte eine Blutungskontrolle in lediglich 19 % der Placebogruppe erreicht werden (p < 0,001). Darüber hinaus wurde eine Reduzierung des Myomvolumens erreicht.
PEARL II
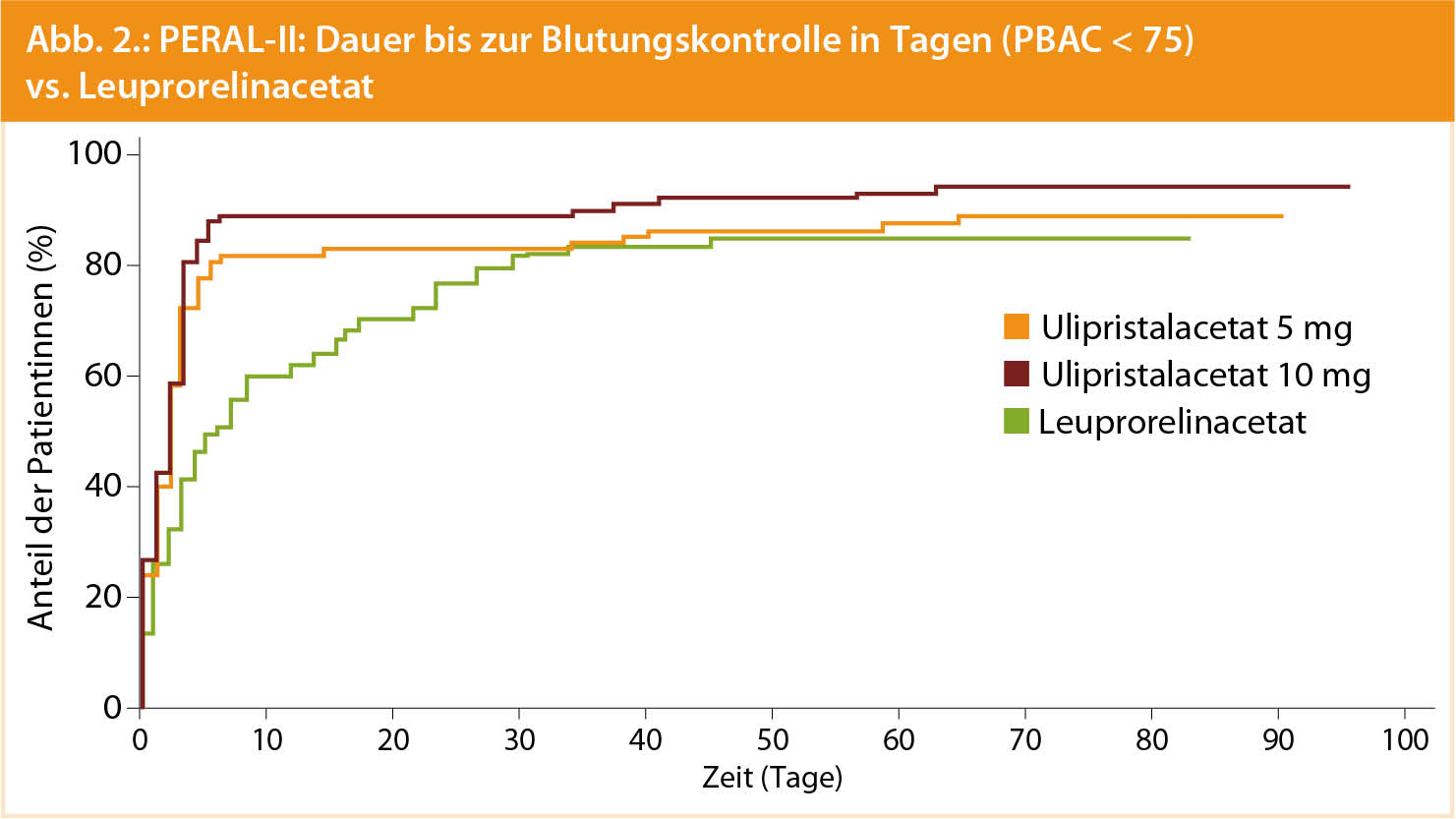
In der PEARL-II-Studie wurde UPA 5 mg mit einem GnRH-Analogon (Leuprorelinacetat 3,75 mg) verglichen. Auch hier erfasste man die Blutungen mit Hilfe eines semiquantitativen Fragebogens, der die Menge der benutzten Binden und Tampons sowie deren Durchblutungsgrad erhob (Pictorial Bleeding Assessment Chart – PBAC). In dieser Studie konnte die Gleichwertigkeit der Behandlung zu dem GnRH-Analogon bewiesen werden. Die Blutungskontrolle unter UPA wurde allerdings wegen des fehlenden Flare-up-Effekts rascher als mit dem GnRH erreicht, das etwa 25 Tage benötigte (Abb. 2).
In der Pearl-II-Studie, in der nur das Volumen der drei größten Myome gemessen wurde, zeigte sich UPA zum GnRH als praktisch gleichwertig mit einer Größenreduktion von 36 % (5 mg) und 42 % (10 mg) im Vergleich zu 53 % (GnRH). Die Reduktion des Myomvolumens wurde mit UPA allerdings auch nach Therapieende beibehalten, während beim GnRH die Volumenreduktion nach 6 Monaten fast gänzlich aufgehoben war.
Fazit
Die Lebensqualität der Patientinnen unter UPA verbesserte sich und erreichte in einem myomspezifischen Fragebogen Werte, die denen von gesunden Frauen gleichzusetzen sind.
Da es im Unterschied zur GnRH-Anwendung mit UPA zu keinem Absinken des Östrogenspiegels kommt, waren auch kaum klimakterischen Beschwerden zu verzeichnen. In der Vergleichsstudie mit GnRH bestanden mäßige bis starke Hitzewallen bei ca. 10 % der UPA und ca. 40 % der GnRH-Patientinnen (p < 0,001).
UPA war generell gut verträglich; es kam allerdings in ca. 60 % der UPA-Fälle zu einer benignen Endometriumveränderung (PRM-associated Endometrial Change – PAEC), die histologisch durch eine geringe mitotische Aktivität von Drüsen und Stroma sowie zystisch dilatierte Drüsen imponiert. Diese bisher nicht gekannte histologische Endometriumveränderung ist in praktisch allen Fällen nach Ende der UPA-Therapie reversibel.
Mit der neuen Behandlungsoption Esmya® (5 mg oral pro Tag, max. 3 Monate) eröffnen sich in der konservativen Intervention neue Wege: rasche Blutungskontrolle bei myombedingter Hypermenorrhö in Kombination mit einer Verkleinerung der Myome.