Neue Operationsmethoden bei Brustkrebs – Skin- und Nipple-Sparing, Lipofilling
Im Laufe der Zeit hat sich die Behandlung des Brustkrebs weg von einer operativ dominierten Behandlung hin zu einer Gesamtbehandlung unter Berücksichtigung aller Therapiemodalitäten wie Chemotherapie, Strahlentherapie, physikalische Therapie und psychologische Betreuung entwickelt. Um diesem umfassenden Behandlungsschema ein entsprechendes Forum bieten zu können, wurden an vielen Abteilungen so genannte Brustzentren etabliert.
Als Mitglied des Brustgesundheitszentrums Tirols und Leiter des Brustteams der Universitätsklinik für Plastische, Rekonstruktive und Ästhetische Chirurgie Innsbruck möchte ich Ihnen einen kleinen Einblick in die operative Behandlung und Rekonstruktion bei Brustkrebspatientinnen geben.
Brusterhaltende Therapie
Um als Brustgesundheitszentrum zertifiziert zu werden, sollte die entsprechende Abteilung heutzutage eine brusterhaltende Therapierate von 80 % erreichen, dies bedeutet, dass bei 80 % der Patientinnen eine Therapie mit Tumorektomie und nachfolgender Bestrahlung möglich sein sollte. Dies wird durch die heutzutage sehr frühzeitige und exakte Diagnostik gut unterstützt. Bei entsprechendem Größenverhältnis von Tumor zur Brust beziehungsweise insgesamt einem kleinen Tumor kann meist eine alleinige Tumorektomie erfolgen. Sollte die Relation Tumor zur Brust jedoch ungünstig sein und eine deutlich ausgedehntere Tumorektomie bis hin zu einer Quadrantenresektion notwendig sein, ist die Verwendung von onkoplastischen Techniken notwendig. Auch durch ungünstige Lage des Tumors kann es notwendig sein, onkoplastische Techniken einzusetzen. Der Begriff „onkoplastische Chirurgie“ wurde 1998 durch Prof. Dr. Audretsch1 bekannt gemacht. Hier werden die Prinzipien der onkologischen Chirurgie und der plastischen Chirurgie kombiniert, um sowohl ausreichende onkologische Sicherheit als auch ein ästhetisch ansprechendes Resultat nach Tumorektomie zu erreichen.
Die onkologische Sicherheit konnte in zahlreichen Studien bis zu einer Tumorgröße von 5 cm in Kombination mit postoperativer Strahlentherapie nachgewiesen werden.2 Ein besonderes therapeutisches Problem stellen in diesem Sinne zentrale Tumoren dar, die zu einer Mitentfernung des Nippel-Areola-Komplexes führen. Die Therapievarianten reichen hier von einfacher Gewebemobilisierung und querer Naht über eine zentrale Tumorektomie, welche in den beiden unteren Quadranten nach medial und lateral extendiert wird und anschließend mit einer Inverted-T-Narbe verschlossen werden kann. Diese Verschlusstechnik entspricht schon in etwa dem operativen Vorgehen im Rahmen einer Mammareduktion. Als weitere Technik bietet sich eine an die periareoläre Bruststraffung nach Benelli angelehnte Technik wiederum mit zentraler Mobilisation und Verschluss des zentralen Defektes mit einer Tabakbeutelnaht an. Bei entsprechender Brustgröße beziehungsweise Ptose können auch Verschlusstechniken angelehnt an die „Inferior-based Pedicle“-Technik verwendet werden, wobei es zu einer sofortigen Rekonstruktion der Areola aus Brusthaut aus dem unteren Brustanteil kommt. Auch hier kommt es letztlich zu einer T-förmigen Narbe. Eine weitere Technik stellt der sogenannte Grisotti-Lappen dar, welcher eher aus dem unteren medialen Anteil kommt und letztlich zu einer L-förmigen Narbe führt. Auch hier wird die Areolahaut aus dem unteren Anteil der Brusthaut sofort rekonstruiert.3
Zusammenfassend kann gesagt werden, dass für die Techniken mit einer sofortigen Rekonstruktion der Areola und T- oder L-förmigen Narben eine gewisse Ptose der Brust, welche den dafür notwendigen Hautüberschuss bereitstellt, notwendig ist. Ein großer Vorteil bei diesen Techniken liegt darin, dass auch die kontralaterale Brust in entsprechender Weise bei gleichem Narbenbild verkleinert und angeglichen werden kann. Man sollte bei Verwendung dieser Techniken jedoch nicht vergessen, dass aufgrund des histopathologischen Befundes unter Umständen eine Nachresektion beziehungsweise bei ausgedehnteren Fällen sogar ein Umstieg auf eine Skin-sparing-Mastektomie notwendig sein kann.
Skin-sparing-Mastektomie
Die Skin-sparing-Mastektomie, welche eine Entfernung der gesamten Brustdrüse unter Erhalt des Hautmantels bedeutet, stellt heute laut den S3-Leitlinien den State of the Art in der nicht brusterhaltenden Tumortherapie dar. Derzeit in Diskussion steht die Weiterentwicklung im Sinne der Nipple-sparing-Mastektomie, welche durch die starke Zunahme der prophylaktischen Mastektomien sowie von den Patienten gefordert wird. Große Studienserien von Maurizio Nava aus dem Tumorzentrum in Mailand oder auch Arbeiten vom Memorial Sloan-Kettering Cancer Center in New York bestätigen die onkologische Sicherheit der Nipple-sparing-Mastektomie.4 Aus ästhetischen Gründen ist die Nipple-sparing-Mastektomie auf jedem Fall zu favorisieren. Die Durchführung einer Skinsparing-oder Nipple-sparing-Mastektomie bedingt normalerweise eine Sofortrekonstruktion der Brust entweder mit Eigengewebe oder mit Expander beziehungsweise Prothese. Zum Eigengewebe kann gesagt werden, dass hier nach wie vor eigentlich der Unterbauchlappen State of the Art ist, wobei dieser heutzutage fast nur noch in seiner Perforatorvariante als so genannter DIEP-Lappen verwendet wird. Hierbei werden nur noch die Blutgefäße aus dem Musculus rectus auspräpariert und nicht mehr ein Teil des Muskels mitentnommen. Eine ebenfalls noch relativ neue Rekonstruktionsvariante stellt der so genannte TMG-Lappen, der transverse myokutane Grazilislappen, dar, welcher von der Oberschenkelinnenseite entnommen wird und insbesondere bei schlanken Patientinnen seine Anwendung findet. Weitere technische Verbesserungen im Rahmen der Eigengewebsrekonstruktion haben sich durch die Verwendung von so genannten Couplersystemen für die Venenanastomose ergeben, welche einen großen Zeitgewinn darstellen und zusätzlich eine hohe rheologische Sicherheit aufweisen.
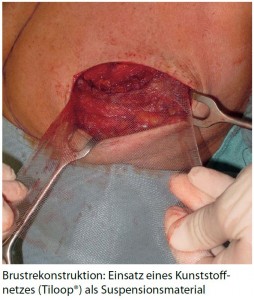 Weiters kann bei Anschluss an die Mammaria- interna-Gefäße heute auch interkostal angeschlossen werden, sodass eine Entfernung des Rippenknorpels nicht notwendig ist und hierdurch ebenfalls Zeit zu Gunsten der Patientin gespart werden kann. Die Alternative zur Eigengewebsrekonstruktion stellt die Rekonstruktion mit Expanderprothese beziehungsweise Expander dar. Hier stellt die Verwendung von Suspensionsmaterialien zwischen dem Unterrand des Musculus pectoralis und der Unterbrustfalte entweder in Form von Kunststoffnetzen (zum Beispiel Tiloop®; siehe Abb.) oder die Verwendung von azellulären dermalen Matrizes (zum Beispiel Strattice®, Protexa® oder Alloderm®) eine wichtige Neuerung dar.5 Durch Verwendung dieser Materialien kann auf eine komplette Muskelabdeckung der Prothese beziehungsweise des Expanders verzichtet werden. Man erhält eine bessere Kontrolle über die Implantatplatzierung und ebenso eine bessere Kontrolle über die Lage der Inframammärfalte. Die Expander können schon am Ende der Operation deutlich stärker vorgefüllt werden als früher, sodass das Ende der Expansionsphase für die Patientin mit weniger ambulanten Füllungen und insgesamt das Endergebnis schneller erreicht wird. Bis jetzt haben sich die Matrizes ihre Verwendung im Bezug auf Infektrate und bei Explantationsrate der früheren Methode zumindest ebenbürtig gezeigt bei einer eben deutlich schnelleren Expansionsrate.6 Wie auch die Arbeiten aus den USA nahelegen, könnten somit eventuell in Zukunft wieder die sofortige Verwendung der definitiven Prothese geplant werden, was zu einem deutlich höheren ästhetischen Ergebnis mit einer Kostenreduktion und einer deutlichen Kosten- und Morbiditätsreduktion für die Patientin einhergeht.
Weiters kann bei Anschluss an die Mammaria- interna-Gefäße heute auch interkostal angeschlossen werden, sodass eine Entfernung des Rippenknorpels nicht notwendig ist und hierdurch ebenfalls Zeit zu Gunsten der Patientin gespart werden kann. Die Alternative zur Eigengewebsrekonstruktion stellt die Rekonstruktion mit Expanderprothese beziehungsweise Expander dar. Hier stellt die Verwendung von Suspensionsmaterialien zwischen dem Unterrand des Musculus pectoralis und der Unterbrustfalte entweder in Form von Kunststoffnetzen (zum Beispiel Tiloop®; siehe Abb.) oder die Verwendung von azellulären dermalen Matrizes (zum Beispiel Strattice®, Protexa® oder Alloderm®) eine wichtige Neuerung dar.5 Durch Verwendung dieser Materialien kann auf eine komplette Muskelabdeckung der Prothese beziehungsweise des Expanders verzichtet werden. Man erhält eine bessere Kontrolle über die Implantatplatzierung und ebenso eine bessere Kontrolle über die Lage der Inframammärfalte. Die Expander können schon am Ende der Operation deutlich stärker vorgefüllt werden als früher, sodass das Ende der Expansionsphase für die Patientin mit weniger ambulanten Füllungen und insgesamt das Endergebnis schneller erreicht wird. Bis jetzt haben sich die Matrizes ihre Verwendung im Bezug auf Infektrate und bei Explantationsrate der früheren Methode zumindest ebenbürtig gezeigt bei einer eben deutlich schnelleren Expansionsrate.6 Wie auch die Arbeiten aus den USA nahelegen, könnten somit eventuell in Zukunft wieder die sofortige Verwendung der definitiven Prothese geplant werden, was zu einem deutlich höheren ästhetischen Ergebnis mit einer Kostenreduktion und einer deutlichen Kosten- und Morbiditätsreduktion für die Patientin einhergeht.
Lipofilling
Zuletzt möchte ich noch auf das Lipofilling eingehen, einer Methode, bei der an einer anderen Körperstelle abgesaugtes Fettgewebe in die Brust injiziert wird, um eine Augmentation beziehungsweise Asymmetrie oder auch eine durch eine Tumorektomie entstandene Konturdeformität zu beheben. Das Lipofilling wird in der plastischen Chirurgie seit über 40 Jahren angewandt, seit zirka 10 Jahren hat diese Technik ein deutliches Revival erlebt. Zahlreiche Studien konnten zeigen, dass sich das Lipofilling hervorragend eignet, um Konturdeformitäten bei Zustand nach Tumorektomie mit Eigengewebsrekonstruktion oder auch Prothesenrekonstruktion auszugleichen. Die Datenlage zur onkologischen Sicherheit ist nicht eindeutig, aber zahlreiche Publikationen vor allem aus Mailand legen auch die onkologische Sicherheit nahe. Auch von radiologischer Seite gibt es zahlreiche Publikationen über eine sichere Differenzierung des beim Lipofilling auftretenden Mikrokalks vom Mikrokalk eines Mammakarzinoms.7
Trotzdem gibt es Statements von großen Gesellschaften der plastischen Chirurgie wie zum Beispiel der amerikanischen oder der italienischen, welche empfehlen, aufgrund der noch nicht hundertprozentig sicheren Datenlage eine Verwendung bei Tumorpatientinnen nur bei Patientinnen durchzuführen, welche in Zentren behandelt werden und bei denen eine regelmäßige Nachkontrolle auch in Hinblick auf das Lipofilling erfolgen kann. Grundsätzlich wird die Injektion des Fettes diffus in die Brustdrüse abgelehnt und stattdessen empfohlen, einerseits dorsal der Drüse in den Brustmuskel zu injizieren beziehungsweise andererseits in den Subkutanbereich zu injizieren, um eine etwaige Interferenz mit dem Brustdrüsengewebe möglichst zu vermeiden.
- Audretsch W., Rezai M., Kolotas C. et al.: Tumor-specific immediate reconstruction in breast cancer patients. Perspect. Plast Surg 1998; 11:71
- Veronesi U., Cascinelli N., Mariani L. et al.: Twenty-year follow-up of a randomized study comparing breast-conserving surgery with radical mastectomy for early breast cancer. N Engl J Med 2002; 347:1227
- Huemer G.M., Schrenk P., Moser F. et al.: Oncoplastic Techniques Allow Breast-Conserving Treatment in Centrally Located Breast Cancers.Plast Reconstr Surg 2007; 120 (2):390-398
- de Alcantara Filho P., Capko D., Barry J.M. et al.: Nipple- sparing mastectomy for breast cancer and risk-reducing surgery: the Memorial Sloan-Kettering Cancer Center experience. Ann Surg Oncol 2011 Oct; 18 (11):3117-22
- Gurunluoglu R., Gurunluoglu A., Williams S.A. et al.: Current Trends in Breast Reconstruction: Survey of American Society of Plastic Surgeons 2010. Ann Plast Surg 2011 Aug 22
- Sbitany H., Serletti J.M.: Acellular Dermis-Assisted Prosthetic Breast Reconstruction: A Systematic and Critical Review of Efficacy and Associated Morbidity.Plast reconstr Surg 2011; 128 (6):1162-1169
- Spear S.L.; Al-Attar A.: Discussion: Mammographic Changes after Fat Transfer to the Breast Compared with Changes after Breast Reduction: A Blinded Study. Plast Reconstr Surg 2012; 129 (5):1039-1041

























































































