Nicht-chirurgische Prävention des Mammakarzinoms
Für das Mammakarzinom wurde eine Vielzahl potenziell präventiver Interventionen wissenschaftlich untersucht, womit Aussagen zur Wirksamkeit oder Unwirksamkeit möglich sind.
Diät
Diätetische Maßnahmen gehören zu den am häufigsten empfohlenen Maßnahmen zur Brustkrebsprävention. Rationale Grundlage dafür ist u. a. die mitogene Wirkung von Glukose und die in epidemiologischen Studien beschriebene Korrelation zwischen erhöhtem Gewicht, Body-Mass-Index (BMI), Hüftumfang und einer erhöhten Brustkrebsinzidenz, -morbidität und -mortalität.
Was nun konkret den Zusammenhang zwischen BMI und Brustkrebs betrifft, so kann aufgrund der vorliegenden Daten angenommen werden, dass postmenopausale Frauen mit einem BMI > 32 ein etwa 3-fach erhöhtes Lebenszeitrisiko für Brustkrebs haben.
Es ist angesichts dieser Zahl naheliegend anzunehmen, dass effektive Maßnahmen zur Optimierung des BMI auch das Brustkrebsrisiko reduzieren. Allerdings bedingt eine Reduktion des BMI nicht notwendigerweise auch eine Reduktion des Brustkrebsrisikos. Es ist z. B. durchaus denkbar, dass sowohl der BMI als auch die Brustkrebserkrankung eine oder mehrere gemeinsame Determinanten wie z. B. genetische Faktoren oder eine lebenszeitsensitive Schädigung/Protektion des Brustepithels durch Nahrungsbestandteile aufweisen, die durch eine BMI-Reduktion nicht beeinflussbar sind. Außerdem ist es durchaus denkbar, dass aufgrund der ethnisch heterogenen genetischen Brustkrebsentstehung diätetische Einflüsse durch Gen-Umwelt-Interaktionen die Entstehung von Brustkrebs nur in bestimmten Populationen beeinflussen.
Eine ganze Reihe von indirekten Hinweisen legt in bestimmten Populationen eine protektive Wirkung bestimmter Diäten auf das Brustkrebsrisiko nahe, so z. B. in mediterranen Ländern die typische lokale Diät, die reich an Kohlenhydraten und mehrfach ungesättigten Fettsäuren ist und einen geringen Anteil an Fleisch und tierischen Fetten aufweist. Auch eine fettarme, früchte- und gemüsereiche Diät wurde in unkontrollierten Studien an Brustkrebsüberlebenden mit einem reduzierten Rezidivrisiko assoziiert.
Im Gegensatz zur protektiven Wirkung einer Diät auf das Rezidivrisiko des Mammakarzinoms wurde aber bisher keine Diät identifiziert, die das Mammakarzinom auch primär verhindern kann. So konnte u. a. in einer retrospektiven Untersuchung an > 60.000 Frauen kein Zusammenhang zwischen einer fettarmen, fisch-, früchte- und gemüsereichen Diät und der Häufigkeit von Mammakarzinomen festgestellt werden.
Im Rahmen des Womens’ Health Initiative Diet Modification Trial wurde bei > 48.000 Frauen zwischen 50 und 79 Jahren der Einfluss einer fettarmen Diät (< 20 % Fettanteil; 5-mal täglich Früchte bzw. Gemüse) auf die Brustkrebsinzidenz untersucht. Nach 8 Jahren Beobachtungsdauer konnte auch in dieser Studie keine Reduktion der Mammakarzinom-Häufigkeit in der Interventionsgruppe nachgewiesen werden. Es ist also daher bis dato ungeklärt, ob und in welchem Ausmaß eine Diät tatsächlich zur Prävention des Mammakarzinoms eingesetzt werden kann.
Sport
Eine prospektiv-randomisierte Studie, die einen positiven Einfluss einer bestimmten Sportart auf das Mammakarzinomrisiko nachweist, existiert nicht. Allerdings weisen über 40 epidemiologische Studien darauf hin, dass sportliche Betätigung wahrscheinlich einen protektiven Einfluss auf die Entstehung des Mammakarzinoms hat. Danach ist eine sportliche Betätigung von mehreren Stunden pro Woche mit einer bis zu 66%igen relativen Risikoreduktion assoziiert. Eine einschlägige Untersuchung veranschlagt konkret den notwendigen Aufwand mit zumindest 160 Wochenstunden Sport pro Jahr. Eine weitere prospektive Kohortenstudie legt jedoch auch für die relativ wenig anstrengende und vielen Frauen zugängliche Sportart des forcierten Gehens (Nordic Walking) einen protektiven Einfluss nahe.
Aufgrund der Datenlage ist es wahrscheinlich sinnvoll, Frauen zur Brustkrebsprävention eine sportliche Betätigung im Ausmaß zwischen 3 und 5 Wochenstunden zu empfehlen.
Phytoöstrogene
Eine Reihe von epidemiologischen Studien belegt eine im Vergleich zu den USA und Europa geringere Prävalenz und Inzidenz von Mammakarzinomen in asiatischen Ländern. Phytoöstrogene wirken als natürliche selektive Östrogenrezeptormodulatoren (SERMs) mit einer etwa 150-fach geringeren Rezeptoraffinität als Östradiol sowie einer Selektivität für den Östrogenrezeptor beta. Es ist daher vorstellbar, dass Phytoöstrogene als kompetitive Antagonisten von Östradiol wirken und das Brustepithel vor proliferativen Stimuli schützen. Derzeit existiert aber keine prospektiv-randomisierte Studie, die den protektiven Einfluss von Phytoöstrogenen auch tatsächlich nachweist.
Eine mögliche Ursache für die Diskrepanz zwischen den epidemiologischen Daten und den negativen Ergebnissen von Untersuchungen zu Phytoöstrogensupplementen könnte darin liegen, dass nicht der kompetitiv-antagonistische Effekt von Phytoöstrogenen von Relevanz ist, sondern der östrogenagonistische Effekt in der Adoleszenz. Eine Stimulation des Brustepithels in der Adoleszenz führt zu einer lokalen Proliferation und damit eventuell zu einer höheren Resistenz gegenüber chemischen und physikalischen Noxen für die Dauer des restlichen Lebens. In Übereinstimmung mit dieser Hypothese stehen epidemiologische Daten aus Asien, die das Ausmaß der Phytoöstrogenkonsumation in der Jugend mit dem Brustkrebsrisiko korrelieren.
Aufgrund der derzeitigen Datenlage kann eine peri- oder postmenopausale Phytoöstrogentherapie zur Brustkrebsprävention jedenfalls nicht empfohlen werden.
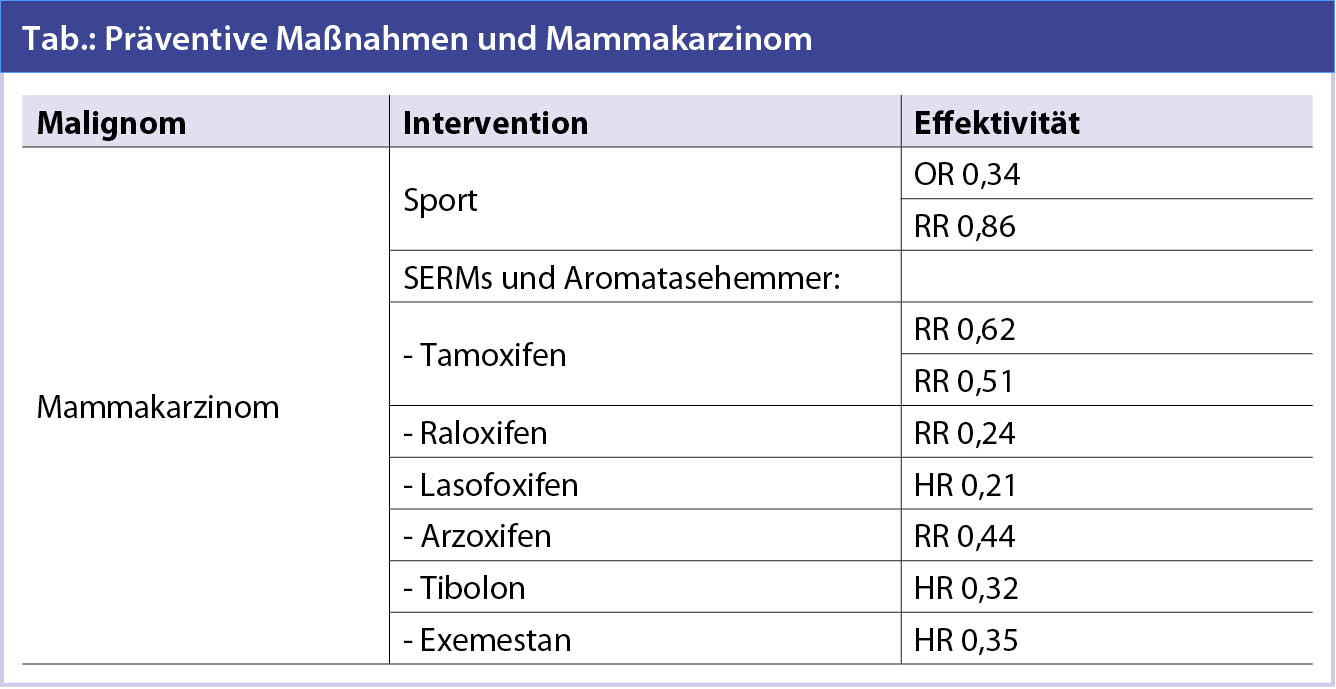
SERMs und Aromatasehemmer
Die SERMs Tamoxifen und Raloxifen sind zur Chemoprävention von Brustkrebs nachweislich geeignet. In einer Metaanalyse prospektiv-randomisierter Studien wurde eine 38%ige Reduktion der Mammakarzinominzidenz während einer 5-jährigen präventiven Therapie errechnet. Der Schutzeffekt ist auf Östrogenrezeptor- (ER) und/oder Progesteronrezeptor-(PR)-positive Mammakarzinome beschränkt. In dieser Gruppe von Mammakarzinomen beträgt die Reduktion 48 %. In der größten Präventionsstudie wurde durch Tamoxifen (20 mg pro Tag) eine Reduktion der Mammakarzinomhäufigkeit um 49 % erreicht. Die Reduktion der Inzidenz von Carcinomata in situ betrug 50 %. Die Teilnehmerinnen dieser Studie waren alle nach dem Gail-Modell (www.cancer.gov/bcrisktool/) als „Risikofälle“ definiert, d. h. sie wiesen ein 5-Jahres-Risiko > 1,67 % auf. Unerwünschte Nebenwirkungen unter Tamoxifen waren ein erhöhtes Risiko für Endometriumkarzinome, für Thrombosen und Katarakte. Hitzewallungen waren ebenfalls häufiger.
Die Ergebnisse der MORE-Studie (7.705 Frauen mit Osteoporose; Raloxifen 60 mg pro Tag versus Placebo) belegen, dass auch der präventive Einsatz von Raloxifen sinnvoll ist. Insgesamt führte die Einnahme von Raloxifen nach 4 Jahren zu einer 76%igen Reduktion des Auftretens von Mammakarzinomen. Dieser bemerkenswerte und klinisch überaus relevante Effekt von Raloxifen fand sich jedoch nur bei Frauen mit Serumöstradiolspiegeln > 10 pmol/l, während Frauen mit niedrigeren Serumspiegeln dieselbe Mammakarzinomhäufigkeit aufwiesen wie Frauen in der Placebogruppe.
Im direkten Vergleich zwischen Tamoxifen (20 mg pro Tag) und Raloxifen (60 mg pro Tag) wurde nach 81 Monaten Nachbeobachtungszeit ein signifikant stärkerer präventiver Effekt für Tamoxifen nachgewiesen. In der Raloxifengruppe waren allerdings signifikant weniger Nebenwirkungen festzustellen. Inzwischen wurde auch nachgewiesen, dass der protektive Effekt einer 5-jährigen Therapie mit Tamoxifen oder Raloxifen insgesamt für mindestens 8 Jahre anhält.
Tibolon, eine Substanz, die das Mammakarzinomrezidivrisiko erhöht, hat paradoxerweise bei älteren Brust-gesunden Frauen mit Osteoporose den gegenteiligen Effekt und reduziert signifikant das Mammakarzinomrisiko (relative Risikoreduktion 68 %). Dieser Effekt wurde in einer randomisierten Studie mit 5.438 postmenopausalen Frauen mit Osteoporose im Sinne eines sekundären Endpunktes nachgewiesen.
Aromatasehemmer: Neben SERMs sind auch steroidale und nicht-steroidale Aromatasehemmer zur Brustkrebsprävention geeignet. In der Adjuvanz führt Anastrozol im Vergleich zu Tamoxifen zu einer signifikanten Reduktion kontralateraler Mammakarzinome. Anastrozol wird derzeit in der IBIS-II-Studie als Chemopräventivum getestet. Ergebnisse liegen noch nicht vor. Ergebnisse für den steroidalen Aromatasehemmer Exemestan liegen hingegen bereits vor. In der NCIC-CTG-MAP.3-Studie wurde Exemestan (25 mg pro Tag) gegenüber Placebo bei 4.560 Frauen > 35 Jahre mit erhöhtem Brustkrebsrisiko getestet. Als erhöhtes Risiko galt in dieser Studie u. a. ein Alter > 60 Jahre und ein 5-Jahres-Mammakarzinomrisiko > 1,67 % nach dem bereits erwähnten Gail-Modell. Exemestan reduzierte gegenüber Placebo das Brustkrebsrisiko signifikant (65 % relative Risikoreduktion). Eine Einbuße an Lebensqualität war durch die präventive Einnahme von Exemestan nicht zu registrieren. Allerdings klagten vor allem prämenopausale Frauen häufiger über Östrogenentzugssymptome sowie Arthralgien und Muskelschmerzen.
Weitere Substanzen wie Lasofoxifen und Arzoxifen wurden ebenfalls in prospektiven, randomisierten Studien untersucht und wiesen eine mammakarzinompräventive Wirkung auf.
Sowohl Tamoxifen und Raloxifen als auch Tibolon, Exemestan, Lasofoxifen und Arzoxifen haben eine objektiv nachgewiesene mammakarzinompräventive Wirkung. Alle genannten Substanzen sind zwar wirksam, sind aber zur Mammakarzinomprävention nicht zugelassen.
Aspirin
Aspirin und Vitamine nehmen in der Prävention generell einen besonderen Stellenwert ein, da sie leicht erhältlich sind und von den meisten Menschen als grundsätzlich nebenwirkungsfrei eingeschätzt werden.
Experimentelle Arbeiten lassen darauf schließen, dass Aspirin und NSAIDs sich theoretisch zur Brustkrebsprävention eignen. Hauptangriffspunkt beider Substanzen ist das Enzym Cyclooxygenase (COX), von dem zumindest zwei Isoformen existieren: COX-1 und COX-2. Eine COX-2-Überexpression wurde in diversen Tumorgeweben nachgewiesen, u. a. auch im Mammakarzinomgewebe. Ebenfalls nachgewiesen wurde eine COX-2-abhängige lokale Induktion der Angiogenese sowie eine Induktion der lokalen Aromataseaktivität durch Prostaglandin E2 (PgE2) als Hauptmetabolit der COX-2. Beide Faktoren – eine Induktion der Angiogenese und eine Induktion der Aromataseaktivität und damit eine erhöhte parakrine Östradiolproduktion – sind als Tumorpromotoren bekannt. Eine medikamentöse Hemmung der COX-2 ist daher ein theoretisch valider Ansatz der Mammakarzinomprävention.
In einer Teilstudie der WHI wurde untersucht, ob die präventive Einnahme von 100 mg Aspirin jeden zweiten Tag die Gesamtkrebsinzidenz beeinflusst. Dies war nicht der Fall. Es wurde keine Reduktion der Gesamtkrebsinzidenz und auch keine Reduktion der Mammakarzinominzidenz beobachtet. Aspirin ist daher nach heutigem Wissensstand nicht zur Mammakarzinomprävention geeignet. Weitere randomisierte Studien, die den Einfluss von nicht-steroidalen Antirheumatika (NSAIDs) auf die Entstehung von Mammakarzinomen untersuchen, liegen zurzeit nicht vor. Allerdings scheint die Einnahme von Aspirin bei Frauen nach Mammakarzinom das Rezidivrisiko zu reduzieren, worauf eine Übersichtsarbeit epidemiologischer Studien hinweist.
Vitamine
Vitamin D: Im Rahmen der WHI wurde der präventive Effekt von 1.000 mg Calcium und 400 IE Vitamin D täglich über 7 Jahre gegenüber Placebo untersucht. In dieser Studie wurde die Rate an Mammakarzinomen (als sekundärer Endpunkt) nicht reduziert.
Vitamin E, Beta-Carotin: Eine Vitamin-E-Supplementierung führt laut vorliegenden Daten zu keiner Reduktion der Mammakarzinominzidenz. Dieser gilt in analoger Weise auch für Beta-Karotin.
Metformin
Die Einnahme von Metformin ist bei Diabetikern und Diabetikerinnen gegenüber anderen antidiabetischen Medikamenten mit einer geringeren Krebsinzidenz und Krebsmortalität assoziiert. In einer Metaanalyse von 11 einschlägigen Studien betrug die Reduktion etwa 30 % sowohl für die Krebsinzidenz als auch für die Krebsmortalität. Diese Assoziation zeigte sich bei beim Mammakarzinom. Ob ein mammakarzinompräventiver Effekt von Metformin tatsächlich existiert oder z. B. nur ein erhöhtes Risiko anderer Antidiabetika gegenüber Metformin besteht, kann dzt. nicht abschließend beantwortet werden. Aktuell wird untersucht, ob Frauen mit frühem Mammakarzinom von einer zusätzlichen adjuvanten Metformintherapie profitieren.
Statine
In einer Reihe von klinischen Studien wurde eine inverse Korrelation zwischen der Einnahme von Statinen und einem reduzierten Mammakarzinomrisiko registriert. So wurde z. B. in einer prospektiven, landesweiten Untersuchung an dänischen Frauen das Auftreten von Mammakarzinomen mit der Verschreibung von Statinrezepten korreliert. Simvastatin-Anwenderinnen hatten pro 100 Frauen und pro 10 Statin-Anwendungsjahren 10 Fälle weniger an Mammakarzinomen gegenüber Nicht-Simvastatin-Anwenderinnen. Ähnliche Resultate hinsichtlich hydrophoben, lipophilen Statinen wie Simvastatin, Fluvastatin und Lovastatin ergaben Untersuchungen in den USA. Allerdings existieren auch negative Studien und ein direkter präventiver Wirknachweis in prospektiv-randomisierten Studien fehlt bisher.