Zum Einfluss des Genotyps auf die endokrine Therapie des Mammakarzinoms – Tamoxifen und CYP2D6
Der selektive Östrogenrezeptor-Modulator (SERM) Tamoxifen spielt seit Jahrzehnten eine zentrale Rolle in der Behandlung des Rezeptor-positiven Mammakarzinoms. Trotz Einführung der Aromatasehemmer in der Therapie des postmenopausalen endokrin responsiven Mammakarzinoms ist Tamoxifen weltweit nach wie vor das meistrezeptierte Medikament zur Behandlung dieser Erkrankung. In den letzten 10 Jahren untersuchte eine Vielzahl von Studien den Einfluss der Pharmakogenetik auf den Metabolismus vom Tamoxifen und den damit verbundenen individuellen Unterschieden in seiner Wirksamkeit.
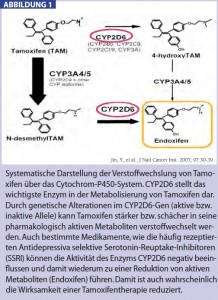
Metabolisierung von Tamoxifen – Stoffwechselprodukte sind die eigentlich wirksamen Substanzen: Tamoxifen hat eine relativ geringe Bindungsfähigkeit am Östrogenrezeptor und wird als „Prodrug“ bezeichnet. Verschiedene Cytochrom- P450-Enzyme (CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CAP3A4 und CYP3A5) katalysieren die Biotransformation von Tamoxifen in seine aktiven und inaktiven Metaboliten. CYP2D6 spielt eine dominante Rolle in der Produktion von 4-Hydroxy-Tamoxifen und Endoxifen (Abb. 1). Diese beiden Metaboliten haben eine zumindest 10-fach höhere Bindungsfähigkeit zum Östrogenrezeptor im Vergleich zu Tamoxifen. Die Konzentrationen von Endoxifen ist bei Patientinnen unter Tamoxifentherapie etwa 6–12-mal höher als die Plasmaspiegel von 4-Hydroxy-Tamoxifen. Dies legt den Schluss nahe, dass Endoxifen letztendlich der wichtigste Metabolit für die Wirksamkeit der endokrinen Therapie darstellt. Genetische Variationen, welche zu einer unterschiedlichen Expression von CYP2D6 führen, können somit zu einer reduzierten Endoxifenspiegeln führen.
Polymorphismus im CYP2D6-Genlocus: Bis dato wurde über 100 allelische Varianten von CYP2D6 identifiziert, welche zu veränderter Enzymaktivität führen können. Eine generell akzeptierte Klassifizierung bezeichnet für 2 Wildtyp-CYP2D6-Allele homozygote Individuen, wie CYP2D6 *1/*1, als extensive Metabolisierer (EM). Im Gegensatz dazu werden Personen mit einem oder zwei Allelvarianten mit reduzierter oder keiner enzymatischen Aktivität als intermediäre Metabolisierer (IM) bzw. schlechte („poor“) Metabolisierer (PM) bezeichnet. Eine Minderheit der Population trägt mehrere Genkopien der CYP2D6-Allele und werden aus diesem Grunde als ultrarapide Metabolisierer (UM) klassifiziert (Abb. 2).
Interaktion von CYP2D6 und Medikamenten: CYP2D6 spielt neben der Metabolisierung von Tamoxifen eine wichtige Rolle in der Metabolisierung von rund 25 % aller häufig verwendeten Medikamenten, wie zum Beispiel Analgetika (Tramadol, Codein), häufig verschriebene Antidepressiva (SSRIs) oder Antihypertensiva (Metoprolol). Menschen mit einer stark reduzierten Aktivität von CYP2D6 aufgrund des Genotyps („poor metabolizer“) zeigen vermehrt Nebenwirkungen auf diese Medikamente und/oder erhöhte Plasmaspiegel dieser Substanzen.
Aus diesem Grund fokussiert sich derzeit das Interesse in Bezug auf die Tamoxifentherapie beim Mammakarzinom auch zunehmend auf die ko-administrierte Medikation, inbesondere aufgrund der Tatsache, dass etwa 25 % aller Patientinnen mit Mammakarzinoms wegen depressiver Verstimmungen oder massiver Hitzewallungen Serotonin-Noradrenalin-Reuptake- Inhibitoren (SSRI/SNRI) verschrieben bekommen. Diese Antidepressiva haben die Fähigkeit, CYP2D6 in seiner Funktion zu inhibieren und im Endeffekt die Metabolisierung von Tamoxifen zu vermindern. Die gleichzeitige Gabe von Paroxetin bei Patientinnen unter Tamoxifen führte zu einer über 50%igen Reduktion der Spiegel des aktiven Metaboliten Endoxifen.
Effekt der CYP2D6-Genotyps auf das Brustkrebs-spezifische Überleben von Patientinnen unter Tamoxifen-Therapie: In den letzten 5 Jahren wurden mindestens 14 Studien veröffentlicht, welche einen Zusammenhang von CYP2D6-Genotyp und dem Überleben der Patientinnen unter Tamoxifentherapie zeigten. In diesen Zusammenhang konnte festgestellt werden, dass Patientinnen mit einem Poor-Metabolizer-(PM)- Genotyp niedrige Spiegel des aktiven Metaboliten Endoxifen aufweisen und damit im direkten Vergleich mit Patientinnen mit dem Wildtypgen eine schlechteres Überleben zeigen. Allerdings wurden im selben Zeitraum ungefähr die gleiche Anzahl von Studien publiziert, in denen kein Zusammenhang von Genotyp und Outcome gezeigt werden konnte.
Hitzewallungen und andere Tamoxifen-assoziierte Wirkungen: In einzelnen Untersuchungen konnte gezeigt werden, dass Patientinnen mit einem Extensive-Metabolizer-(EM)- oder Ultrarapid- Metabolizer-(UM)-Genotyp aufgrund höherer zirkulierender Endoxifenspiegel auch mit vermehrten endokrinen Nebenwirkungen in Form von Hitzewallungen reagieren. Aus diesem Grund ist die Wahrscheinlichkeit, dass genau diese Patientinnen die Tamoxifentherapie vorzeitig beenden, deutlich höher als bei Frauen, die Tamoxifen schlechter verstoffwechseln. Aber auch in Bezug auf diese Fragestellung präsentiert sich die Datenlage alles andere als eindeutig.
Sollte eine CYP2D6-Testung in der klinischen Praxis empfohlen werden? Trotz intensiver Forschung in Bezug auf CYP2D6 und klinische Konsequenzen eines veränderten Genotyps bleibt die Frage des tatsächlichen Einflusses des Genotyps oder der verabreichten Komedikation kontroversiell diskutiert. Auch wenn ein Teil der Evidenz die Hypothese unterstützt, dass eine verminderte CYP2D6-Aktivität mit einem schlechteren Outcome in Bezug auf das Mammakarzinom verbunden ist, ist derzeit eine generelle Testung des CYP2D6-Genotyps – bis auf das Einlangen von Ergebnissen von prospektiven Studien – nicht empfohlen. Derzeit wird in keiner der gängigen Leitlinien eine derartige molekulargenetische Analyse des CYP2D6-Locus empfohlen. Trotzdem gibt es in der klinischen Praxis Situationen, in denen unter Umständen eine CYP2D6- Testung angedacht werden kann. Insbesondere in Situationen, in denen eine relative Kontraindikation gegenüber einem Aromatasehemmer besteht.
FAZIT: Derzeit ist in den vorliegenden Daten eine Tendenz in Richtung schlechterer Prognose von Patientinnen unter Tamoxifentherapie mit einem oder mehreren hypofunktionellen Varianten des CYP2D6-Allels zu beoabachten. Zusätzlich scheinen bestimmte Medikamente, die die Aktivität von CYP2D6 inhibieren, ebenfalls zu einem Wirkungsverlust der endokrinen Therapie mit Tamoxifen zu führen. Trotz intensiver Bemühungen fehlen derzeit noch die Ergebnisse von entsprechenden prospektiven Studien. Eine routinemäßige Testung des CYP2D6-Genotyps ist derzeit nicht indiziert. Allerdings soll die gleichzeitige Verschreibung von CYP2D6-Inhibitoren (wie z. B. SSRI) nur unter strenger Indikation erfolgen bzw. vermieden werden.
* nach einem Vortrag im Rahmen des Symposiums „Herausforderungen der modernen endokrinen Therapie“ der Österreichischen Gesellschaft für Senologie anlässlich der 31. Jahrestagung der Deutschen Gesellschaft für Senologie in Dresden (23.–25. Juni 2011)