Biobanking im Rahmen der chronischen Nierenerkrankungen

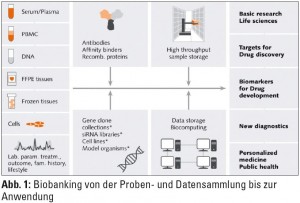 Biobanken sind geordnete stoffliche Sammlungen biologischer Proben mit den zugeordneten Daten in strukturierter, auswertbarer Form. Die probenassoziierten Patientendaten werden in Datenbanken gespeichert, verarbeitet und verwaltet. Biobanken für die medizinische Forschung enthalten typischerweise Gewebeproben, Blut, Harn, Zellen oder DNA-Proben humanen Ursprungs. Sie schaffen wichtige Voraussetzungen für den wissenschaftlichen Fortschritt, indem sie biologisches Material und dazugehörige Hintergrundinformationen der Spender für Forschungs- und Entwicklungsprojekte zur Verfügung stellen. Ihre Funktionsfähigkeit liegt im Interesse der Allgemeinheit, da jeder erkrankte Mensch vom medizinischen Fortschritt profitieren kann (Abb. 1).
Biobanken sind geordnete stoffliche Sammlungen biologischer Proben mit den zugeordneten Daten in strukturierter, auswertbarer Form. Die probenassoziierten Patientendaten werden in Datenbanken gespeichert, verarbeitet und verwaltet. Biobanken für die medizinische Forschung enthalten typischerweise Gewebeproben, Blut, Harn, Zellen oder DNA-Proben humanen Ursprungs. Sie schaffen wichtige Voraussetzungen für den wissenschaftlichen Fortschritt, indem sie biologisches Material und dazugehörige Hintergrundinformationen der Spender für Forschungs- und Entwicklungsprojekte zur Verfügung stellen. Ihre Funktionsfähigkeit liegt im Interesse der Allgemeinheit, da jeder erkrankte Mensch vom medizinischen Fortschritt profitieren kann (Abb. 1).
Grundsätzlich unterscheidet man im humanmedizinischen Bereich populationsbasierte von krankheitsspezifischen Biobanken. Die ersteren werden für groß angelegte Populationsstudien verwendet. Dazu zählt beispielsweise die repräsentative Biomaterialdatenbank PopGen des Universitätsklinikums Schleswig-Holstein für populationsbasierte Studien zu genetischen Risikofaktoren. Krankheitsspezifische Biobanken dienen der Sammlung von Patientenproben sowie assoziierten klinischen Daten. Sie werden als Informationsquelle zu Diagnose, Therapie und Forschung herangezogen.
Pharmaindustrie, kommerzielle und akademische Biobanken
Pharmacogenetics Working Group: Nur wenige pharmazeutische Unternehmen sind wirtschaftlich in der Lage, eigene Biobanken aufzubauen und zu unterhalten. Diese Unternehmen sind überwiegend in der sogenannten Pharmacogenetics Working Group organisiert (Abbott Laboratories, Bayer Schering Pharma AG, Merck & Co., Novartis GmbH, u. a.). Die Erwartungen dieser Working Group an den zukünftigen Nutzen von Biobanken sind ein vertieftes Wissens über die molekularen Grundlagen von Krankheiten, ein besseres ursächliches Verständnis der Krankheitsdisposition, den Reaktionen von Patientenkollektiven auf eine Wirksubstanz, die Entwicklung von sichereren und wirksameren medikamentösen Therapien sowie die Gewinnung von Targets für neue medikamentöse Behandlungsmöglichkeiten.
Die meisten Unternehmen versuchen über Kooperationen mit geeigneten universitären Institutionen und Kliniken, Material in ausreichender Quantität und Qualität zu akquirieren. Das gesammelte biologische Material und die zugehörigen Patientendaten sind für definierte Forschungsvorhaben im Interesse der Unternehmen bestimmt. Die lukrierenden Einrichtungen haben hingegen nur begrenzte Möglichkeit, diese Kollektionen für eigene akademische Interessen zu nutzen. Ein Abschluss von Kooperationsverträgen zwischen den beteiligten Institutionen könnte u. a. auch Immaterialgüterrechte wie z. B. die Regelung von Autorenschaften bei wissenschaftlichen Publikationen vertraglich sichern.
Kommerzielle Biobanken: Seit einigen Jahren bieten Betreiber kommerzieller Biobanken, wie Indivumed GmbH oder GulfStream BioInformation Corporation, zunehmend qualitativ hochwertiges Material gemeinsam mit klinischen Daten an. Diese Firmen stellen neben geeigneten Proben auch bestimmte molekularbiologische Analysetechnologien bereit, die im industriellen Kontext normalerweise nicht zur Verfügung stehen.
Akademische Biobanken: Besonders für (immun)histologische Analyse von Gewebeproben und auch für andere molekularbiologische Untersuchungsmethoden greift die Industrie gerne auf die Expertise von – häufig mit Biobanken assoziierten – universitären Instituten zurück. Dem Auftraggeber wird in diesen Fällen lediglich die Auswertung zur Verfügung gestellt, die Gewebeproben verbleiben in der Biobank. Durch den Verzicht auf die direkte Weitergabe von Probenmaterial werden datenschutzrechtliche Probleme umgangen. Die ausschließliche Weitergabe von Ergebnissen ermöglicht eine effiziente Nutzung der Proben.
Proben für akademische Biobanken werden meist im Rahmen von Forschungsprojekten gewonnen. Nach Einholung eines positiven Votums der zuständigen Ethik kommission zur Durchführung der Studie, Patientenaufklärung und -einwilligung kann die akademische Einrichtung das im Rahmen der Studie gesammelte Probenmaterial sowie korrespondierende diagnostische und klinische Patientendaten unabhängig und selbstbestimmend nutzen. Die Universitätsklinik für Nephrologie in Innsbruck betreibt eine Biobank mit Probenmaterial von Patienten mit chronischen Nierenerkrankungen. Innerhalb des EU-Projektes SysKid wird derzeit eine prospektive Kohortenstudie bei Patienten mit Diabetes mellitus Typ II in primären Gesundheitsversorgungseinrichtungen durchgeführt. Blut- und Harnproben, klinische Daten und Laborparameter werden über einen Zeitraum von 48 Monaten gesammelt. Die Proben werden in Innsbruck gelagert, die Patientendaten werden in einer dafür eingerichteten Datenbank gespeichert. Ziel dieses Biobankings ist es, statistisch ausreichende Proben- und Datenmengen für unterschiedlichste zukünftige Analysetechnologien zur biomarkergestützten Diagnose und Prognose von chronischen Nierenerkrankungen bereitstellen zu können.
Qualität von Probenmaterial und Daten, Omics-Technologien
Um die Qualität von Proben und Daten zu gewährleisten, ist beim Biobanking eine definierte Standardvorgehensweise notwendig. Diese Standardisierung betrifft neben der Probenentnahme, deren Aufarbeitung und Lagerung auch die Datenerhebung.
Mit dem Einzug der Omics-Technologien, welche eine umfassende Messung von molekularen Effektoren und Regulatoren auf den verschiedenen Ebenen der molekularen Organisation zellulärer Systeme ermöglichen, änderten sich die Anforderungen an die Probensammlung. Diese analytischen Verfahren (Genomics, Proteomics, Transcriptomics, Metabolomics) erfordern häufig eine sofortige, komplizierte Aufarbeitung v. a. von Blutproben. Proben, die diese Qualitätskriterien nicht erfüllen, können für diese Analysetechnologien nicht genutzt werden.
Ethische Aspekte und Datenschutz
In Österreich hat die Bioethikkommission beim Bundeskanzleramt zur Schaffung rechtlicher Rahmenbedingungen für die Nutzung von Forschungsinfrastrukturen wie Biobanken und statistischen Datenbeständen einen Bericht sowie Empfehlungen und Stellungnahmen zur Schaffung rechtlicher Rahmenbedingungen veröffentlicht (http:// oesterreich.gv.at):
- „Biobanken für die medizinische Forschung: Bericht der Bioethikkommission beim Bundeskanzleramt vom 07. Mai 2007“
- „Biobanken für die wissenschaftliche Forschung: Ergänzung zum Bericht der Bioethikkommission vom Mai 2007, 14. März 2011“
Anonymisierung und Pseudonymisierung sind Maßnahmen des Datenschutzes und verhindern eine Zuordnung personenbezogener Daten. Sie sind im Umgang mit Biobanken unabdingbar, da die verarbeiteten Informationen höchst persönlicher Natur sind.
Anonymisieren bedeutet, dass personenbezogene Daten derart verändert werden, dass die Einzelangaben über persönliche oder sachliche Verhältnisse nicht mehr oder nur mit einem unverhältnismäßig großen Aufwand an Zeit, Kosten und Arbeitskraft einer bestimmten oder bestimmbaren Person zugeordnet werden können. Zusätzlich wird der Code, der eine Verbindung zwischen Proben und Daten einerseits und dem Spender andererseits herstellen kann, irreversibel gelöscht.
Pseudonymisieren ist das Ersetzen des Namens und anderer Identifikationsmerkmale durch ein Kennzeichen (Code) zu dem Zweck, die Bestimmung des Betroffenen auszuschließen oder wesentlich zu erschweren. Die Verbindung zwischen pseudonymisierten Daten und identifizierenden Daten des Spenders (Name, Adresse, Telefonnummer etc.) kann nur durch autorisierte und zur Verschwiegenheit verpflichtete Personen hergestellt werden.
Voraussetzung „informed consent“: Einen weiteren Schutz der Spender gewährleistet die verpflichtende Einholung der Einwilligung – in den englischsprachigen Konventionen zur Humanforschung (Council for International Organizations of Medical Sciences – CIOMS) als „informed consent“ bezeichnet, ein Begriff, der sich auch im deutschsprachigen Raum etabliert hat. Die Verwendung von biologischem Material und personenbezogenen Daten ist nur dann zulässig, wenn der Spender im Voraus über Risiken und Nutzen des Forschungsprojektes informiert wurde und seine Einwilligung durch eine Unterschrift bestätigt.
Die Einholung dieser informierten Einwilligung von Spendern mag für zweckgebundene, zeitlich begrenzte Forschungsvorhaben relativ einfach möglich sein, für Biobanken können aber weder die Modalitäten der Verwendung von Proben und Daten noch eine zeitliche Begrenzung festgelegt werden. Es ist also nicht möglich, den Spender über Zweck, Bedeutung und Tragweite des Forschungsvorhabens angemessen zu informieren. Diese Auflage ist somit unvereinbar mit dem Zweck der meisten Biobanken als Forschungsinfrastruktur für künftige wechselnde Forschungsvorhaben, deren Forschungsziele zum Zeitpunkt der Zusammenstellung der Biobank noch nicht genau bestimmt sind.
In Österreich stehen Betreibern von Biobanken zurzeit keine klaren, transparenten gesetzlichen Regelungen zur Verfügung, u. a. fehlen auch spezielle Vorschriften, die auf die strukturellen Besonderheiten von Biobanken in Bezug auf die Zweckbindung eingehen. Eine rasche Schaffung gesetzlicher Bestimmungen für die Etablierung und Nutzung von Biobanken wäre wünschenswert.
Biobanking in Österreich
Österreichische Biobanken haben maßgeblichen Anteil an der medizinischen Forschung. Erwähnt sei die Biobank der Medizinischen Universität Graz, die eine führende Rolle im internationalen Netzwerk der „Biobanking and Biomolecular Resources Research Infrastructure“ (www.bbmri.eu) spielt. Auch Biobanken der Medizinischen Universität Wien (www.meduniwien.ac.at/orgs) sowie der Medizinischen Universität Innsbruck (www.i-med.ac.at/mypoint/news/2010050501.xml) stellen Schwerpunkte innerhalb dieser Institutionen dar.






















































































