HIV und Eigennierenerkrankung
Vor 10 Jahren stellten sich die Nephrologen die Frage, ob eine HIV-Infektion prinzipiell eine Kontraindikation für die Nierentransplantation bedeutet. So wurde in den im Jahr 2003 publizierten European Renal Practice Guidelines in Nephrology, Dialysis and Transplantation von Sawyer und Ritz festgehalten, dass HIV-Positivität eine absolute Kontraindikation für die Nierentransplantation darstellt. Da sich die Einschätzung in den letzten Jahren geändert hat, werden die Nierentransplantation bei HIV- Erkrankung, aber auch Eigennierenerkrankungen im Zusammenhang mit einer HIV-Infektion für Nephrologen in den nächsten Jahren zum Thema werden.
Im Folgenden sollen Zustände wie das akute Nierenversagen (AKI – acute kidney injury), HIV-assoziierte Nierenerkrankungen, nephrotoxische metabolische Langzeiteffekte der HAART sowie Empfehlungen zum nephrologischen Management vorgestellt werden.
Akutes Nierenversagen
Die Ursachen für akutes Nierenversagen bei HIV-Patienten ähneln jenen bei Nicht-HIV-Patienten. Die häufigste Ursache ist die akute Tubulusnekrose auf Basis von Sepsis, Dehydratation, Hypotension sowie Nephrotoxizität. Allerdings finden sich bei stationärer Aufnahme von HIV-positiven Patienten in 20% der Fälle ein akutes Nierenversagen sowie eine hohe Mortalität mit 18% nach 2 Monaten (davon 80% mit der Diagnose Aids bei Aufnahme). In rezenten Untersuchungen konnte gezeigt werden, dass gerade in dieser Patientenpopulation das akute Nierenversagen mit erhöhter kardiovaskulärer Mortalität und schlechter Prognose hinsichtlich Langzeit-Outcome der Nierenfunktion vergesellschaftet war. Es besteht eine Assoziation zwischen dem akuten Nierenversagen und Mortalität sowie zwischen akutem Nierenversagen und terminaler Niereninsuffizienz bei HIV-positiven Patienten.
HIV-assoziierte Nierenerkrankungen
HIVAN (HIV-assoziierte Nephropathie): Erstmalig wurde die HIVAN als Komplikation von Aids im Jahre 1984 in New York als Collapsing Focal Segmental Glomerulosclerosis beschrieben. HIVAN war gekennzeichnet durch eine nephrotische Proteinurie und Progression zur Dialysepflichtigkeit innerhalb von 8–16 Wochen. Mittlerweile hat sich HIVAN als eigenständige klinische Entität etabliert (collapsing FSGS). HIVAN ist nicht mit fortgeschrittener Immunsuppression im Rahmen der HIV-Infektion assoziiert, sondern die renalen Läsionen können zu jedem Zeitpunkt der HIV-Infektion auftreten, auch bereits vor Serokonversion. Die Mikroalbuminurie scheint ein früher Marker einer HIV-assoziierten Nephropathie zu sein, die Prävalenz der HIV- Positivität liegt bei über 11%. Interessanterweise tritt HIVAN vor allem bei Afroamerikanerinnen auf – mehr als 90% der Patienten mit HIVAN sind Afroamerikaner. Es war auch lange Zeit die am stärksten zunehmende Ursache für die terminale Niereninsuffizienz in dieser Population und stellte nach Hypertonie und Diabetes die dritthäufigste Ursache für die Dialysepflichtigkeit in der Altersgruppe von 20–64 Jahren im letzten Jahrzehnt des vorigen Jahrtausends dar.
Mittlerweile ist die Inzidenz der Dialysepflichtigkeit in der HIV-Population rückläufig. Die Prävalenz nimmt jedoch weiter zu, da sich die Überlebensraten für Aids deutlich verbessert haben.
HIVAN stellt derzeit die siebenthäufigste Ursache für Dialysepflichtigkeit bei Afroamerikanern dar (Daten aus dem USRDS 2007). Auch in Europa, am Beispiel von Frankreich gezeigt, kommt es zu einer Zunahme der Patienten mit HIV-Infektion an der Dialyse, 1997 betrug der Zuwachs 79%. Dies dürfte in Frankreich vor allem auf den Zuzug von Personen aus Endemiegebieten wie Karibik und Subsahara zurückzuführen sein. Die Mortalität von Patienten mit HIVAN- induzierter CKD5D ist deutlich höher als von HIV-negativen Patienten. Erfreulicherweise sieht man, dass sich in den letzten Jahren das Überleben der Patienten mit HIV-Infektionen an der Dialyse deutlich verbesserte.
Zur Therapie der HIVAN liegen keine randomisierten kontrollierten Studien vor. Im Vordergrund stehen nephrologische Allgemeinmaßnahmen wie die Gabe von ACE-Hemmern oder Angiotensinrezeptorblockern, für die es Daten für verbessertes Nierenüberleben gibt, Cyclosporin, das bei Kindern zu einer Remission der Proteinurie führte (keine Daten für Erwachsene) und natürlich die HAART (highly active antiretroviral therapy). Der Einsatz der HAART führte zu einem deutlichen Rückgang der HIVAN. Als Mechanismus wird eine Inhibition von mTOR diskutiert. mTOR-Inhibitoren könnten hier eventuell einen therapeutischen Nutzen bringen, diesbezügliche Studien sind allerdings noch ausständig.
Andere Glomerulopathien: Neben der HIV-assoziierten Nephropathie gibt es eine Reihe von lupusähnlichen Glomerulonephritiden, FSGS, Immunkomplex-Nephritis, interstitielle Nephritis und thrombotische Mikroangiopathie vor allem in den USA. In Europa stehen die IgA-Nephritis sowie Diabetes und Nephroangiosklerose im Vordergrund (z. B. Daten aus Frankreich). In Südafrika ist die zweithäufigste Ursache für eine Nierenerkrankung bei HIV-positiven Patienten eine Immunkomplexglomerulonephritis. Die anderen Glomerulonephritiden im Rahmen einer HIV-Infektion führen zu einem deutlich späteren Verlust der Nierenfunktion als die HIVAN. Die HIV-assoziierte Immunkomplexerkrankung (HIVICK) tritt erst nach einem Zeitraum von durchschnittlich 10 Jahren auf. Zu 70% findet man ein nephrotisches Syndrom, zu 100% eine Hämaturie, zu 80% eine Hypertonie und zu 50% zusätzlich eine Hepatitis-C-Infektion. Bei 70% der Betroffenen kommt es innerhalb eines Jahres nach der Diagnosestellung zu einer dialysepflichtigen Niereninsuffizienz. Mit Ausnahme der HAART gibt es bisher keine Therapievorschläge.
Nephrotoxische und metabolische Langzeiteffekte der antiretroviralen Therapie
Die HAART verbessert die glomeruläre Filtrationsrate, ist allerdings potenziell nephrotoxisch. Die Identifizierung und Beachtung der renalen Risikofaktoren vor Start von HAART kann die therapieassoziierten toxischen Nebenwirkungen minimieren. Die Nierenfunktion von Patienten unter HAART sollte daher bei jeder Visite kontrolliert werden. Die Angst vor möglichen nephrotoxischen Effekten von HAART ist jedoch kein Grund, diese lebensverlängernde Therapie nicht einzusetzen.
Nukleotid-Reverse-Transkriptase-Inhibitoren (NtRTI, Nukleotidanaloga): Unter den antiretroviralen Therapeutika sind besonders Nukleotidanaloga durch Nierentoxizität gekennzeichnet und können zu akutem Nierenversagen, Fanconi-Syndrom, nephrogenem Diabetes insipidus oder interstitieller Nephritis führen.
Tenofovir (Viread®) wird unverändert über den Harn durch aktive Sekretion via proximale Tubuluszellen eliminiert, Probenezid und NSAR senken die intrazelluläre Konzentration. Aufgrund der Nephrotoxizität ist ein solcher therapeutischer Ansatz allerdings nicht sinnvoll. 20% der Patienten unter Tenofovir-freier HAART und 65% der Patienten unter HAART mit Tenofovir entwickeln im Laufe von 5 Jahren Tubulopathien. Ohne entsprechende Kontrollen können Tubulopathien nicht erkannt werden, bevor es zu einer Störung der Nierenfunktion mit Serumkreatininanstieg kommt. Daher sollten bei jeder Visite Kontrollen von Serum- phosphor, Proteinurie und Harnglukose durchgeführt werden. Beta-2-Mikroglobulin im Harn vor Therapiebeginn kann bereits einen frühen Marker für die Tubulopathie darstellen. Durch die Beta-2-Mikroglobulin-Bestimmung kann eine Subgruppe von HIV-Patienten mit einem erhöhten renalen Risiko unter Tenofovir identifiziert werden. Daten zur Progression des Nierenfunktionsverlustes unter Tenofovir sind kontroversiell. Das Risiko scheint nur leicht erhöht, der Einfluss auf die Nierenfunktion über die Jahre dürfte gering sein.
Die meisten Studien ergaben eine geringe absolute Therapieabbruchrate aufgrund von renaler Dysfunktion (0–2%). Daten zu Tenofovir bei Patienten mit CKD sind sehr limitiert. Es sollte vor allem eine Dosisanpassung und ein entsprechendes Monitoring angestrebt werden, um eine sichere Anwendung dieser Substanz zu gewährleisten.
Nukleosid-Reverse–Transkriptase–Inhibitoren (NRTI; Nukleo– sidanaloga): Auch NRTI können zu den oben genannten Symptomen wie akutem Nierenversagen, Fanconi-Syndrom, Hypokaliämie und Hypomagnesiämie (Abacavir, Didanosin, Lamivudin etc.) führen. Bekannt ist auch die mitochondriale Zytopathie, da NRTI die DNA-Polymerase hemmen und die DNA-Polymerase für die Replikation der mitochondrialen DNA verantwortlich ist. Die Folge ist ein sekundäres Defizit von Enzymen der mitochondrialen Atemkette, die von mitochondrialer DNA codiert werden. Durch Verringerung der oxidativen Phosphorylierung entsteht ein Adenosintriphosphat(ATP)-Defizit und es kommt zu einer Laktatproduktion über die anaerobe Atmungskette. 20% der Patienten, die mit NRTI behandelt werden, entwickelten eine asymptomatische Hyperlaktatämie aufgrund der mitochondrialen Zytopathie. Diese Komplikation wird typischerweise nach mehreren Therapiemonaten manifest und kann auch nur temporär auftreten. Schwere Laktatazidosen sind selten (1,5–2%) und mit hoher Mortalität vergesellschaftet (80%). Zu den Risikofaktoren zählen längere Behandlungsdauer, höheres Alter, weibliches Geschlecht, Schwangerschaft, Adipositas, Hepatitis C, CKD und die Kombination mit Ribavirin und Alkohol.
Eine weitere seltene Nebenwirkung der HAART ist die Rhabdomyolyse. Sie sollte bei Auftreten von akutem Nierenversagen insbesondere unter Therapie mit Zidovudin oder Didanosin in Betracht gezogen werden. In einer Biopsieserie fanden sich in 10% der Fälle von akutem Nierenversagen indirekte Hinweise auf eine Rhabdomyolyse. Es gibt einige Fall- berichte einer Rhabdomyolyse unter der Kombination einer HAART mit Statinen. Die Behandlung der Hyperlipidämie sollte daher immer eventuelle Arzneimittelinteraktionen berücksichtigen.
Proteaseinhibitoren, hier vor allem Indinavir, können zu Nierenkoliken aufgrund von Nephrolithiasis oder Obstruktion des Harntraktes durch strahlendurchlässige Nierensteine führen. Unter Indinavir waren renale Koliken vor allem unter Dosen von 2 x 800 mg relativ häufig. Seit der Empfehlung zur Verwendung von Indinavir in der Dosierung von 2 x 400 mg wurden keine neuen Fälle von renalen Koliken mehr gemeldet. Vereinzelt wurden auch Nierenkoliken unter Lopinavir, Saquinavir, aber auch Nelfinavir beschrieben. Für Atazanavir finden sich im FDA-Reporting-System über 4 Jahre 30 Fälle von assoziierter Nephrolithiasis und von interstitieller Nephritis. Die meisten Fälle machten eine stationäre Aufnahme mit Nephrostoma, Lithotripsie oder chirurgischer Intervention notwendig. Bisher wurden keine Langzeitkomplikationen hin- sichtlich CKD unter Atazanavir berichtet. Risikofaktoren sind Dehydratation sowie eine Steinanamnese.
Chronische Niereninsuffizienz (CKD) aufgrund von Hypertonie und Diabetes
Eine cross-sektionalen Studie, an der 31 europäische Länder, Israel und Argentinien beteiligt waren, zeigt, dass bei 4% der HIV-positiven Patienten nach MDRD-Formel eine CKD3 vorliegt. Risikofaktoren für CKD bei HIV stellen das Alter, niedrige CD4+-T-Zellzahl sowie eine kumulative Exposition gegenüber Tenofovir oder Indinavir dar. Single-Center-Studien mit kleineren Fallzahlen zeigen eine höhere Prävalenz (Brasilien
1,1–5,6%, Schweiz 18%, Indien 27%, Iran 20%). Ein signi- fikanter Anstieg des Blutdrucks um über 10 mmHg wurde bei 21% der Patienten mit Lopinavir/Ritonavir innerhalb eines Jahres beobachtet. Die Kombination wäre ein prädiktiver Faktor für die Hypertonie. Auch die Diabetesinzidenz ist unter HAART erhöht. Unter Ritonavir fand sich eine vierfach höhere Inzidenz.
Empfehlungen zum nephrologischen Management
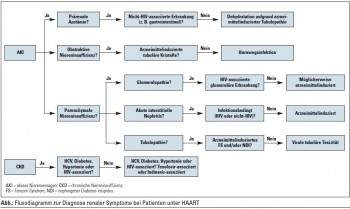
Die Abbildung zeigt das Flussdiagramm zur Diagnose renaler Symptome bei Patienten unter HAART.
Wichtig ist, die Ursache des akuten Nierenversagens ähnlich dem allgemeinen Algorithmus zu evaluieren (prärenal, obstruktiv, intrarenal). Bei Diagnose der HIV-Infektion sollte mittels Harnanalyse und eGFR eine präexistente CKD ausgeschlossen werden. Patienten mit GFR < 60 ml/min und/oder Proteinurie sollten einem Nephrologen vorgestellt werden. Patienten mit Diabetes sollten auf Mikroalbuminurie getestet werden, wobei ein Harnstreifentest nicht ausreicht. Patienten mit hohem Risiko für CKD (Afroamerikaner, CD4 < 200/mm3, HIV-RNA > 4.000 Kopien/ml, Diabetes, Hypertonie, HCV) sollten jährlich, Patienten unter Tenofovir alle 3 Monate „renal“ gescreent werden. Bei unklarer Nierenerkrankung sollte eine Nierenbiopsie durchgeführt werden, dies insbesondere bei ausgeprägter Proteinurie und Reduktion der GFR, weil bei dieser Konstellation das größte Risiko für eine terminale Niereninsuffizienz besteht.
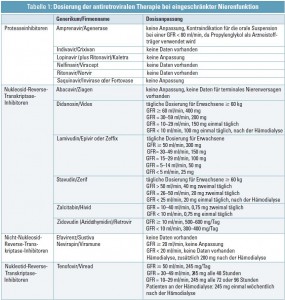
Unter Tenofovir-Therapie steht bei CKD-Patienten vor allem das Screening hinsichtlich Tenofovir-induzierter tubulärer Dysfunktionen im Vordergrund, das in folgenden Situationen durchgeführt werden sollte: GFR < 90 ml/min, Komedikation mit anderen renal eliminierten Medikamenten (z. B. Adefovir, Aciclovir, Ganciclovir oder Cidofovir), bestehende Komorbiditäten wie Hypertonie oder Diabetes sowie Verwendung von mit Ritonavir geboosterten Proteaseinhibitoren- Therapieschemata. Das Screening sollte zweimal im Jahr durchgeführt werden und inkludiert die Messung von Kaliumphosphat, Harnsäure und Bikarbonat, die Messung der tubulären Resorption von Phosphat, die fraktionelle Harnsäureexkretion, Beta-2-Mikroglobulin im Harn und Überprüfung einer möglichen Glukosurie. Wesentlich ist auch die Dosisanpassung an die Nierenfunktion (Tab. 1). Keine Dosisanpassung ist erforderlich bei Etravirin, Proteaseinhibitoren wie Tipranavir/Ritonavir, Darunavir/Ritonavir-Kombination, Enfuvirtid oder Raltegravir. CCR5-Rezeptor-Antagonisten wie Maravicor werden zu 25% eliminiert. Hier ist Vorsicht bei einer GFR < 50 ml/min geboten.
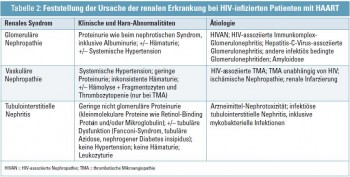
NEPHRO Spot Zusammenfassend kann festgehalten werden, dass die HIV- Erkrankung eine Herausforderung für den Nephrologen darstellt. Wichtig wäre, wie in Tabelle 1 angeführt, zur Feststellung der Ursache der renalen Erkrankung eine Abklärung hinsichtlich glomerulärer, vaskulärer oder tubulointerstitieller Nephritis.
Eine enge Zusammenarbeit mit HIV-Spezialisten ist daher unabdingbare Voraussetzung.