Therapie und Management der HIV-Infektion
Highly Active Antiretroviral Therapy (HAART)
Die ART der HIV-Infektion stellt immer eine Kombinationstherapie aus mehreren Wirkstoffklassen dar, die als „highly active antiretroviral therapy“ (HAART) bezeichnet wird. Unter Monotherapien entstehen rasch Resistenzen, wie die klinische Erfahrung mit der Behandlung mit Retrovir in den 1990er-Jahren gezeigt hat.
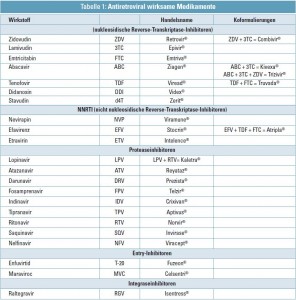
Die Zahl der antiretroviral wirksamen Medikamente ist in den letzten 2 Jahrzehnten massiv gestiegen (Tab. 1). Die heute in der Klinik eingesetzten Substanzen gehören 4 Gruppen an:
1. Nukleos(t)idische Reverse-Transkriptase-Inhibitoren (N(t)RTI), nicht nukleosidische Reverse-Transkriptase- Inhibitoren (NNRTI),
2. Proteaseinhibitoren (PI),
3. Entry-Inhibitoren und
4. Integraseinhibitoren (INSTI).
Die Kombination mehrerer Substanzen derselben Wirkstoffklasse bzw. aus verschiedenen Wirkstoffklassen in Koformulierungen hat durch Reduktion der Pillenzahl die Einnahme der HAART für Patienten deutlich einfacher gemacht.
Nebenwirkungen: Die häufigsten Nebenwirkungen der HAART sind zu Beginn der Therapie Übelkeit und Durchfall (PI mehr als NRTI), Hautausschläge (NNRTI), Hypersensitivitätssyndrome (ABC, NVP), Schlafstörung, Schwindel (EFV), Hyperbilirubinämie (ATV). Langfristige Nebenwirkungen bzw. Spätfolgen betreffen das kardiovaskuläre System (erhöhtes KHK-Risiko: PI, ABC), den Stoffwechsel (Insulinresistenz, Hyperlipidämie: PI), die Nierenfunktion (TDF) und den Knochenstoffwechsel (TDF). N(t)RTI werden vor allem renal ausgeschieden und ihre Dosierung muss an die Nierenfunktion angepasst werden, während PI großteils über die Leber abgebaut werden.
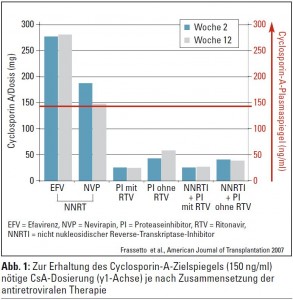
Interaktionspotenzial: Von besonderer Wichtigkeit bei multimorbiden Patienten, die mehrerer Medikamente bedürfen, ist das Interaktionspotenzial der antiretroviralen Substanzen untereinander als auch mit anderen Pharmaka. Alle NNRTI und PI werden über Zytochrom P450 metabolisiert und stellen entweder Induktoren oder Inhibitoren dieses Enzymsystems dar. Wegen der großen Komplexität der zu erwartenden Interaktionen bieten Datenbanken einen schnellen und aktuellen Überblick zur Wirksamkeit und Verträglichkeit von therapeutischen Kombinationen (z. B. www.hiv-druginteractions.com, University of Liverpool). Relevante Interaktionen und klinische Herausforderungen ergeben sich auch bei der gleichzeitigen Gabe von Immunsuppressiva wie Cyclosporin A, wobei je nach Zusammensetzung der ART viel geringere Dosierungen zu sehr hohen Spiegeln führen können oder deutlich höhere Dosierung zur Aufrechterhaltung eines therapeutischen Spiegels benötigt werden können (Abb. 1).
Hilfe bei unklaren Interaktionen kann das sogenannte Drug Monitoring bieten, d. h. das Messen der Plasmaspiegel der potenziell interagierenden Substanzen. Diese Maßnahme stellt keine Routineuntersuchung dar und ist nicht für alle antiretroviralen Substanzen etabliert (PI, NNRTI), kann aber auch bei Patienten mit Complianceproblemen, virologischem Versagen oder unklaren Resorptionsstörungen (z. B. Diarrhö) hilfreich sein.
Therapiebeginn
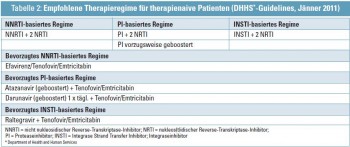
Die aktuellen Richtlinien des Department of Health and Human Services (DHHS) geben 3 gleichwertige Therapieregime für therapienaive Patienten an, die alle aus einem „backbone“ zweier N(t)RTIs in Kombination mit entweder einem NNRTI, einem PI oder einem Integraseinhibitor bestehen (Abb. 2). Die Auswahl der einzelnen Kombinationen sollte Patientencharakteristika wie Komorbiditäten und Komedikationen (mögliche Interaktionen), Kinderwunsch (Teratogenität), Compliance und Lebensstil (einmal tägliche Medikation, morgens oder abends etc.) berücksichtigen.
Vor dem Beginn einer ART ist die Durchführung eine Resistenztestung wichtig. Die Übertragung resistenter Viren erfolgt zwar nach wie vor nur in einer Minderheit der Fälle und ist in den letzten Jahren trotz des breiteren Einsatzes der HAART nicht weiter angestiegen, sie erreicht aber für bestimmte Wirkstoffgruppen doch klinisch relevante Werte (10–15% primäre Resistenzen, v. a. für NNRTI). Selbstverständlich muss auch vor dem Einsatz von CCR5-Antagonisten eine Tropismus-Bestimmung erfolgen, das heißt die Austestung des vom HI-Virus verwendeten Korezeptors. Denn der Einsatz dieser Substanzen ist nur bei ausschließlich CCR5-tropen Viren sinnvoll.
Derzeit stellt eine Kombination aus Tenofovir/Emtricitabin oder Abacavir/Lamivudin die empfohlene „backbone“-Kombination dar. In Einzelfällen können jedoch auch nicht in den Guidelines empfohlene Therapieregime einen geeigneteren Therapieansatz darstellen.
Die Empfehlungen zum Zeitpunkt des Therapiebeginns haben sich in den letzten Jahren mehrmals stark geändert. Während man in den Anfängen der HAART-Regime (1995/96) für einen raschen bzw. sogar sofortigen Therapiebeginn plädierte, wurde aufgrund schlechter Verträglichkeit und Resistenzentwicklungen in weiterer Folge ein Zuwarten zur klinischen Progression oder einer CD4-Zellzahl unter 200 Zellen/µl bevorzugt. Rezente Studien zeigten jedoch nun doch einen Vorteil eines früheren Therapiebeginns, der durch verbesserte Verträglichkeit und dauerhafte Wirksamkeit der aktuellen Kombinationspräparate auch praktikabel ist. Verlässliche Erkenntnisse über Nutzen und Risiken eines frühen Therapiebeginns erwartet man sich von einer derzeit laufenden Multicenterstudie (START-Studie), die randomisiert einen sofortigen Therapiebeginn bei Diagnosestellung und einer CD4-Zellzahl > 500/µl versus einen Therapiebeginn bei Erreichen der derzeit gültigen Richtwerte (im Allgemeinen < 350/µl, siehe unten) vergleicht.
Indikation zur Therapie
Konsens über die Sinnhaftigkeit einer antiretroviralen Therapie besteht zurzeit bei
1) symptomatischen HIV-Patienten Stadium B und C (nach CDC) sowie bei
2) asymptomatischen Patienten mit weniger als 350 CD4- Zellen/µl.
Bei Patienten mit 350–500 CD4-Zellen/µl sollte bei Vorliegen von Komorbidität(en) wie einer Hepatitis-B- oder -C-Koinfektion oder einer HIV-assoziierten Organpathologie (z. B. Nierenfunktionsstörung) ein Therapiebeginn empfohlen, bei Risikofaktoren für eine beschleunigte Progression (hohe Viruslast, rascher CD4-Zellabfall, Alter > 50 Jahre) oder dem Vorliegen von erhöhtem kardiovaskulärem Risiko oder Malignomen eine Therapie zumindest erwogen werden (Tab. 3).
Einen Sonderfall stellt die Behandlung von HIV-infizierten Schwangeren dar. Hier kann die Therapie nicht nur in der mütterlichen Indikation, sondern auch in der kindlichen Indikation (Vermeidung der vertikalen Transmission) begründet sein. Besteht keine Indikation zur Behandlung der Mutter per se, so sollte eine ART nach dem ersten Trimenon, spätestens jedoch in der 28. Schwangerschaftswoche begonnen werden, um zum Zeitpunkt des größten Risikos einer vertikalen Transmission – der Geburt – eine virologische Suppression erreicht zu haben.
Ziel der antiretroviralen Therapie
Ziel der ART ist eine konstante Suppression der Virusreplikation und damit in weiterer Folge eine Immunrekonstitution (Wiederanstieg, Stabilisierung bzw. Normalisierung der CD4- Zellzahl). Regelmäßige Kontrollen des Therapieerfolgs und der Verträglichkeit sind indiziert. Das erreichbare Ausmaß der Immunrekonstitution sowie der Zeitrahmen, der zum Erreichen normaler CD4-Zellzahlen nötig ist, wird maßgeblich durch die CD4-Zellzahl zu Beginn der Therapie bzw. den CD4- Nadir (tiefster im Laufe der HIV-Infektion jemals gemessener CD4-Zellwert) bestimmt. Aber auch andere Faktoren wie das Patientenalter, die Dauer der Infektion, Koinfektionen und Komorbiditäten, aber auch noch nicht identifizierte Ursachen beeinflussen diesen Vorgang. Rezente Studien zeigen, dass es auch nach Normalisierung der CD4-Zellzahl im Blut nicht zu einer kompletten Wiederherstellung aller Immunfunktionen kommt und z. B. schon im Rahmen der akuten HIV-Infektion gesetzte Schäden im Bereich des lymphatischen Systems im Gastrointestinaltrakt (MALT) nicht mehr korrigiert werden können. Weiters bleiben, wenn auch im Vergleich zur unbehandelten HIV-Infektion geringer ausgeprägte Zeichen einer chronischen Immunaktivierung bestehen. Die im Rahmen der Immunrekonstitution wiedergewonnenen T-Zellen sind jedoch funktionstüchtig. Der beste Hinweis hierfür ist, dass gewöhnlich nach Überschreiten definierter CD4-Werte prophylaktische antimikrobielle Therapien abgesetzt werden können, die bei Patienten mit stark reduzierter CD4-Zellzahl zur Vermeidung von opportunistischen Infektionen (PCP, To- xoplasmose, MAC) gegeben werden müssen.
NEPHRO Spot
Mit keiner der derzeit vorhandenen Therapien ist eine Heilung der HIV-Infektion möglich. Grund dafür ist das sogenannte latente Reservoir – schlafende HI-Viren in ruhenden Immunzellen, die durch die ART nicht angegriffen und eliminiert werden können. Dieses Reservoir bleibt über viele Jahre stabil, setzt immer wieder in geringer (meist unter der Nachweisgrenze liegender) Menge Viren frei und wird bei kontinuierlicher erfolgreicher ART nur sehr langsam kleiner. Theoretische Berechnungen haben ergeben, dass dieses Reservoir erst etwa nach 70 Jahren Therapie eliminiert ist. Auch wenn die HIV-Infektion eine chronische Krankheit bleibt, so ist sie doch zu einer gut behandelbaren Erkrankung geworden. Der Erfolg der ART lässt sich deutlich an der gesteigerten Lebenserwartung der infizierten Personen zumindest in Ländern mit uneingeschränktem Zugang zu Therapie ablesen. Der immer größer werdende Anteil an älteren Patienten sowie die lange Krankheitsdauer stellen den Behandler allerdings vor neue Herausforderungen. Damit wird es auch immer wichtiger, die HIV-Infektion als Systemerkrankung mit Auswirkungen auf fast alle Organsysteme zu erkennen und rechtzeitig mit der Behandlung zu beginnen.