Neuroimaging bei Parkinson-Syndromen
Die MSA ist wie der MP und die DLB eine Alpha-Synukleinopathie, die entsprechend den Diagnosekriterien immer mit autonomen Symptomen wie Blasenfunktionsstörungen oder orthostatischer Dysregulation vergesellschaftet ist. Je nach Auftreten von Zusatzsymptomen zum Untersuchungszeitpunkt wird die MSA in zwei Unterformen unterteilt: die MSA-P zeigt überwiegend Zeichen eines L-Dopa-refraktären PS und ist neuropathologisch durch striatonigrale Degeneration (SND) gekennzeichnet, wohingegen die MSA-C mit zerebellären Zeichen einhergeht und auf einer olivo-ponto-zerebellären Atrophie (OPCA) beruht. Im Verlauf der Erkrankung bietet ein Großteil der PatientInnen neben den autonomen Symptomen sowohl Parkinson- als auch zerebelläre Symptome, auch neuropathologisch liegt in den meisten Fällen sowohl eine SND als auch eine OPCA vor.
Die PSP ist eine Tau-Protein-assoziierte neurodegenerative Erkrankung und kann sich im Frühstadium heterogen präsentieren. Der klassische Phänotyp, das Richardson-Syndrom (RS), ist durch das Vorliegen einer supranukleären vertikalen Blickparese, posturaler Instabilität und Fallneigung mit Stürzen nach hinten gekennzeichnet. Daneben gibt es aber noch atypische Präsentationen wie die Parkinson- Variante der PSP (PSP-P) mit einem initial auf L-Dopa meist gering bis mäßiggradig ansprechenden PS, die erst im späteren Verlauf die Symptome des RS zeigt. Die meisten bildgebenden Studien wurden mit RS-PatientInnen durchgeführt, wohingegen die eigentliche Schwierigkeit in der Diagnose der sich atypisch präsentierenden PSP-P liegt.
Die CBD ist wie die PSP eine Tauopathie und neuropathologisch durch eine asymmetrische kortikale Degeneration gekennzeichnet. Die klassische Manifestation der CBD ist die klinische Präsentation als kortikobasales Syndrom (CBS, corticobasal syndrome) und umfasst eine strikt asymmetrische Symptomausprägung wie unilaterale Extremitätenapraxie (ggf. mit „Alien-limb-Phänomen“ der fremden Extremität) u. a. vergesellschaftet mit Myoklonus, Dystonie, Bradykinese und Rigor der betreffenden Extremität. Allerdings haben rezente klinisch-neuropathologische Studien gezeigt, dass sich eine CBD phänotypisch auch als PSP oder als eine frontotemporale Demenz präsentieren kann, während andererseits einem CBS neuropathologisch eine CBD, eine PSP, eine frontotemporale Demenz oder eine Alzheimer-Erkrankung zugrunde liegen können. Die meisten Bildgebungsstudien wurden bei klinisch diagnostizieren PatientInnen mit CBS durchgeführt. Interessanterweise ergaben Nachuntersuchungen von in Allgemeinpraxen diagnostizierten MP-PatientInnen Fehldiagnoseraten von bis zu 50 %. Die Diagnose sollte daher durch NeurologInnen gestellt werden. Die zurzeit erreichbare Zuverlässigkeit der klinischen Diagnose MP liegt jedoch selbst in spezialisierten Zentren und im fortgeschrittenen Stadium bei maximal 90 %.
Die DLB manifestiert sich im Gegensatz zum MP mit einem frühzeitigen demenziellen Syndrom. Zu den Kernsymptomen der DLB gehören außerdem fluktuierende kognitive Defizite, insbesondere der Aufmerksamkeit, und wiederholte detaillierte visuelle Halluzinationen. Die DLB ist wie der MP eine Alpha-Synukleinopathie, wobei sich die Lewy-Körperchen hauptsächlich in Neokortex, limbischem Kortex, Hirnstamm und Nucleus basalis Mynert finden.
Bildgebende Untersuchungen können wesentlich zur Diagnostik von Parkinson-Syndromen beitragen und haben in den letzten Jahren daher einen wichtigen Stellenwert in der klinischen Routine erlangt. SPECT (single photon emisson computed tomography) und PET (positron emission tomography) sind nuklearmedizinische funktionelle Bildgebungsverfahren, die die Untersuchung von Hirnperfusion, -stoffwechsel und Rezeptorsystemen erlauben. Die Dopamintransporter-SPECT (DAT-SPECT) kann zwischen Parkinson-Syndromen mit und ohne dopaminerger Degeneration differenzieren und hat zurzeit den höchsten praktischen Stellenwert unter den funktionellen Bildgebungsverfahren. Untersuchungen des Zuckerstoffwechsels (FDGPET) und D2-Rezeptor-Untersuchungen (IBZM-SPECT) können zur Differenzierung der verschiedenen degenerativen Parkinson-Syndrome beitragen.
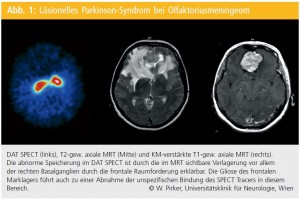
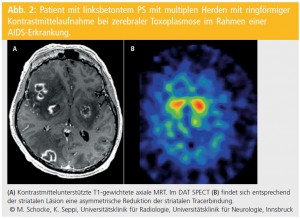
In der Regel sollte vor funktionellen bildgebenden Untersuchungen (SPECT, PET) eine kraniale Computertomographie (CT) oder Magnetresonanztomographie (MRT) durchgeführt werden, um Fehlinterpretationen aufgrund von strukturellen Läsionen zu vermeiden. Die Abbildungen 1 und 2 demonstrieren Beispiele einer verminderten striatalen Tracerbindung in der DAT-SPECT-Untersuchung bei strukturellen Läsionen und zeigen die Notwendigkeit der Kenntnis eines strukturellen Befundes bei Durchführung einer funktionellen Bildgebung auf.
Die strukturelle Bildgebung mittels kranialer CT oder MRT dient primär dem Ausschluss läsioneller Parkinson-Syndrome z.B. bei Raumforderungen im Frontallappen bzw. in den Basalganglien, wobei die MRT die im Vergleich zur CT wesentlich sensitivere Methode darstellt. Bei atypischen Parkinson-Symptomen und selteneren heredo-metabolischen Störungen finden sich in der konventionellen MRT bei einem Teil der PatientInnen charakteristische Atrophiemuster bzw. Veränderungen der Signalintensität, die eine diagnostische Abgrenzung vom MP erlauben. Entscheidende Verbesserungen in der Diagnostik könnten moderne MRT-Techniken wie die Verwendung suszeptibilitätsgewichteter Sequenzen, die sensitiv auf die Entdeckung von Eisenablagerungen sind, die Rela – xometrie, mit deren Hilfe Eisenablagerungen quantifiziert werden, sowie die Diffusions- Tensor-Bildgebung (DTI, diffusion tensor imaging), mit deren Hilfe die Bewegung der Wassermoleküle über den Diffusionskoeffizienten und über die fraktionale Anisotropie im hoch organisierten ZNS beschrieben werden können, bieten. Die DTI kann sogar den Verlauf der einzelnen Faserbündel durch das ZNS visualisieren, dies wird auch als Traktographie bezeichnet. Gerade in der Neurobildgebung wird auch immer mehr die Verwendung von 3-Tesla-MRT-Geräten propagiert.
Zudem hat die transkranielle Parenchymsonographie (TCS) für die Differenzialdiagnose des MP über das letzte Jahrzehnt zunehmend an Bedeutung gewonnen, indem bei 90 % der PatientInnen mit MP eine so genannte Hyperechogenität im Mittelhirn im Bereich der Substantia nigra (SN+) nachweisbar ist, wobei dieses Ultraschallsignal bei ca. 10 % der gesunden Menschen vorliegt. Ziel dieser Übersichtsarbeit ist es, der Leserin, dem Leser einen Überblick über den Stellenwert der wichtigsten bildgebenden Verfahren in der heutigen klinischen Diagnostik bei der Abklärung von neurodegenerativen Parkinson- Syndromen zu geben.
Funktionelle Bildgebung
DAT-SPECT und F-Dopa-PET bei Morbus Parkinson
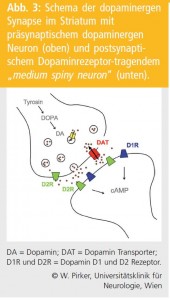
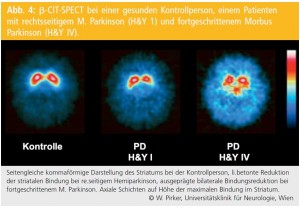
Der MP ist durch eine relativ selektive Degeneration dopaminerger Neurone in der Substantia nigra (SN) und ihrer Nervenendigungen im Striatum gekennzeichnet (Abb. 3). Damit kommt es im Krankheitsverlauf zu einer zunehmenden Reduktion der Dichte von Dopamintransportern (DAT), die selektiv an dopaminergen Nervenendigungen im Striatum exprimiert sind. Die postsynaptischen Dopaminrezeptoren bleiben dagegen im Wesentlichen intakt. DAT-SPECT-Untersuchungen zeigen beim MP eine progressive Reduktion der striatalen Tracerspeicherung mit zunehmender Dauer und Schwere der Erkrankung (Abb. 4).
Bei PatientInnen mit Hemiparkinson ist die striatale Bindung kontralateral zur klinisch betroffenen Seite stärker reduziert, eine leichte Minderspeicherung findet sich in der Regel aber auch ipsilateral. Die Reduktion der DATBindung ist im Putamen ausgeprägter als im Kopf des Nucleus caudatus. Die mittels PET gemessene striatale F-Dopa-Speicherung reflektiert die Aktivität der Dopa-Dekarboxylase in dopaminergen Nervenendigungen. Sie nimmt analog zur DAT-Bindung im SPECT mit zunehmender Erkrankungsdauer ab.
Hohe Sensitivität: Die DAT-SPECT kann mit hoher Sensitivität zwischen gesunden Personen und PatientInnen mit MP differenzieren. Entscheidend für die Beurteilung der Untersuchung ist das Erkennen des pathologischen Musters der striatalen Bindung beim MP (Asymmetrie, Putamen stärker betroffen als Nucleus caudatus). Die semiquantitative Auswertung (Berechnung der Ratio aus spezifischer und unspezifischer Bindung) kann wesentliche Zusatzinformationen liefern. Nicht allen Zentren stehen jedoch Kontrollwerte aus einem geeigneten Normalkollektiv zur Verfügung. Bei grenzwertigem Befund und anhaltend unklarer klinischer Diagnose kann im Einzelfall eine Wiederholung der SPECTUntersuchung nach 1 bis 2 Jahren sinnvoll sein.
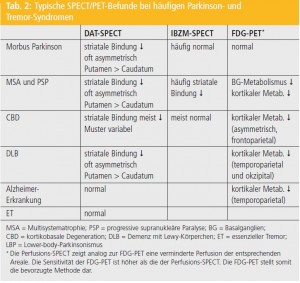
SWEDD: Die hohe Sensitivität des funktionellen Imagings in der Frühdiagnose des Morbus Parkinson wurde durch einige prospektive SPECT- bzw. PET-Studien in Frage gestellt, die zeigten, dass etwa 10 % der PatientInnen mit der klinischen Diagnose eines sehr milden MP eine normale striatale DAT- bzw. F-Dopa- Bindung aufweisen. Diese normalen bildgebenden Befunde bei PatientInnen mit der klinischen Diagnose eines Morbus Parkinson wurden als SWEDD (scans without evidence for dopaminergic deficit) bezeichnet. Der SPECT- bzw. PET-Befund blieb bei diesen PatientInnen nach einem mehrjährigen Beobachtungszeitraum normal. Bislang ist kein SWEDD-Patient dokumentiert, bei dem das Parkinson-Syndrom eine weitere klinische Progredienz gezeigt hätte. Es ist daher mit großer Wahrscheinlichkeit davon auszugehen, dass diese PatientInnen nicht unter einem MP leiden. Als eine mögliche Ursache wurde unlängst ein im Erwachsenenalter auftretender dystoner Extremitätentremor, der leicht mit einem Parkinson-Tremor verwechselt werden kann, beschrieben. Die Tabelle 2 zeigt typische SPECT/PET-Befunde bei häufigen Parkinson- und Tremor-Syndromen.
Im Gegensatz zum MP zeigen PatientInnen, die im Rahmen einer Depression milde extrapyramidale Symptome entwickeln, PatientInnen mit psychogenem Parkinson-Syndrom, essenziellem und psychogenem Tremor sowie Dopa-responsiver Dystonie eine normale striatale DAT-Bindung.
Ein Parkinsonoid nach Gabe niedriger Neuroleptika- Dosen kündigt bei älteren PatientInnen nicht selten einen beginnenden MP, der ohne Neuroleptikum noch subklinisch war, an. Dieser kann mittels DAT-SPECT dokumentiert werden. Ergibt die DAT-SPECT einen Normalbefund, kann davon ausgegangen werden, dass das PS medikamentös induziert ist und nach Absetzen des auslösenden Medikaments abklingen wird.
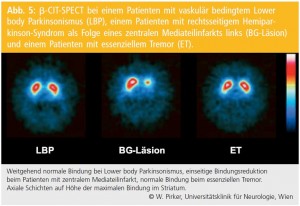
Vaskuläre Parkinson-Syndrome: Marklagerläsionen bzw. lakunäre Infarkte in den Basalganglien führen häufig zu Parkinson-Syndromen mit Betonung der unteren Körperhälfte (lower body parkinsonism, LBP), gelegentlich aber auch zu Parkinson-Syndromen, die schwer vom MP oder von aPS differenzierbar sind. DAT-SPECT-Untersuchungen bei vaskulär bedingtem Lower-body-Parkinsonismus zeigen meist eine normale oder nur leicht reduzierte striatale DAT-Bindung. Territorialinfarkte unter Einbeziehung der Basalganglien können zu einer Reduktion der DAT-Bindung im Bereich des Substanzdefektes führen (Abb. 5). Die sehr seltenen vaskulären Parkinson-Syndrome durch Läsion im Bereich der Substantia nigra führen zu einer streng einseitigen Reduktion der striatalen DAT-Bindung. Im Einzelfall können PatientInnen mit vaskulären Parkinson-Syndromen ein Muster reduzierter striataler DAT-Bindung zeigen, das nicht vom MP zu unterscheiden ist. Die DAT-SPECT kann bei der Fragestellung vaskuläres Parkinson-Syndrom vs. Morbus Parkinson in folgenden Fällen zur Diagnose beitragen:
- Die SPECT ergibt eine normale DAT-Bindung,
- Die SPECT ergibt ein Muster der striatalen DAT-Bindung, das klar vom MP abweicht (z. B. streng einseitiger Bindungsverlust).
In beiden Fällen ist ein MP mit großer Wahrscheinlichkeit ausgeschlossen. Ein MP-typischer DAT-SPECT-Befund schließt aber ein vaskuläres Parkinson-Syndrom nicht mit letzter Sicherheit aus. Die richtige Interpretation des SPECT-Befundes ist in diesen Fällen nur unter Einbeziehung der strukturellen Bildgebung möglich.
SPECT und PET bei atypischen Parkinson-Syndromen
Atypische Parkinson-Syndrome degenerativer Ätiologie wie MSA, PSP und CBD sind durch schlechtes oder fehlendes Ansprechen auf L-Dopa und rascheren Krankheitsverlauf mit früher Behinderung gekennzeichnet. Neuropathologisch zeigen diese Erkrankungen eine Degeneration zahlreicher Neuronensysteme des ZNS, die üblicherweise das „präsynaptische“ dopaminerge System und die „postsynaptischen“ Neuronen des Striatums einschließt. Die DAT-SPECT zeigt bei atypischen Parkinson-Erkrankungen in der Regel eine Reduktion der striatalen Bindung. Das Muster der striatalen DAT-Bindung erlaubt keine individuelle Differenzierung von PatientInnen mit Morbus Parkinson, MSA und PSP.
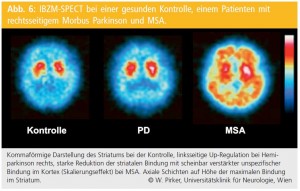
IBZM-SPECT: Dopaminrezeptor-Untersuchungen mit IBZM zeigen bei etwa zwei Drittel der PatientInnen mit MSA bzw. PSP eine Reduktion der striatalen D2-Rezeptor-Bindung. Dagegen ergibt die IBZM-SPECT-Untersuchung beim MP typischerweise einen Normalbefund (Abb. 6), obschon die Häufigkeit abnormer IBZM-Befunde bei MP-PatientInnen in manchen Literaturstellen mit bis zu 30 % angegeben wird. Daher ist die Aussagekraft von IBZM-Studien in der Differenzialdiagnose neurodegenerativer Parkinson- Syndrome nur begrenzt. Zum einen schließt ein Normalbefund eine MSA oder PSP nicht aus, zum anderen kann sich manchmal hinter einer pathologischen IBZM-Studie auch ein MP verbergen. Die Aussagekraft von IBZMSPECT- Studien kann durch eine Therapie mit Neuroleptika, Metoclopramid, Kalziumantagonisten wie Flunarizin und Cinnarizin und durch eine Therapie mit Dopaminagonisten massiv eingeschränkt sein. Auf ein rechtzeitiges Absetzen dieser Substanzen ist vor Durchführung einer IBZM-SPECT-Untersuchung zu achten.
Bei nichtdementen PatientInnen mit MP ergeben SPECT-Untersuchungen der Hirnperfusion bzw. Untersuchungen des Glukosestoffwechsels mittels FDG-PET üblicherweise Normalbefunde. Bei der MSA bzw. PSP können sich eine reduzierte striatale und kortikale Perfusion bzw. ein reduzierter Glukosemetabolismus in diesen Regionen zeigen. Bei der CBD zeigt sich eine deutlich asymmetrische Hypoperfusion bzw. ein asymmetrischer Hypometabolismus in Kortex und Basalganglien. Die IBZM-SPECT ergibt bei der CBD jedoch meist keinen eindeutig pathologischen Befund.
Demenz mit Lewy-Körperchen
Die Demenz mit Lewy-Körperchen (DLB) ist durch eine Degeneration des nigrostriatalen dopaminergen Systems, eine schwere Degeneration cholinerger Projektionssysteme und das Auftreten von Lewy-Körperchen im Kortex gekennzeichnet. DLB-PatientInnen zeigen daher wie beim MP eine reduzierte striatale DAT-Bindung. Die Alzheimer-Erkrankung zeigt dagegen keine relevante dopaminerge Degeneration und damit keine Bindungsreduktion in der DAT-SPECT. Die DAT-SPECT kann daher zuverlässig zwischen DLB (reduzierte Bindung) und Alzheimer-Erkrankung (Normalbefund) unterscheiden. Perfusions-SPECT-Untersuchungen bzw. FDGPET zeigen bei der DLB ebenso wie bei der Alzheimer-Erkrankung häufig ein temporoparietales Perfusions- bzw. Stoffwechseldefizit. Im Gegensatz zur Alzheimer-Erkrankung findet sich bei der DLB häufig eine Hypoperfusion bzw. ein Hypometabolismus auch im okzipitalen Kortex. Dieses Muster erlaubt im Einzelfall aber keine zuverlässige Differenzierung von DLB und Alzheimer-Erkrankung.
Heredodegenerative und -metabolische Erkrankungen
Eine große Zahl heredodegenerativer und -metabolischer Erkrankungen kann mit einem, in Einzelfällen L-Dopa-responsiven, Parkinson- Syndrom assoziiert sein.
Morbus Wilson: Der Morbus Wilson ist eine autosomal-rezessiv vererbte Kupferspeicher- Krankheit mit hepatalen und anderen internistischen, zerebellären und extrapyramidalen Symptomen. Die Differenzialdiagnose Morbus Wilson sollte bei allen PatientInnen mit einem Parkinson-Syndrom bzw. einer unklaren Bewegungsstörung mit einem Beginn vor dem 50. Lebensjahr in Erwägung gezogen werden. Einzelfälle mit späterer Manifestation neurologischer Symptome wurden beschrieben. SPECT-Studien zeigen beim Morbus Wilson, insbesondere bei PatientInnen mit neurologischer Verlaufsform, prä- und postsynaptische Veränderungen des dopaminergen Systems. Die striatale IBZM-Bindung ist häufig reduziert. Auch DAT-SPECT-Untersuchungen zeigen häufig eine reduzierte striatale Bindung. Das Muster der striatalen DAT-Bindung kann von einem MP nicht zu unterscheiden sein. Dies ist von besonderer Relevanz für die Interpretation von DATSPECT- Untersuchungen bei jungen Parkinson- PatientInnen. Die spezifische Diagnose des Morbus Wilson erfolgt durch die Kupferbestimmung im Leberbiopsat. Für einige Mutationen ist ein direkter Gennachweis verfügbar.
Doparesponsive Dystonie (DRD): Die DRD ist ein seltenes generalisiertes dystones Syndrom mit charakteristischen Tagesschwankungen, das auf einem hereditären Defekt eines Kofaktors des Dopa-synthetisierenden Enzyms Tyrosin-Hydroxylase bzw. einer Mutation des Tyrosin-Hydroxylase-Gens selbst beruht. L-Dopa in niedriger Dosierung führt zu einer exzellenten Kontrolle dieser ansonsten progredienten, schwer behindernden Erkrankung. Eine Abgrenzung vom juvenilen (dann oft hereditären) MP kann, da bei diesem ebenfalls häufig dystone Symptome auftreten, schwierig sein. Im Gegensatz zum MP ist das dopaminerge System bei der DRD strukturell intakt. PatientInnen mit DRD zeigen daher eine normale striatale DAT-Bindung. Die DAT-SPECT kann also zwischen DRD und juvenilem Morbus Parkinson differenzieren.
Morbus Huntington: Die rigid-akinetische Variante kann mit anderen Parkinson-Syndromen verwechselt werden. Beim Morbus Huntington kommt es frühzeitig zu einer Degeneration D2-Rezeptor-tragender, GABA-erger Neurone im Striatum. Die IBZM-SPECT zeigt daher in der Regel eine reduzierte striatale D2-Rezeptor-Bindung. Aufgrund des seit einigen Jahren verfügbaren direkten Gennachweises hat die SPECT-Untersuchung beim Morbus Huntington an klinischer Bedeutung eingebüßt.
Spinozerebelläre Ataxien (SCA): Die SCAs sind eine heterogene Gruppe von autosomal dominant vererbten zerebellären Degenerationen, die in variabler Kombination mit degenerativen Veränderungen von Kortex, Basalganglien, Hirnstamm, Rückenmark oder peripherem Nervensystem auftreten können. PatientInnen mit spinozerebellärer Ataxie Typ 2 und 3 (SCA 2 und 3) können das klinische Bild eines atypischen Parkinson-Syndroms oder eines typischen L-Dopa-responsiven Morbus Parkinson bieten. DAT-SPECT-Untersuchungen zeigten sowohl bei SCA 2 als auch bei SCA 3 eine stark reduzierte striatale DAT-Bindung. Eine reduzierte DAT-Bindung findet sich auch bei der häufig als choreatisch- ataktisches Syndrom in Erscheinung tretenden SCA 17 (entspricht Huntington’s disease-like disorder 4).
Strukturelle Bildgebung
Im Laufe der letzten Jahrzehnte hat die Magnetresonanztomographie (MRT) immer weiter Einzug in die Abklärung neurodegenerativer Erkrankungen gehalten. Dementsprechend wird bei der Diagnostik von PS von den Leitlinien der Deutschen Gesellschaft für Neurologie einmalig eine strukturelle Bildgebung – vorzugsweise eine MRT – im Rahmen der Basisdiagnostik, vor allem zum Ausschluss eines symptomatischen PS aufgrund von strukturellen Läsionen, empfohlen. Tatsächlich lassen sich auch mit Hilfe der konventionellen MRT PatientInnen mit MP von PatientInnen mit aPS unterscheiden, wenn sich bestimmte, für aPS pathognomonische Zeichen darstellen lassen. Durch Anwendung spezieller Sequenzen und Algorithmen lässt sich die diagnostische Information aus der konventionellen MRT-Bildgebung bei PatientInnen mit PS erheblich erweitern. Voxel-basierte Morphometrie (VBM, voxel-based morphometry), funktionelle MRT, Spektroskopie oder MR-Traktographie werden aber aktuell nur im wissenschaftlichen Zusammenhang untersucht und haben keinen Stellenwert in der klinischen Routinediagnostik. Dies gilt nicht in gleichem Maß für die DWI, wo der Nachweis bzw. Ausschluss von Veränderungen der Diffusivität im Bereich von Putamen und Kleinhirnstielen bereits jetzt an spezialisierten Zentren für die Differenzierung zwischen MP und aPS routinemäßig verwendet wird. Da durchwegs sämtliche Literaturstellen auf Befunden von 1,5-Tesla-(T-)Geräten beruhen, beziehen sich Befunde über Signalveränderungen in diesem Artikel – falls nicht anders angegeben – auf die auch in der klinischen Routine meistverwendeten Magnetfeldstärken von 1,5 T.
MRT bei Morbus Parkinson
Beim Morbus Parkinson zeigt die konventionelle MRT mittels Routinesequenzen (T1-, T2- und PD-Gewichtung) in den frühen Krankheitsstadien in der Regel einen altersentsprechenden normalen Befund. Vor allem im Frühstadium lassen sich keine mittels MRT fassbaren spezifischen Signalpathologien im Sinne einer Neurodegeneration im Bereich des nigrostriatalen Systems detektieren. In späteren Krankheitsstadien allerdings können gelegentlich eine präfrontale kortikale Atrophie, leichte Signaländerungen im Bereich der Substantia nigra (SN) wie Hyperinten sitäten in T2- Bildern oder Verwaschen der Grenzen zum Nucleus ruber hin und ein Aneinanderrücken dieser beiden Strukturen auftreten.
Derartige Veränderungen sind jedoch schwer von altersabhängigen Normvarianten abgrenzbar; bis heute konnte noch kein spezifischer MRT-Marker für MP identifiziert werden. In einer 1,5-T-MRT-Studie konnte allerdings eine Erhöhung der Diffusivität im Tractus olfactorius bei frühen MP-PatientInnen beschrieben werden. Dieses Signal konnte mit einer diagnostischen Wertigkeit von 94 % zwischen MP-PatientInnen und Kontrollen unterscheiden. Diese Ergebnisse entspringen aber einem experimentellen Setting und müssen erst reproduziert werden.
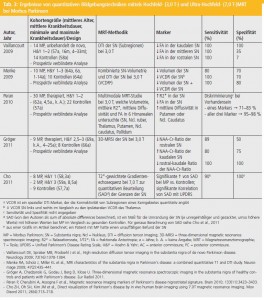
Mehrere rezente Hochfeld-MRI-Studien wurden bei PatientInnen mit MP durchgeführt und zeigten hauptsächlich im Bereich der Substantia nigra interessante Ergebnisse, welche in Tabelle 3 zusammengefasst sind. Alle diese Ergebnisse müssen jedoch noch reproduziert werden und sind daher als experimentell zu werten.
MRT bei atypischen Parkinson-Syndromen
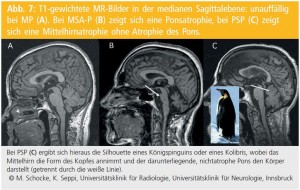
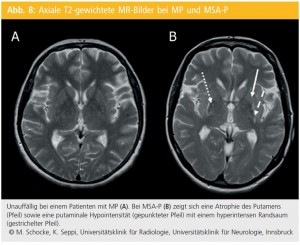
Die größte Wertigkeit der MRT besteht in der Differenzialdiagnose von neurodegenerativen Parkinson-Syndromen. Bis heute konnten mehrere Strukturveränderungen bei PatientInnen mit MSA, PSP und CBD in der MRT beschrieben werden; einige von diesen Veränderungen besitzen eine hohe Spezifität (Abb. 7 und 8). Hingegen beträgt die Gesamt- Sensitivität in Abhängigkeit von der Erkrankungsdauer und dem Krankheitsstadium nur etwa 60–80 %.
Die in den folgenden Abschnitten beschriebenen Veränderungen in T1- und T2-Sequenzen bei aPS können jedoch in frühen Krankheitsstadien und bei Erstmanifestation fehlen. Hier scheint die Verwendung diffusionsgewichteter MRT, die bei MSA-P und seltener bei PSP eine Gewebsschädigung im Putamen zeigen kann, sensitiver zu sein. Die Tabellen 4 bis 6 fassen die typischen Abnormitäten in der MRT bei PatientInnen mit aPS zusammen. Die meisten der bislang durchgeführten MRT-Studien bei PatientInnen mit aPS bedienten sich klinischer Diagnosekriterien ohne neuropathologische Verifizierung, somit können Fehldiagnosen nicht ausgeschlossen werden. Da klinisch die diagnostische Treffsicherheit in späten Krankheitsstadien höher als in frühen ist, wurden vorwiegend PatientInnen in fortgeschrittenen Krankheitsstadien untersucht. Daten zur MRT-gestützten Diagnosefindung in frühen Krankheitsstadien fehlen weitgehend.
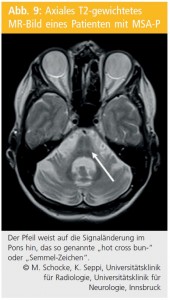
Multisystematrophie (MSA): Pathognomonische MRT-morphologische Veränderungen, welche die Diagnose einer MSA-P favorisieren, sind ein hyperintenser putaminaler Randsaum in T2-Sequenzen, der häufig in Kombination mit einer putaminalen T2-Hypointensität auftritt, sowie eine striatale Atrophie mit Betonung des dorsolateralen Putamens. Für eine MSA-C sprechen hingegen Veränderungen in den infratentoriellen Hirnregionen wie Atrophie von Zerebellum, des mittleren Kleinhirnstiels (MCP, middle cerebellar peduncle) und des Pons sowie eine pontine T2-Veränderung in Form einer in axialen Ausrichtung positionierten Kreuzformation (Semmelzeichen, „hot cross bun sign“, Abb. 9).
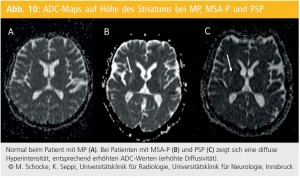
Eine Studie konnte anhand von 3,0-T-MRUntersuchungen jedoch zeigen, dass der T2- hyperintense putaminale Randsaum auch bei gesunden Kontrollen beobachtet werden kann und somit bei diesen Feldstärken womöglich als unspezifisches Zeichen unklarer pathologischer Relevanz zu werten ist. Im letzten Jahrzehnt gab es wachsendes Interesse an der diffusionsgewichteten Bildgebung zur Differenzialdiagnose der MSA. Insbesondere scheinen sich die putaminalen Veränderungen bei der MSA-P bereits früh im Krankheitsverlauf durch eine erhöhte Diffusivität im Putamen darzustellen. So wurden in diversen Studien MSA-P-PatientInnen mit einer Krankheitsdauer von 3 bis zu 6 Jahren mit einer hohen diagnostischen Treffsicherheit gegenüber MP-PatientInnen und gesunden Kontrollen abgegrenzt. Vorsicht ist bei der Unterscheidung der MSAP von der PSP geboten, da auch diese Entität regelmäßig mit Erhöhung der putaminalen Diffusivität einhergehen kann (Abb. 10).
Außerdem führen chronisch vaskuläre Veränderungen der Basalganglien zu einer Erhöhung der Diffusivität, was aufgrund ihrer Häufigkeit oft Schwierigkeiten bei der Interpretation dieses Parameters bereiten kann. Eine abnorm erhöhte Diffusivität findet sich auch in anderen Hirnstrukturen wie im MCP, Pons und Zerebellum, wobei supratentorielle Veränderungen im Bereich der Basalganglien auf eine MSA-P, infratentorielle Veränderungen auf eine MSA-C hinweisen.
Progressive supranukleäre Paralyse (PSP): Passend zu den neuropathologischen Veränderungen bei der PSP zeigen sich in der MRT eine Atrophie des Mittelhirns, besonders im Bereich von Mittelhirnhaube und Mittelhirndach (Tegmentum und Tectum), sowie Strukturpathologien der oberen Kleinhirnstiele (SCP, superior cerebellar peduncle) und der unteren Olive. Zusätzlich findet sich eine Substanzminderung im Frontal- und Temporallappen. Aus der Atrophie des Mittelhirns mit Abflachung und Eindellung der rostrodorsalen Mittelhirnhaube und daraus folgender Größenzunahme des dritten Ventrikels resultiert bildmorphologisch in der medianen Sagittalschicht das sogenannte „Kolibri- oder Königspinguin-Zeichen“ („king pinguin sign“, „humming bird sign“, Abb. 7C).
Dieses Zeichen findet sich kaum bei PatientInnen mit anderen neurodegenerativen Parkinson- Syndromen, weshalb ein Vorhandensein dieses „Kolibri-Zeichens“ spezifisch für die PSP zu sein scheint, obschon dieses Zeichen bei bis zur Hälfte der PSP-PatientInnen, insbesondere in weniger fortgeschrittenen Stadien, fehlen kann.
Zusätzlich konnte durch eine planimetrische Ausmessung der mittsagittalen Mittelhirn- und Ponsfläche alleine, oder in Kombination mit dem Verhältnis zwischen Breite der oberen und mittleren Kleinhirnstiele (MR-Parkinsonism Index, MRPI, d. h. Ponsfläche/Mittelhirn x MCP-Durchmesser/SCP-Durchmesser) ein Diskriminator zwischen PSP und anderen neurodegenerativen Parkinson-Syndromen beschrieben werden. Welche Ausmessungen und daraus errechneten Ratios wirklich die diagnostische Treffsicherheit, insbesondere in Frühstadien der Erkrankungen, zu erhöhen vermögen, bleibt vorerst offen.
Wie regelmäßig bei der MSA-P, kann es in diffusionsgewichteten Sequenzen bei der PSP zu einem Anstieg der putaminalen Diffusivität kommen, so dass hohe Werte mit denen der MSA und niedrige Werte mit denen des MP überlappen können. Des Weiteren haben einige kleine Studien eine PSP-spezifische Zunahme der Diffusivität im SCP gezeigt. Es bedarf allerdings weiterer Studien, bevor dieses Zeichen für die routinemäßige Abklärung von Parkinson-Syndromen herangezogen werden kann. Die meisten MRT-Studien wurden mit RS-PatientInnen durchgeführt, wohingegen die eigentliche Schwierigkeit in der Diagnose der sich atypisch präsentierenden PSP-P liegt. Inwieweit sich die oben genannten MRI-Marker auch bei anderen PSP-Formen nachweisen lassen, muss durch entsprechende Studien aufgedeckt werden.
Kortikobasale Degeneration (CBD): Wenige Studien haben sich mit MRT-Veränderungen bei der CBD befasst. In Übereinstimmung mit der Neuropathologie findet sich typischerweise eine asymmetrische, kontralateral zur klinisch stärker betroffenen Seite ausgeprägte, frontoparietale kortikale Atrophie, gelegentlich kommt aber auch eine symmetrische Globalatrophie vor. Veränderungen der Basalganglien können häufig fehlen, obschon manchmal eine Atrophie des Putamens imponieren kann. Des Weiteren kann sich das Mittelhirn in der MRT atrophisch zeigen, Marklagergliosen können häufig gefunden werden und demarkieren sich als kleine T2- Hyperintensitäten der angrenzenden weißen Substanz. Noch limitierter ist die Studienlage für die diffusionsgewichtete Bildgebung bei der CBD. Eine erhöhte Diffusivität wurde im Putamen beschrieben, interessanterweise aber auch in asymmetrischer Weise in den Hemisphären. In Anbetracht der klinischen Heterogenität der CBD muss hier die MRTStudienlage allerdings mit kritischem Auge betrachtet werden.
Demenz mit Lewy-Körperchen (DLB): Während sich beim MP in frühen Erkrankungsstadien in der MRT bei den Routinesequenzen in der Regel ein altersentsprechender normaler Befund findet, weisen PatientInnen mit DLB und MP-PatientInnen mit Demenz (PDD, Parkinson’s disease with dementia) häufig eine Atrophie subkortikaler Strukturen bei relativem Erhalt des medialen Temporallappens auf. Dieses Atrophie-Muster unterscheidet die DLB von der Alzheimer-Erkrankung, bei welcher sich häufig bereits in Frühstadien eine Atrophie des medialen Temporallappens mit der Hippocampusformation findet. Während sich der Erhalt des medialen Temporallappens in der MRT womöglich als differenzierender Marker zwischen DLB und Alzheimer-Erkrankung etablieren könnte und bereits Einzug in die revidierten Konsensuskriterien für die klinische Diagnose der DLB gefunden hat, lassen sich die DLB und die PDD mittels MRT nicht unterscheiden.
MRT zum Ausschluss sekundärer Parkinson-Syndrome
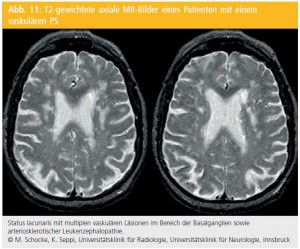
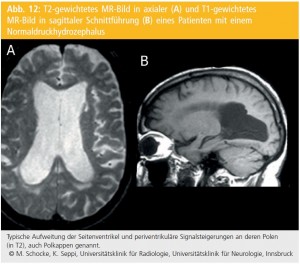
T1- und T2-gewichtete Untersuchungen finden ihre Anwendung in der Differenzialdiagnose von sekundären oder symptomatischen PS. Diese können auf dem Boden von Raumforderungen im Bereich der Basalganglien, des Hirnstamms oder des frontalen Marklagers durch strategische vaskuläre Läsionen (Mikro- und Makroangiopathien) oder im Rahmen eines Normaldruckhydrozephalus entstehen. Da für die zugrunde liegende Ursache eines sekundären PS therapeutische sowie zum Teil heilende Maßnahmen bestehen, erfordern diese Parkinson-Syndrome eine diagnostische Abklärung unter Einbeziehung von Befunden der zerebralen Bildgebung (Abb. 11 und 12).
Lakunäre Infarkte im Bereich der Basalganglien, Frontalhirninfarkte oder eine subkortikale, meistens frontal betonte Leukenzephalopathie können Ursachen eines vaskulären PS sein. Die Entwicklung der Symptome gestaltet sich je nach zugrunde liegender Erkrankung schleichend auf dem Boden einer subkortikalen arteriosklerotischen Enzephalopathie (SAE) oder (sub-)akut bei lakunären Hirninfarkten, die den externen Teil des Globus pallidus, Teile des Thalamus oder selten die Substantia nigra betreffen. Für die Diagnosestellung muss hierbei ein zeitlicher Zusammenhang zwischen Auftreten der motorischen Symptome und den vaskulären Läsionen bestehen. Ein Normaldruckhydrozephalus manifestiert sich klinisch in einer frontalen Gangstörung mit begleitender subkortikaler Demenz sowie Inkontinenz; man spricht auch vom „lower body parkinsonism“, da hierbei die Gangstörung im Vordergrund steht und selten eine Tremorkomponente beobachtet wird.
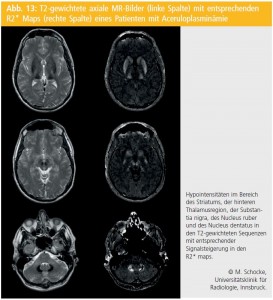
Seltene Ursachen: Des Weiteren können seltene Ursachen wie fokale Läsionen im Rahmen einer multiplen Sklerose, die Wilson- Krankheit, striatopallidodentale Kalzinose bei Morbus Fahr, das manganassoziierte PS und die Neurodegeneration mit Eisenablagerungen im Gehirn (Neurodegeneration with brain iron accumulation, NBIA-Syndrom) oder Morbus Huntington (Westphal-Variante) ursächlich für ein symptomatisches PS sein. Die neuronale Schädigung durch erhöhte Kupferablagerungen beim Morbus Wilson spiegelt sich typischerweise in der MRT in einer Mittelhirnatrophie mit T2/FLAIR-Signalanhebung in der Mittelhirnhaube („Pandabär- Zeichen“) und in randständig betonten T2-Hyperintensitäten in Putamen, Pallidum, Nucleus caudatus bzw. entlang der Pyramidenbahn wider. Schädigungen der Basalganglien durch Eisenablagerungen bei NBIA-Syndromen zeigen in der MRT hingegen typischerweise herabgesetzte Signalintensitäten in Putamen, Nucleus caudatus, Thalamus und Pallidum, wobei bei der PKAN (Pantothenate kinase-associated neurodegeneration), einer Form dieser Syndrome, eine Hyperintensität im inneren Segment des Globus pallidus auftritt und als „Tigerauge-Zeichen“ („Eye of the tiger“) beschrieben wird. Daneben sind die verminderten Signalintensitäten bei der PKAN meist auf den Globus pallidus und die SN begrenzt, während sich die Hypointensitäten bei der Neuroferritinopathie und der Acoerulinoplasminämie (anderen Formen von NBIA-Syndromen, Abb. 13), aber auch in anderen Kerngebieten, wie im Striatum, Thalamus oder Nucleus dentatus finden. Symmetrische Kalzinosen der Basalganglien, des Nucleus dentatus und des periventrikulären Marklagers im Rahmen einer striatodentalen Kalzifikation (Morbus Fahr) demarkieren sich in der MRT unter Umständen nur unzureichend, hier sollte ergänzend eine zerebrale CT durchgeführt werden.
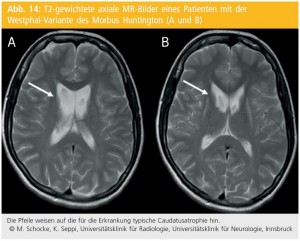
Die Westphal-Variante der Huntington-Erkrankung präsentiert sich häufig mit einem juvenilen PS, in der MRT findet sich typischerweise eine Atrophie von Nucleus caudatus und Putamen sowie eine kortikale, frontal betonte Atrophie (Abb. 14). Schließlich können auch Toxin-assoziierte PS mit MRT-Signalalterationen der Basalganglien einhergehen, z. B. zeigen sich bei chronischer Manganexposition im T1-gewichteten Bild häufig Hyperintensitäten im Globus pallidus.
Transkranielle Weichteilsonographie
Die transkranielle B-Mode-Doppler-Sonographie (TCS, transcranial sonography) kann dazu verwendet werden, über das temporale akustische Knochenfenster Hirnparenchym darzustellen und das Ausmaß eines echogenen Signals im Bereich der Substantia nigra oder der Basalganglien zu beurteilen. Das Mittelhirn kommt hierbei als schmetterlingsartig geformte Struktur zur Darstellung. Die TCS kann neben klinisch-neurologischer Untersuchung sowie struktureller und funktioneller Bildgebung mittels MRT und SPECT-Verfahren als zusätzliche nichtinvasive und kosteneffiziente Untersuchung bei der Differenzierung von Parkinson-Syndromen eingesetzt werden. Nachdem ein ausreichendes temporales Knochenfenster Voraussetzung für die TCS ist, kann diese Methode jedoch bei über 10 % der Bevölkerung nicht angewendet werden. Die sonographische Darstellung der Basalganglien besitzt vor allem beim MP eine geringere Wertigkeit; bei aPS kann, wie im folgenden Absatz angeführt, eine Hyperechogenität in diesem Bereich diagnostische Hinweise auf die Erkrankung geben.
Hyperechogenität in der Substantia nigra: Durch die Darstellung einer Hyperechogenität im Bereich der Substantia nigra bei PatientInnen mit MP wird die TCS seit 1995 routinemäßig zur Diagnostik von Bewegungsstörungen verwendet. Dabei geht es um die hyperechogene Fläche, die ab einer gewissen Größe als pathologisch beurteilt werden kann, wobei in der Literatur für die Grenzwerte einer Hyperechogenität im Bereich der Substantia nigra (SN+) unterschiedliche Werte berechnet wurden. Während manche Studien als Cut-off für eine SN+ die dritte Quartile der größeren Ausdehnung der Echogenitäten im Bereich beider SN einer gesunden Kontrollpopulation verwendet haben, wurden bei anderen Studien der Mittelwert plus eine Standardabweichung der größeren der beiden Echogenitäten im Bereich der SN einer gesunden Kontrollpopulation als Grenzwert verwendet.
Bei ungefähr 90 % der PatientInnen mit MP kann eine SN+ nachgewiesen werden. Die Ausdehnung des echogenen Signals ist dabei unabhängig vom Alter der PatientInnen, von Dauer und Schweregrad der Erkrankung, korreliert nicht mit dem Grad der striatalen Dopamintransporterverfügbarkeit und zeigt keine Progression im Laufe der Erkrankung. Trotzdem ist die Hyperechogenität auf der kontralateral zur klinisch stärker betroffenen Seite meistens größer.
Allerdings haben auch bis zu 15 % der gesunden Bevölkerung eine vermehrte Echogenität in der SN, Familienangehörige 1. Grades können sogar noch häufiger pathologische Befunde zeigen. Eine prospektive verblindete Studie an 60 neuerkrankten PatientInnen mit PS (von denen im Follow-up nach einem Jahr 43 PatientInnen als MP und 13 PatientInnen als aPS klassifiziert wurden, 4 weitere hatten kein Parkinson-Syndrom im Follow-up) ergab eine diagnostische Wertigkeit des Markers SN+ von 88,3 % für die Diagnose eines MP, wobei die Sensitivität bei 90,7 % und die Spezifität bei 82,4 % lag. Für die Differenzierung zwischen MP und aPS ergaben sich Werte für Sensitivität und Spezifität von 94,8 % bzw. 90 % bei einem positiv prädiktiven Wert von 97,4 %.
Häufig findet sich bei PatientInnen mit aPS eine vermehrte Hyperechogenität uni- oder bilateral in den Basalganglien, insbesondere im Linsenkern. Allerdings scheint die diagnostische Wertigkeit einer Hyperechogenität im Bereich der Basalganglien unzureichend zu sein, wie oben genannte Arbeit an den 60 neuerkrankten PatientInnen mit PS gezeigt hat. Die diagnostische Wertigkeit einer Hyperechogenität im Bereich der Basalganglien bei PatientInnen mit aPS wurde dabei mit 68,2 % beziffert, bei einer Sensitivität von 66,7 % und einer Spezifität von 68,6 %.
Resümee
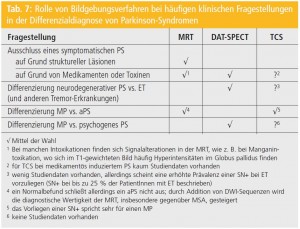
PatientInnen mit neurodegenerativen Parkinson- Syndromen stehen heutzutage einem großen Armamentarium von diagnostischen Untersuchungstechniken struktureller und funktioneller Natur gegenüber. Tabelle 7 fasst die Rolle von Bildgebungsverfahren bei häufigen klinischen Fragestellungen zusammen. Eine genaue Diagnose ist für PatientInnen dabei von großer therapeutischer und prognostischer Relevanz. Bis auf die DAT-SPECT-Untersuchung sind die weiteren nuklearmedizinischen Untersuchungsmethoden wie IBZM-SPECT und PET-Verfahren hauptsächlich wissenschaftlichen Fragestellungen vorbehalten. Zu den wichtigsten Indikationen für die DAT-SPECT-Untersuchung in der Klinik gehören die Frühdiagnose des MP bei fraglicher und asymptomatischer Symptomausprägung sowie die Differenzierung neurodegenerativer Parkinson- Syndrome (MP und aPS) von nichtdegenerativen Parkinson- und Tremor-Syndromen. Eine Differenzierung zwischen MP und aPS ist freilich mittels DAT-SPECT-Untersuchung nicht möglich. Allerdings kann aber die Unterscheidung von Alzheimer-Erkrankung und DLB erhebliche therapeutische Konsequenzen (evtl. L-Dopa-Therapie, Wahl eines Neuroleptikums) mit sich bringen und so die DATSPECT- Untersuchung eine sinnvolle klinische Indikation sein. Tabelle 2 zeigt typische SPECT/PET-Befunde bei häufigen Parkinson- und Tremor-Syndromen.
Die Domäne der strukturellen Bildgebung mittels MRT in der Parkinson-Diagnostik ist der Ausschluss symptomatischer Formen durch Läsionen im Bereich der Basalganglien, des Hirnstamms oder des frontalen Marklagers sowie der Ausschluss eines Normaldruckhydrozephalus. Beim MP zeigt die MRT in der Regel keine spezifischen Zeichen einer Neurodegeneration, bei den aPS hingegen können sich spezifische bildgebende Zeichen demarkieren. So finden sich infra- und supratentoriell bei PatientInnen mit MSA und PSP häufig charakteristische Atrophiemuster bzw. Veränderungen der Signalintensität, und beim CBS lässt sich häufig eine asymmetrische, kontralateral zur klinisch stärker betroffenen Seite ausgeprägte, frontoparietale kortikale Atrophie detektieren. Nützlich in der Differenzierung der DLB von der Alzheimer- Demenz kann außerdem der Nachweis einer Atrophie subkortikaler Strukturen bei relativem Erhalt des medialen Temporallappens sein. Tabelle 6 fasst nützliche MRT-Marker bei 1,5 Tesla als Hilfestellung zur Diagnose der neurodegenerativen PS zusammen. Unter den neueren Verfahren ist die DWI zurzeit am meisten etabliertet, Änderungen in der Diffusivität können bei der MSA und der PSP womöglich früh im Krankheitsverlauf auftreten und wurden besonders im Bereich des Putamen bereits in mehreren Studien beschrieben. Rezente Studien beim MP zur Beurteilung des Eisengehaltes und der fraktionellen Anisotropie in der SN mittels 3-T-MRT sind als experimentell zu werten. Trotz der starken Untersucherabhängigkeit sowie der mangelnden Durchführbarkeit bei eingeschränkten Schallbedingungen kann die TCS im Kontext mit klinischen und anderen Untersuchungsergebnissen als eine sinnvolle Erweiterung der diagnostischen Maßnahmen in der Differenzialdiagnose von Parkinson- Syndromen angesehen werden, da das Bestehen einer SN+ für das Vorliegen eines MP spricht. Allerdings sind weiterführende Validierungsstudien gegenüber klinischen Standards erforderlich. Die mehrfach berichtete erhöhte Prävalenz einer SN+ bei PatientInnen mit essenziellem Tremor von bis zu 25 % scheint sich bereits als limitierender Faktor der Technik herauszukristallisieren.
Literatur bei den Verfassern
Empfohlene Literatur:
– Berg D, Godau J, Walter U, Transcranial sonography in movement disorders. Lancet Neurol. Nov 2008; 7(11):1044–1055.
– Berg D, Steinberger JD, Warren Olanow C, Naidich TP, Yousry TA, Milestones in magnetic resonance imaging and transcranial sonography of movement disorders. Mov Disord. May 2011; 26(6):979–992.
– Brooks DJ, Pavese N, Imaging biomarkers in Parkinson’s disease. Prog Neurobiol 2011; 95:614–628.
– Brooks DJ, Seppi K, MSA NWGo, Proposed neuroimaging criteria for the diagnosis of multiple system atrophy. Mov Disord 2009; 24(7):949–964.
– Gaenslen A, Unmuth B, Godau J, et al., The specificity and sensitivity of transcranial ultrasound in the differential diagnosis of Parkinson’s disease: a prospective blinded study. Lancet Neurol. May 2008; 7(5):417–424.
– Gibb WR, Lees AJ, The relevance of the Lewy body to the pathogenesis of idiopathic Parkinson’s disease. J Neurol Neurosurg Psychiatry. Jun 1988; 51(6):745–752.
– Hotter A, Esterhammer R, Schocke MF, Seppi K, Potential of advanced MR imaging techniques in the differential diagnosis of parkinsonism. Mov Disord. 2009; 24 (Suppl 2):S711–S720.
– Kägi G, Bhatia KP, Tolosa E, The role of DAT-SPECT in movement disorders. J Neurol Neurosurg Psychiatry 2010; 81:5–12.
– Litvan I, Bhatia KP, Burn DJ et al., Movement Disorders Society Scientific Issues Committee report: SIC Task Force appraisal of clinical diagnostic criteria for Parkinsonian disorders. Mov Disord. May 2003; 18(5):467–486.
– Mahlknecht P, Hotter A, Hussl A, Esterhammer R, Schokke M, Seppi K, Significance of MRI in diagnosis and differential diagnosis of Parkinson’s disease. Neurodegener Dis 2010; 7(5):300–318.
– Mahlknecht P, Schocke M, Seppi K (Differential diagnosis of parkinsonian syndromes using MRI), Nervenarzt. Oct 2010; 81(10):1168–1179.
– Marshall V, Grosset D, Role of dopamine transporter imaging in routine clinical practice. Mov Disord 2003; 1415–1418.
– Oertel WH, Reichmann H, Kapitel Parkinson-Syndrome: Diagnostik und Therapie. Aus: Leitlinien für Diagnostik und Therapie in der Neurologie. Herausgebende Autoren: Diener HC, Putzki N, Georg Thieme Verlag, 4. überarbeitete Auflage 2008. S. 82ff.
– Perju-Dumbrava L, Kovacs GG, Pirker S et al., Dopamine transporter imaging in autopsy-confirmed Parkinson’s disease and multiple system atrophy. Mov Disord 2012; 27:65–71.
– Pirker W, Scherfler C, Brücke T, Poewe W und der wissenschaftliche Beirat der ÖPG. Klinische Indikationen für SPECT-Untersuchungen bei Bewegungsstörungen. Paktuell 3/2005:2–11. Online: http://www.parkinson.at/fileadmin/p-aktuell/2005/Paktuell_ Dez_05.pdf
– Pirker W, Correlation of dopamine transporter imaging with Parkinsonian motor handicap – how close is it? Mov Disord 2003; 18(Suppl 7):43–51. – Poewe W, Deuschl G, Kapitel 2 Parkinson-Krankheit, Kap. 2.2 Diagnose und Differentialdiagnose. Aus: Parkinson- Syndrome und andere Bewegungsstörungen. Herausgebende Autoren: Oertel WH, Deuschl G, Poewe W, Georg Thieme Verlag 2012; S. 50ff.
– Poewe W, Scherfler C, Role of dopamine transporter imaging in investigation of parkinsonian syndromes in routine clinical practice. Mov Disord 2003; 18(Suppl 7):16–21.
– Scherfler C, Seppi K, Kapitel 29 Diagnostische Verfahren bei Bewegungsstörungen, Kap. 29.1.3 Magnetresonanztomografie. Aus: Parkinson-Syndrome und andere Bewegungsstörungen. Herausgebende Autoren: Oertel WH, Deuschl G, Poewe W, Georg Thieme Verlag 2012; S. 577ff. – Scherfler C, Kapitel 29 Diagnostische Verfahren bei Bewegungsstörungen, Kap. 29.1.1 Single-Photon-Emissionstomografie. Aus: Parkinson-Syndrome und andere Bewegungsstörungen. Herausgebende Autoren: Oertel WH, Deuschl G, Poewe W, Georg Thieme Verlag 2012; S. 574ff.
– Schuff N, Potential role of high-field MRI for studies in Parkinson’s disease. Mov Disord 2009; 24 (Suppl 2):S684–S690.
– Seppi K, Poewe W, Brain magnetic resonance imaging techniques in the diagnosis of parkinsonian syndromes. Neuroimaging Clin N Am. Feb 2010; 20(1):29-55.
– Stockner H, Kapitel 29 Diagnostische Verfahren bei Bewegungsstörungen, Kapitel 29.1.4 Transkranielle Sonografie. Aus: Parkinson-Syndrome und andere Bewegungsstörungen. Herausgebende Autoren: Oertel WH, Deuschl G, Poewe W, Georg Thieme Verlag 2012; S. 579.
– Wadia PM, Lang A, The many faces of corticobasal degeneration. Parkinsonism Relat Disord 2007; 13(suppl 3):S336–S340.
– Walker Z, Jaros E, Walker RWH et al. Dementia with Lewy bodies: a comparison of clinical diagnosis, FP-CIT single photon emission computed tomography imaging and autopsy. J Neurol Neurosurg Psychiatry 2007; 78:1176–1181.
– Wenning GK, Colosimo C, Geser F, Poewe W, Multiple system atrophy. Lancet Neurol Feb 2004; 3(2):93–103.
– Williams DR, Lees AJ, Progressive supranuclear palsy: clinicopathological concepts and diagnostic challenges. Lancet Neurol 2009; 8(3):270–9.
– Williams DR, Lees AJ, How do patients with parkinsonism present? A clinicopathological study. Intern Med J 2009; 39:7–12.
| Abkürzungen: | |||
| A | Fläche | OPCA | olivo-ponto-zerebelläre Atrophie |
| aPS | atypisches Parkinson-Syndrom | PD | proton density, Protonen-Dichte |
| CBD | Kortikobasale Degeneration | PDD | Parkinson-Demenz, Parkinson’s Disease with dementia |
| CBS | Kortikobasales Syndrom | PET | positron emission tomography |
| CT | Computertomographie | PKAN | Pantothenate kinase-associated neurodegeneration |
| D | Durchmesser | PS | Parkinson-Syndrom |
| DAT r | Dopamintransporte | PSP | progressive supranukleäre Paralyse |
| DLB | Demenz mit Lewy-Körperchen | RS | Richardson-Syndrom |
| DRD | Dopa-responsive Dystonie | SAE | subkortikale arteriosklerotische Enzephalopathie |
| DTI | diffusion tensor imaging | SCA | Spinozerebelläre Ataxie |
| DWI g | diffusion weighted imagin | SCP | superior cerebellar peduncle |
| FDG | 18F-Fluordesoxyglukose | SN | Substantia nigra |
| IBZM | I-123-Iodobenzamid | SND | striatonigrale Degeneration |
| LBP | Lower Body Parkinsonism | SPECT | single photon emission tomography |
| MCP | middle cerebellar peduncle | SWEDD | scans without evidence for dopaminergic deficit |
| MP | Morbus Parkinson | T | Tesla |
| MRPI | MR-Parkinson-Index | TCS | transkranielle Sonographie |
| MRT | Magnetresonanztomographie | VBM | voxelbasierte Morphometrie |
| MSA | Multisystematrophie | ZNS | Zentralnervensystem |
| NBIA | Neurodegeneration Brain Iron Accumulation | ||