Anti-HER2-Therapie interdisziplinär betrachtet
In den aktuellen 1. Internationalen Konsensus-Guidelines für das fortgeschrittene Mammakarzinom (ABC1)1 wird die Bedeutung eines interdisziplinären Zugangs bei der Betreuung von Brustkrebspatientinnen betont. Unter dem Vorsitz von Univ.-Prof. Dr. Michael Gnant, Medizinische Universität Wien, diskutierten bei einem Symposium im Rahmen des ESMO 2012* Onkologen, eine spezialisierte onkologische Schwester und ein Psychologe die Therapie des HER2-positiven metastasierten Mammakarzinoms aus den unterschiedlichen Blickwinkeln.
Lebensverlängerung durch Anti-HER2-Therapien
Jene rund 25–30 % der Mammakarzinompatientinnen, bei denen der humane epidermale Wachstumsfaktorrezeptor 2 (HER2) überexprimiert ist, haben eine schlechtere Prognose sowohl in Hinblick auf das Gesamtüberleben als auch das Risiko für viszerale Rezidive. Wie Dr. Hope S. Rugo, University of California, San Francisco, USA, ausführte, befasst sich die onkologische Forschung derzeit intensiv mit Strategien zur Beeinflussung von HER2 und der nachgeschalteten Signalwege (Abb. 1).
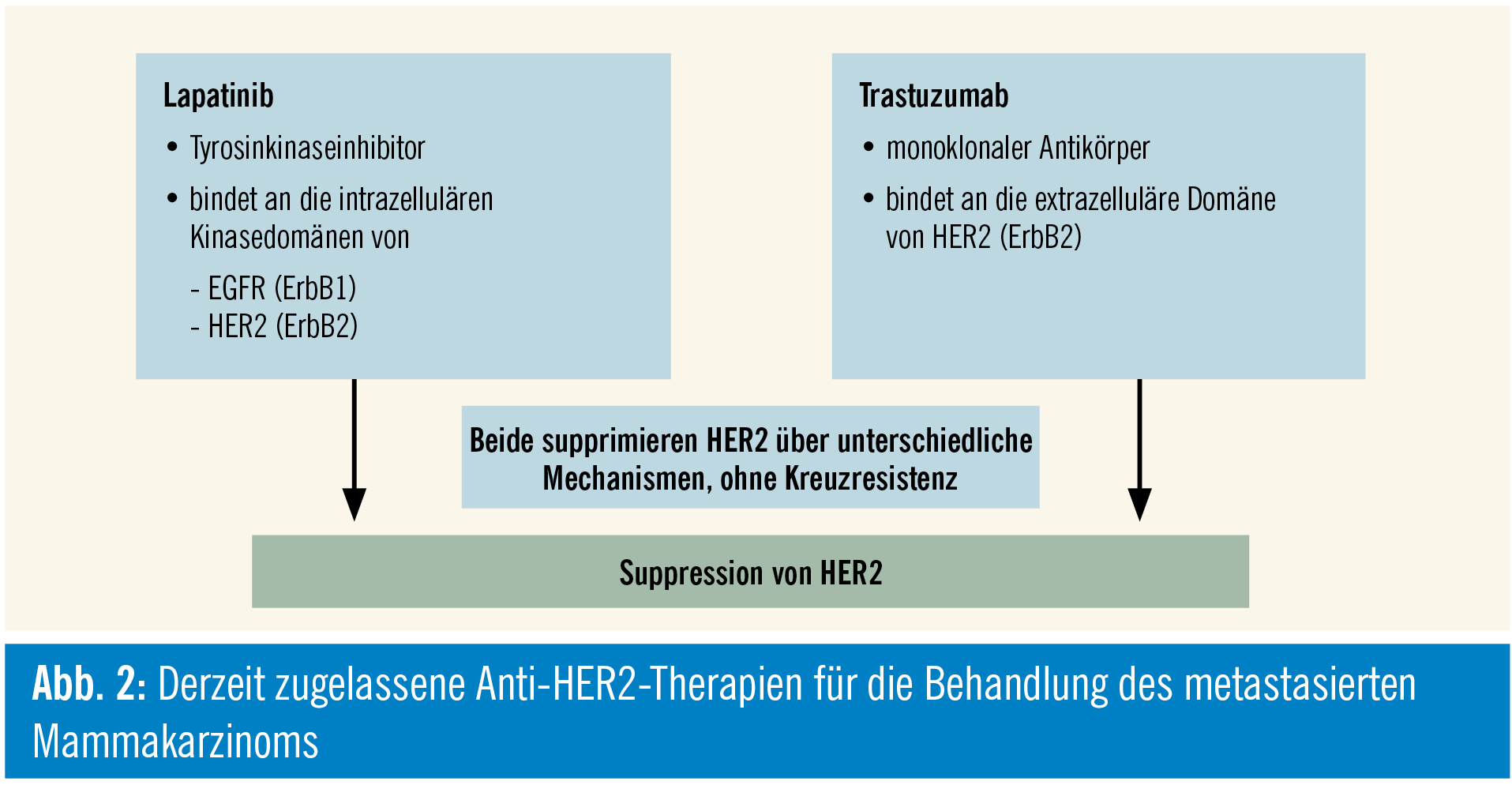
Derzeit sind in Europa mit dem Tyrosinkinaseinhibitor Lapatinib und dem monoklonalen Antikörper Trastuzumab zwei zielgerichtete Therapien zugelassen, die HER2 supprimieren (Abb. 2). In den USA hat auch Pertuzumab eine entsprechende Zulassung. Diese drei Substanzen bringen für Patientinnen mit HER2-positivem Mammakarzinom einen Lebenszeitgewinn.
Trastuzumab, Pertuzumab: Trastuzumab ist zur Behandlung von Patienten mit HER2-positivem metastasiertem Brustkrebs indiziert als Monotherapie zur Behandlung von Patienten, die mindestens zwei Chemotherapieregime gegen ihre metastasierte Erkrankung erhalten haben, bzw. in der First-Line-Therapie als Kombination mit Paclitaxel oder Docetaxel. Trastuzumab verlängert in Kombination mit einer Chemotherapie das Überleben von Patientinnen mit HER2-positivem, lokal fortgeschrittenem oder mit metastasiertem Mammakarzinom um mehrere Monate im Vergleich zu einer alleinigen Chemotherapie2, 3.
Der monoklonale Antikörper Pertuzumab bindet an einer anderen Region von HER2 als Trastuzumab. In Kombination mit Trastuzumab und Docetaxel verlängerte Pertuzumab das progressionsfreie Überleben von Patientinnen mit HER2-positivem metastasiertem Mammakarzinom im Vergleich zu Trastuzumab/Docetaxel von 12,4 auf 18,5 Monate (p < 0,001; CLEOPATRA-Studie)4. Ein beträchtlicher Teil der Patientinnen mit HER2-positivem Mammakarzinom entwickelt jedoch eine Resistenz gegen die Anti-HER2-Therapie oder ist intrinsisch resistent5.
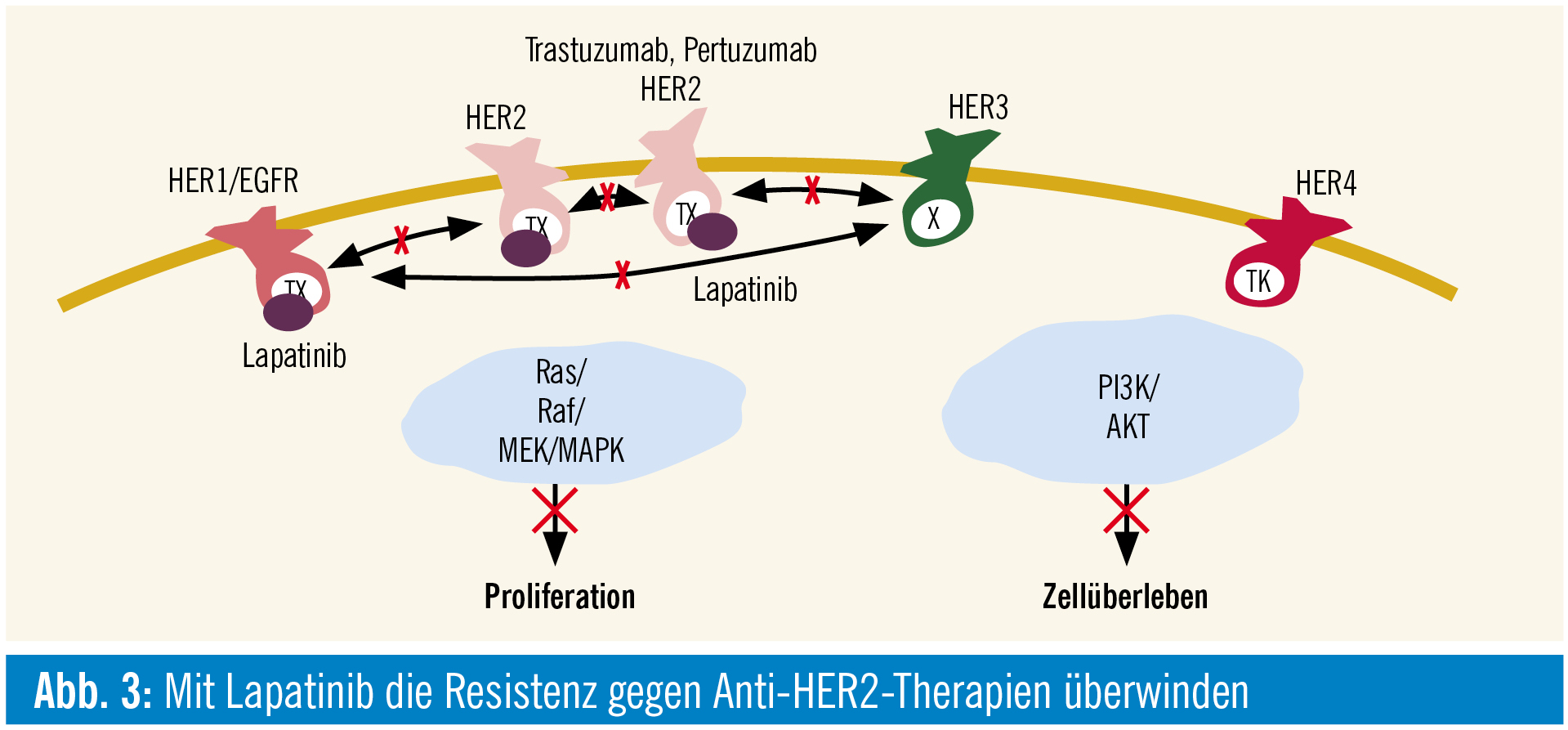
Lapatinib: Lapatinib ist als einziger Wirkstoff für die Anwendung nach Trastuzumabversagen zugelassen und ist in der Lage, die Resistenz gegen Anti-HER2-Therapien zu überwinden (Abb. 3). Lapatinib bindet an die intrazelluläre Kinasedomäne von EGFR1 („epidermal growth factor receptor 1“) und HER2 und inhibiert die nachgeschalteten MAPK- und PI3K-Signalwege.
Bei Patientinnen, bei denen es unter Anthrazyklin und Trastuzumab zu einer Progression gekommen war, bzw. bei Patientinnen mit Trastuzumabversagen im metastasierten Setting verbesserte Lapatinib/Capecitabin das progressionsfreie Überleben im Vergleich zu Capecitabin alleine von 4,3 auf 6,2 Monate (p = 0,0001)6. Das Gesamtüberleben war in beiden Gruppen vergleichbar.
Wie Blackwell et al.7 in einer rezent publizierten Studie zeigen konnten, verlängert Lapatinib in Kombination mit Trastuzumab im Vergleich zu Lapatinib alleine das mediane Gesamtüberleben um 4,5 Monate. Die Patienten des Kombinationsarms waren bereits mit durchschnittlich drei Linien Trastuzumab und fünf Linien Chemoterapie vorbehandelt.
Lapatinib/Capecitabin erwies sich auch bei Patientinnen mit unbehandelten Hirnmetastasen als wirksam (LANDSCAPE-Studie). Bei 20,5 % der Patientinnen konnte eine ≥ 80%ige Reduktion des Metastasenvolumens erreicht werden, bei 45,5 % eine Reduktion um 50–80 %; nur bei 15,9 % der Patientinnen kam es zu einer Progression8. ZNS-Metastasen treten relativ früh im Krankheitsverlauf auf. Die Patientinnen haben immer noch einer Lebenserwartung von bis zu 1–2 Jahren, wie Dr. Thomas Bachelot, Centre Léon Bérard, Lyon, Frankreich, berichtete. Die Ganzhirnbestrahlung als Standardtherapie für viele Patientinnen mit Hirnmetastasen führt bei 31–57 % der Patienten zu neurokognitiven Beeinträchtigungen9. Eine systemische Therapie bietet nicht nur die Chance, die Ganzhirnbestrahlung hinauszuzögern. Eine retrospektive Analyse von Bartsch et al. konnte darüber hinaus zeigen, dass die zusätzliche Gabe von Lapatinib im Gegensatz zur alleinigen Therapie mit Trastuzumab das Überleben von Patientinnen mit HER2-positivem Mammakarzinom und Hirnmetastasen verlängert (p = 0,002). Die Lapatinibtherapie war ein unabhängiger positiver Prädiktor für das Überleben10.
Lapatinib ist auch in Kombination mit einem Aromatasehemmer zur Behandlung postmenopausaler Patientinnen mit Hormonrezeptor- und HER2-positivem metastasiertem Brustkrebs zugelassen, die nicht für eine Chemotherapie vorgesehen sind11.
Beforschte Therapieoptionen: Als weitere Therapieoptionen werden derzeit unter anderem T-DM1, Everolimus, Neratinib und Afatinib evaluiert. T-DM1 verlängerte das progressionsfreie Überleben nach Trastuzumab/Taxan-Versagen von 6,4 auf 9,6 Monate (p < 0,0001; EMILIA-Studie)12. Everolimus wird derzeit als Second-Line-Behandlung des HER2-positiven Mammakarzinoms untersucht (BOLERO 1, BOLERO 3).
Management von Nebenwirkungen
Diarrhö: Unter Lapatinib entwickeln rund zwei Drittel der Patienten eine Diarrhö, in den meisten Fällen vom Grad 1 oder 2. Bei 42 % der Patienten trat die erste Episode innerhalb von 6 Tagen nach Beginn der Lapatinibtherapie auf6. Meist war die Symptomatik mit einer Standardtherapie, beispielsweise mit Loperamid beherrschbar.
Hautausschläge: Ein weiteres Problem sind Hautausschläge, die in der Regel gering ausgeprägt sind. Bereits vor Beginn einer Therapie mit Lapatinib/Capecitabin sollte eine Untersuchung der Haut erfolgen. Trockene Hautareale sollten zweimal täglich mit einer dicken, alkoholfreien Pflegecreme eingecremt werden. Sonnenlichtexposition sollte ebenso wie Kälte, kaltes Wasser und Wind gemieden werden.
Psychologische Aspekte
Das Problem, dass selbst Krebspatientinnen nicht immer zu 100 % compliant sind, beleuchtete Prof. Rob Horne, Imperial College London: „Wenn sich Patienten gegen eine Therapie entscheiden, dann misstrauen sie in der Regel nicht dem betreuenden Arzt, sondern der Therapie.“ Neben praktischen Problemen beeinflussen Erfahrungen, Überzeugungen und Ressourcen der Patienten die Haltung gegenüber der Krebstherapie und damit die Compliance. Alle diese Aspekte sollten beleuchtet werden, um Patientinnen bestmöglich betreuen zu können.
* „HER2-targeted Therapy für Metastatic Breast Cancer – A multidisciplinary Approach“, Symposium im Rahmen des ESMO 2012, Wien