ASCO 2012: Gastrointestinale Tumoren
Ösophaguskarzinom
Für die definitive Strahlenchemotherapie wurden die Daten der PRODIGE-5-Studie vorgestellt. Patienten mit nichtoperablem Ösophagus-Ca wurden in 2 Gruppen randomisiert. Im Standardarm erhielten die Patienten Bestrahlung mit 50 Gy über 5 Wochen, gemeinsam mit 2 Zyklen 5-FU-Cisplatin-Chemotherapie gefolgt von 2 weiteren Zyklen 5-FU-Cisplatin ohne Bestrahlung. Im experimentellen Arm erhielten die Patienten ebenfalls eine Bestrahlung mit 50 Gy über 5 Wochen kombiniert mit 3 Zyklen FOLFOX-Chemotherapie gefolgt von 3 weiteren Chemotherapiezyklen mit FOLFOX. Bezüglich des primären Endpunktes ist die Studie negativ. Mit einem medianen Gesamtüberleben von 20,2 Monaten im experimentellen Arm verglichen mit 17,5 Monaten im Kontrollarm war der Unterschied nicht signifikant. In einem Nebenaspekt ist diese Studie jedoch dennoch beachtenswert. In der experimentellen Gruppe ist die Toxizität bis auf Neurotoxizität deutlich geringer, insbesondere ist die Zahl der plötzlichen Todesfälle und der therapieassoziierten Todesfälle deutlich reduziert. Auf Grund dieser signifikanten Verbesserung im Toxizitätsprofil ist bei Patienten, die für eine definitive Bestrahlung vorgesehen sind, eine Umstellung vom 5 FU/Cisplatin auf FOLFOX zu diskutieren.
Magenkarzinom
Kuratives Therapiekonzept
Für Patienten mit operablem Adenokarzinom des gastroösophagealen Übergangs oder des Magens ist in Europa bei Kaukasiern eine perioperative Chemotherapie nach Tumorboardvorstellung als Standard anzusehen. In Asien wird das Hauptaugenmerk auf eine postoperative Chemotherapie mit einem oralen 5-FU-Prodrugs +/– Oxaliplatin gelegt. Für kaukasische Patienten ist dieses Konzept nicht etabliert. Diskutiert wurde jedoch die Intensivierung der postoperativen Chemotherapie. In diesem Zusammenhang ist das „late-breaking abstract“ der ITACA-S-Studie bemerkenswert. Hier wurden in einer großen italienischen Studieninitiative 1.106 Patienten ab einem Stadium pT2b oder N+ nach stattgehabter D2-Operation randomisiert und erhielten im Standardarm 5-FU/LV, im experimentellen Arm 4 Zyklen FOLFIRI gefolgt von 3 Zyklen Docetaxel/Cisplatin. Die Toxizität war im experimentellen Arm deutlich höher. Im Gegensatz dazu kam es jedoch zu keinerlei Verbesserung im erkrankungsfreien Überleben oder im Gesamtüberleben. Diese Daten zeigen, dass eine intensivierte postoperative Chemotherapie (hier mit fast allen effektiven Substanzen) für diese Patienten als nicht indiziert angesehen werden kann. Insgesamt ist somit unverändert die perioperative Chemotherapie Standard.
Palliative Therapie
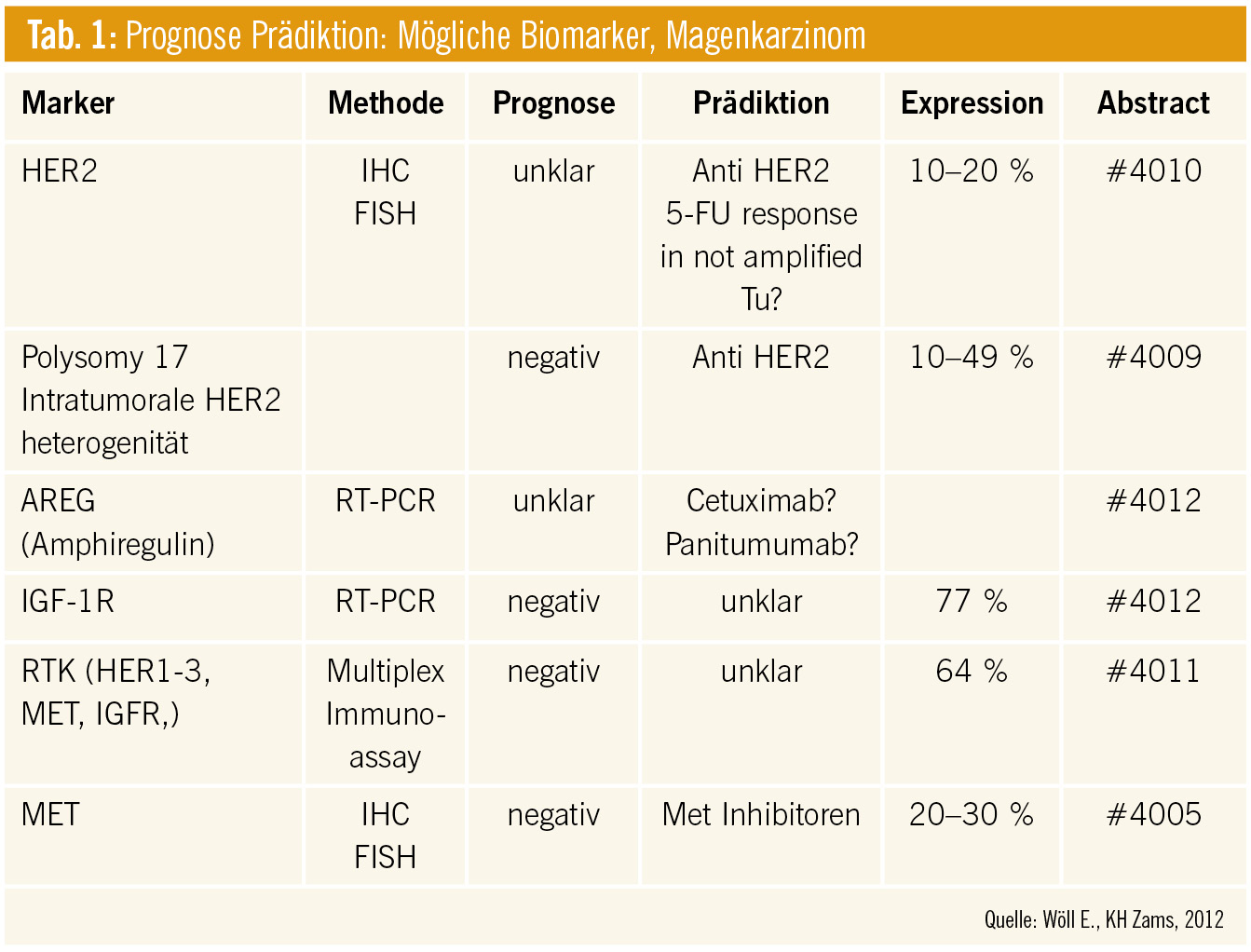
Trastuzumab: Eine adäquate HER2-Testung ist vor Therapiebeginn für inoperable Magenkarzinompatienten notwendig. Für diese Patienten steht derzeit eine Therapie mit Trastuzumab kombiniert mit Cisplatin und 5-FU/Capecitabin (ToGA-Studie) zur Verfügung. Bisher ist jedoch unklar, ob Trastuzumab auch mit anderen Chemotherapien kombiniert werden kann. Dies wird in einer nichtinterventionellen Studie untersucht. Es wurden 110 Patienten mit einer Trastuzumab-Kombination aus unterschiedlichen Zytostatika behandelt. Im gesamten Kolletiv ist das progressionsfreie Überleben mit 6,9 Monaten vergleichbar mit dem Ergebnis der Zulassungsstudie. Trastuzumab wird somit auch bei Patienten mit Kontraindikationen für Cisplatin und 5-FU/Capecitabin mit diversen anderen Chemotherapien als sicher und effektiv eingestuft.
Bevacizumab: Für den Einsatz von Bevacizumab beim Magenkarzinom wurden heuer lediglich Phase-II-Daten vorgestellt, die jedoch in Summe eine gewisse Effektivität für Bevacizumab zeigen. Hier ist die biologische Subgruppierung, in der Wirksamkeit erzielt werden kann, noch unklar. Weitere Untersuchungen mit antiangiogenetischen Substanzen sind aus meiner Sicht beim Magenkarzinom erfolgversprechend und sollten trotz einer negativen Phase-III-Studie (AVAGAST) durchgeführt werden.
EGFR-gerichtete Therapien: Die erste Phase-III-Studie für einen Anti-EGFR-Ansatz liegt mit den Ergebnissen von REAL-3 vor. Hier wurden Patienten mit inoperablem Magenkarzinom in EOX +/– dem humanen Antikörper Panitumumab randomisiert. Auf Grund der überlappenden Toxizität mussten jedoch im experimentellen Arm die Oxaliplatin- und Capecitabin-Dosis reduziert werden. Die Studie ist in ihrem primären Endpunkt negativ. Das Gesamtüberleben im experimentellen Arm war mit 8,8 Monaten schlechter als im Kontrollarm mit 11,3 Monaten (p = 0,013). Somit ist dieser Ansatz für ein unselektioniertes Patientenkollektiv offensichtlich mit einem negativen Effekt verbunden. Zur generellen Bewertung eines Anti-EGFR-Ansatzes sind letztlich die Daten der EXPAND-Studie abzuwarten, die beim ESMO 2012 präsentiert werden (Cetuximab in Kombination mit Chemotherapie). Mögliche Erklärungen für das negative Abschneiden sind die inadäquate Chemotherapiedosis im experimentellen Arm sowie die überlappenden Toxizitätsprofile. Möglicherweise spielt auch eine späte Postchemotherapietoxizität eine Rolle. Letztentlich fehlt beim Magenkarzinom jedoch ein Biomarker, der die Subgruppe von Patienten mit möglichem Benefit klassifizieren könnte. Panitumumab ist in unselektionierten Patienten zweifelsfrei nicht weiter verfolgenswert. Das Hauptaugenmerk muss also in die Entwicklung und Etablierung von prädiktiven Biomarkern gelegt werden.
Zweitlinienchemotherapie: In der Zweitlinientherapie ist derzeit eine Chemotherapie mit Irinotecan oder Docetaxel als Standard anzusehen. In diesem Setting wurden die Daten der WJUG4007- Studie vorgestellt, in der 223 Patienten nach Progress unter 5-FU/Cisplatin randomisiert mit Irinotecan (q2w) oder wöchentlichem Paclitaxel behandelt wurden. Beide Arme zeigten keinen signifikant Unterschied im Gesamtüberleben. Abgesehen von 7,4 % PNP im Paclitaxel-Arm war die Toxizität jedoch im Irinotecan-Arm schlechter. Wöchentliches Paclitaxel ist somit für Patienten, die keine wesentliche Polyneuropathie haben, eine mögliche Zweitlinientherapie. Lebensqualitätsdaten dieser Studie sind jedoch noch abzuwarten.
Pankreaskarzinom
In der kurativen Therapie des Pankreaskarzinoms ist eine adjuvante Gemcitabin-Monotherapie entsprechend der Daten der CONKO-001-Studie sowohl nach R0- als auch R1-Resektion derzeit als Standard anzusehen. Hier wurden Langzeitdaten mit der Fragestellung vorgestellt, ob Faktoren ein Langzeitansprechen voraussagen können. Unter den Untersuchungen der multivariaten Analyse konnte sich nur das Tumor-Grading als Prädiktor etablieren, wobei jedoch nur eine sehr geringe Patientenzahl evaluiert werden konnte. Hier ändert sich somit am Standard nichts.
In der palliativen Therapie wurden heuer zur Erhaltungstherapie mit Sunitinib, aber auch zur Kombinationstherapie eines EGFR-Inhibitors mit einem IGF-1R-Inhibitor und zur Therapie mit einem Hedgehog-Inhibitor in unselektionierten Patienten wenig überzeugende Daten präsentiert. Ähnlich wie beim Magenkarzinom ist in dieser Indikation die Untersuchung von Biologika ohne prädiktive Selektion nicht erfolgversprechend.
Kolonkarzinom
Adjuvante Therapie
Wenig neue Daten wurden zur adjuvanten Therapie im Stadium III vorgestellt. Bemerkenswert ist eine gepoolte Auswertung aus vier großen Studien (X-ACT, XELOXA, NSABP C-08 und AVANT): Aus diesen Studien wurden jeweils die älteren Patienten ausgewertet. Die Analyse bezog sich auf die Wertigkeit von Oxaliplatin, und es konnte gezeigt werden, dass XELOX/FOLFOX bei über 70-jährigen Patienten wirksamer ist als 5-FU oder Capecitabin. Dabei gilt es jedoch, das erhöhte Nebenwirkungsrisiko zu berücksichtigen. In Summe werden daher die bisherigen Daten der MOSAIC- und NSABP-C-07-Studien nicht komplett widerlegt. Sie deuten aus meiner Sicht jedoch auf die mögliche sichere Anwendung einer oxaliplatinhältigen adjuvanten Kombinationstherapie für hoch selektionierte Patienten mit sehr gutem Performance-Status und sehr hohem Rezidivrisiko hin.
Metastasierte Situation
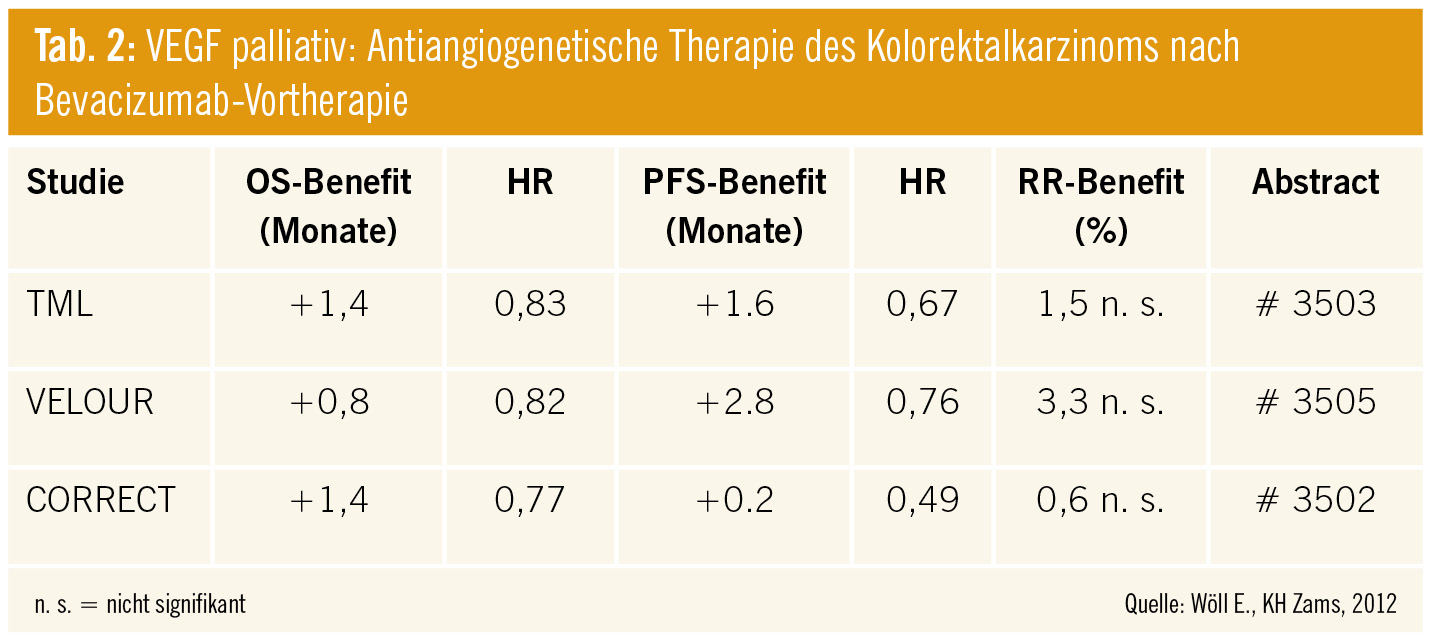
Drei große Studien haben hier den Ansatz einer kontinuierlichen und über den Progress hinausgehenden antiangiogenetischen Therapie entsprechend dem biologischen Konzept untersucht.
TML-Studie: In der TML-Studie, erhielten Patienten in der Erstlinie Bevacizumab und eine Standardchemotherapie (entweder oxaliplatin- oder irinotecanhältig). Bei Progress wurde die jeweilig alternative Chemotherapie eingesetzt. Randomisiert erhielten 50 % der Patienten auch in der Zweitlinientherapie Bevacizumab bis zum Progress. Sowohl was das PFS als auch das Gesamtüberleben anbelangt, konnte in dieser Studie eine Verbesserung erreicht werden. Dies mit den erwarteten und insgesamt günstigen Nebenwirkungen. Das Gesamtüberleben wurde von 9,8 auf 11,2 Monate signifikant verlängert. Diese Ergebnisse entsprechen zwar nicht ganz den sehr hohen Erwartungen, die durch die Anwengungsbeobachtungen und Registerauswertungen vorgelegt wurden, bestätigen jedoch das Prinzip einer zusätzlichen Therapielinie unter Fortsetzung von Bevacizumab. Unklar ist derzeit noch, welche Patientengruppe besonders profitiert. Hier wird in den nächsten Analysen auch die Rolle der KRAS-Mutation ausgewertet. Die diesbezüglichen Daten werden in Kürze vorgestellt.
VELOUR-Studie: Mit der VELOUR-Studie werden ähnliche Daten für eine Fortsetzung der antiangiogenetischen Therapie präsentiert. Aflibercept kombiniert mit FOLFIRI-Chemotherapie bringt eine Verbesserung des Gesamtüberlebens von 12,6 auf 13,5 Monate. Dieser Effekt ist statistisch signifikant. Beim ASCO wurden nun die Daten für jene Patientengruppen vorgestellt, die bereits vor Aflibercept-Gabe mit einem Angiogeneseinhibitor (Bevacizumab) behandelt wurden. Auch in dieser Gruppe wurde das Gesamtüberleben und das PFS verbessert. Somit handelt es sich hierbei um eine Subgruppenanalyse, die auch eine antiangiogenetische Wirksamkeit unabhängig von früherer Bevacizumab-Gabe untersucht.
CORRECT-Studie: Eine dritte Studie, die ein ähnliches Konzept, nun jedoch in einer Letztliniensituation bearbeitet, ist die CORRECT-Studie. Hier wurden Patienten mit fortgeschrittenem metastasiertem kolorektalem Karzinom nach Ausschöpfung der Standardchemotherapie mit Regorafenib (einem Multikinaseinhibitor, der auch die VEGFR 1–3 hemmt) plus beste unterstützende Therapie (BSC) versus Placebo plus BSC randomisiert. Auch hier zeigt sich eine Verbesserung des Gesamtüberlebens von 5 auf 6,4 Monate in der Letztliniensituation. Dieser Effekt ist statistisch signifikant und unabhängig vom KRAS-Status. Als häufigste Toxizitäten traten Hand-Fuß-Syndrom, Fatigue, Hypertonie und Hautreaktionen auf. Regorafenib stellt damit eine neue Therapieoption für Patienten in einer Letztliniensituation dar.
EGFR-Biomarker: Der zweite etablierte molekulare Therapieansatz mit EGFR-gerichteten Antikörpern wurde beim ASCO 2012 vor allem hinsichtlich Biomarker untersucht. Epiregulin und Amphiregulin, zwei Agonisten des EGF-Rezeptors, können möglicherweise die Wirksamkeit eines Anti-EGFR-Ansatzes voraussagen. Das zeigen retrospektive Auswertungen. Letztlich unklar ist jedoch die Methodik. Der Ansatz muss vor einem klinischen Einsatz prospektiv validiert werden.
DREAM-Studie: Auch zur Erhaltungstherapie wurde mit der DREAM-Studie eine große Studie vorgestellt. Hier wurden Patienten nach einer oxaliplatinhältigen oder irinotecanhältigen Bevacizumab-Kombinationstherapie mit Bevacizumab bis zum Progress oder Bevacizumab bis zum Progress kombiniert mit dem TKI Erlotinib behandelt. Bzgl. des progressionsfreien Überlebens zeigt sich ein kleiner, aber signifikanter Vorteil für die Kombinationstherapie. Dieser ist jedoch durch eine nicht unbeträchtliche Erhöhung der Toxizität erkauft. Aus meiner Sicht ist dieser Ansatz aufgrund der Kosten-Nutzen-Abwägung noch nicht reif für den Einsatz in der klinischen Praxis. Bemerkenswert ist jedoch das erstmalig positive Signal für die Kombinationstherapie eines Anti-EGFR-TKI und eines Anti-VEGF-Antikörpers beim kolorektalen Karzinom. Hier sind zur endgültigen Beurteilung weitere Studien abzuwarten.