Ausgewählte Highlights der ASH-Tagung
Beim letztjährigen Annual Meeting der American Society of Hematology (ASH) in San Diego wurden eine Vielzahl neuer Erkenntnissen im Bereich hämatologischer Neoplasien präsentiert. Im Folgenden werden selektiert Beiträge dargestellt, die von Bedeutung für das Verständnis der Pathobiologie oder Verbesserung der Therapie hämatologischer Erkrankungen sind.
Myelodysplastische Syndrome
Thrombopoetinanaloga ermöglichen bei einem Großteil thrombopener MDS-Patienten einen signifikanten Thrombozytenanstieg. Eine Studie von Giagounidis et al. wurde jedoch aufgrund einer erhöhten Rate an transienten Blastenanstiegen abgebrochen (Aristoteles Giagounidis, Abstr. #117). Nach Absetzen des Thrombopoetinanalogons Romiplostim fielen die Blasten wieder ab. Das Gesamtüberleben in dieser Studie, dRomiplostim, ie randomisiert Romiplostim gegenüber Placebo in „Low-Int.-1“-Risiko MDS-Patienten testete, ergab keinen signifikanten Unterschied. Beobachtungen bei Patienten mit schwerer aplastischer Anämie, bei denen ebenfalls Thrombopoetinanaloga zur Therapie der Thrombopenie getestet wurden, zeigten interessanterweise neben einem Thrombozytenanstieg auch einen Anstieg der Leukozyten, was darauf hinweist, dass die Thrombopoetinanaloga auch die Myelopoese stimulieren können. Diese Beobachtung erklärt eventuell die erhöhte Rate an transienten Blastenanstiegen im peripheren Blut unter Romiplostim bei Patienten mit myelodysplastischen Erkrankungen.
Eine weitere biologisch interessante Be obachtung war, dass Eisenchelation bei MDS-Patienten offensichtlich auch einen Einfluss auf den Verlauf der Erkrankung nimmt. Die Zeit zur Transformation wird unter Chelatortherapie um 12 Monate nach hinten verschoben. Die entsprechenden Informationen stammen aus Registerdaten, die 600 „Low risk“-Patienten mit einem Serumferritin von >1000 μg/l oder hoher Transfusionslast einschlossen (Roger M Lyons, Abstr. #2800). Eine zweite retrospektive Studie bestätigt diese Daten und zeigte für eisenchelierte Patienten sogar einen signifikanten Gesamtüberlebensvorteil (Rami S Komrokji, Abstr. #2776).
Akute Leukämien
Höhepunkt im Feld akuter Leukämien war der Beitrag zur Untersuchung von Mutationsfrequenzen in präleukämischen hämatopoietischen Stammzellen (HSC) (Max Jan, Abstr. #4). Mittels „whole exon sequencing“ konnten im Mittel 10 Mutationen in residuellen HSC bei Patienten in kompletter Remission nach Therapie nachgewiesen werden, wobei diese HSC normale In-vitro-Differenzierungskapazität aufwiesen. Zu solch frühen Mutationen gehört beispielsweise die NPM1c-Mutation. Dem Modell einer sequenziellen Akkumulation von Mutationen folgend, gehören dagegen Flt-3 ITD und IDH1 R132H zu späten Mutationen, die in präleukämischen HSC nicht nachzuweisen sind. Genetische Analysen erlauben hierbei die Architektur der Subklone nachzuvollziehen, wobei normale HSC bis zu 50-mal häufiger als präleukämische HSC sind. Die Daten suggerieren, dass präleukämische HSC das zelluläre Target einer suffizienten Therapie der minimalen Resterkrankung darstellen.
Chronische myeloische Leukämie
Bezüglich der Zweit-Generations-TKI in der Erstlinienbehandlung ergaben sich keine neuen Aspekte, außer dass die bereits bekannte Verbesserung der Wirksamkeit von Nilotinib gegenüber Imatinib auch in den letzten Updates der ENESTnd-Studie bestätigt werden konnte. Es kristallisiert sich zudem heraus, dass die frühe Kinetik der BCR-ABL-Reduktion das langfristige Ansprechen vorhersagen kann. Das heißt, dass Patienten mit einer mindestens 90 % Reduktion der BCR-ABL-Last zum Zeitpunkt 3 Monate nach Therapiebeginn langfristig ein optimales Therapieoutcome haben (Andreas Hochhaus, Abstr. #2767). Bisher fehlen jedoch Daten aus prospektiv randomisierten Studien, die bestätigen, dass eine Änderung der Therapie nach diesen frühen Landmarks auch langfristig den Verlauf der Erkrankung modifiziert.
Die interessanteste Neuerung im Bereich der CML/ALL waren die erweiterten Daten zu Ponatinib, einem Tyrosinkinasehemmer, der auch bei T315I-positiver CML wirksam ist. Präsentiert wurden Daten der Phase-II-Studie PACE, in der 403 Patienten mit Ponatinib behandelt wurden (Jorge E Cortes, Abstr. #109). 106 Patienten hatten eine T315l-Mutation, 110 Patienten weitere bereits bekannte Mutationen, die eine Resistenz gegenüber den zugelassenen TKI induzieren. Hauptnebenwirkungen waren Thrombopenien, Hautausschlag, Kopf- und Gelenkschmerzen sowie trockene Haut und Bauchschmerzen. Die Haupt-SAEs waren Pankreatitis, Diarrhö, Anämie, febrile Neutropenie und Pyrexie. Von 159 auswertbaren Patienten in chronischer Phase der CML erreichten bei einem medianen Follow-Up von 57 Tagen 42 % eine MCyR (major cytogenetic response), worunter eine CCyR-Rate (complete cytogentic response) von 25 % nachweisbar war. Patienten in fortgeschrittenen CML-Phasen und ALL-Patienten erreichten zumindest ein major hämatologisches Ansprechen. Somit zeigen erste Daten trotz des noch sehr kurzen Followup, dass Ponatinib eine aktive Substanz bei nachhaltig vorbehandelten und TKIresistenten CML- und ALL-Patienten ist. Damit wird sich eine hochinteressante TKI-Alternative für schwierig zu behandelnde Mutationen entweder als Kombinationstherapie oder als Bridging zu einer möglichen Transplantation mit großer Wahrscheinlichkeit etablieren.
Philadelphia-negative MPN (Myelofibrose)
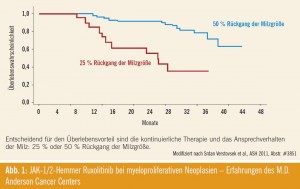
Es ist bisher nicht bekannt, ob die Anwendung von JAK2-Hemmstoffen (wie z. B. Ruxolitinib) zu einem verbesserten Überleben der Patienten mit Int-2- oder High-Risk-Myelofibrose führt. Erste im NEJM 2011 publizierte Daten der Mayo- Klinik deuteten darauf hin, dass Ruxolitinib zu keiner Verbesserung des Überlebens führt. Diese Daten konnten nun durch eine Auswertung einer größeren Patientenkohorte des MD Anderson Cancer Centers widerlegt werden (Abb. 1), wobei die Autoren auch auf den Grund der unterschiedlichen Überlebenseffekte der beiden Kohorten eingehen (Srdan Verstovsek, Abstr. #3851).
Es konnte hier klar gezeigt werden, dass die Anzahl an Therapieabbrüchen und Therapieunterbrechungen in der Mayo-Kohorte deutlich höher war, was wiederum zu einer geringeren median verabreichten Dosis von Ruxolitinib geführt hat. Die mediane Dosis der MD-Anderson-Kohorte ist vergleichbar mit der Dosis, die in der Comfort-I-Studie appliziert wurde. Von letzterer liegen bisher keine signifikanten Überlebensunterschiede vor, was aber primär auf die noch zu kurze Nachbeobachtungszeit zurückzuführen ist. Informationen zur Korrelation der applizierten Dosis und den korrespondierenden Wirkspiegeln im Serum/Plasma und deren Einfluss auf das Therapieansprechen liegen leider derzeit ebenfalls noch nicht vor.
Lymphome
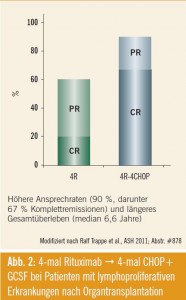
Bei den Lymphomen wurden hochinteressante Daten zu lymphoproliferativen Erkrankungen nach Organtransplantation (PTLD; Post-Transplant Lymphoproliferative Disorder) präsentiert (Ralf Trappe, Abstr. #878). In einer prospektiven Phase-II-Studie (die bisher größte prospektiv untersuchte PTLD-Kohorte) erhielten die Patienten sequenziell 4-mal Rituximab gefolgt von 4-mal CHOP+ GCSF, was zu einer Überlebensverlängerung von 3 Jahren führte. Die Gesamtansprechrate der Patienten, die Rituximab gefolgt von CHOP erhielten, betrug 90 % (67 % CR). (Abb. 2) 74 % der Patienten sind nach 5 Jahren noch progressionsfrei, das mediane Überleben beträgt 6,6 Jahre. Das Ansprechen auf Rituximab ist positiv mit der Zeit zur Progression wie auch mit dem Gesamtüberleben assoziiert. Zudem ist die Mortalität dieses Vorgehens (wahrscheinlich infolge der initialen Tumor-Lastreduktion durch 4-mal R ) erheblich niedriger verglichen zu historischen Vergleichsdaten, die CHOP alleine als First-Line-Therapie erhielten. Interessanterweise waren ca. 50 % der Patienten EBV-negativ, wobei das Vorgehen unabhängig vom EBV-Status zu einem hervorragenden Ansprechen führte. Damit sollte trotz fehlender prospektiv randomisierter Studien dieses Konzept einer Rituximab-„Vorphase” gefolgt von einer effektiven Chemotherapie als „Standard“ in diesem Patientenkollektiv angesehen werden.
Stammzelltransplantation
In der Plenary Session wurde eine wichtige Studie im Bereich der allogenen Stammzelltransplantation präsentiert, die einige Fragen aufwirft (Claudio Anasetti, Abstr. #1). Es werden heute ca. 75 % der allogenen Stammzelltransplantationen mit peripheren Blutstammzellen als Graft-Source durchgeführt. Lediglich in 25 % der Fälle wird Knochenmark transplantiert. Die am ASH präsentierte prospektiv randomisierte Phase-III-Studie hat nun diese beiden Stammzellquellen im Setting der klassischen myeloablativen Konditionierung miteinander verglichen. Es wurden 551 Patienten randomisiert. Das Ergebnis bezüglich des schnelleren Engraftments (5–7 Tage früher) beim Einsatz peripherer Blutstammzellen ist nicht überraschend, ebenso wenig überraschend ist, dass Patienten, die Knochenmark erhielten, eine niedrigere Rate an chronischer Graft-versus- Host-Erkrankung (GvHD) entwickelten, sowie dass die Rate an Transplantatversagen in der Knochenmark-Gruppe um ca. 6 % höher war. Interessant ist jedoch, dass die restlichen Parameter, wie die Rezidivrate und das Gesamtüberleben, sich nicht voneinander unterschieden. Nach 2 Jahren war das Gesamtüberleben jener Gruppe, die periphere Blutstammzellen erhielt, mit 51 % zwar tendenziell besser als das der Knochenmarkgruppe (46 %), nach 3 Jahren jedoch waren die OS-Raten mit 43 % vergleichbar. Passend hierzu zeigte sich auch kein Unterschied in der Rate an Rezidiven (27 % nach 3 Jahren in beiden Gruppen). Für die Lebensqualität jedoch relevant, zeigte sich bei der Rate an extensiver chronischer GvHD ein hochsignifikanter Nachteil in der Gruppe jener Patienten, die periphere Blutstammzellen erhielten: Hier waren 48 % versus 32 % betroffen. Der Stellenwert der Stammzell-Quelle für die Transplantation nach reduzierter Konditionierung bleibt auch durch diese Studie unbeantwortet. Es ist aber anzunehmen, dass auch in diesem Setting, das ja bekanntermaßen durch eine höhere Rate an chronischer GvHD charakterisiert ist, periphere Blutstammzellen ebenfalls einen Nachteil aufweisen. Auf der anderen Seite ist die chronische GvHD mit einem geringeren Rezidivrisiko assoziiert, so dass hier eventuell der Graft-versus-Tumor-Effekt im RIC-SCT-Setting eine höhere Bedeutung hat.
KEY MESSAGES
Myelodysplastische Syndrome
- Studienabbruch mit einem TPO-Agonisten aufgrund eines transienten Blastenanstiegs (mit potenziell höherem AML-Transformationsrisiko) bei MDS-Patienten mit niedrigem/intermediärem Risikoprofil
- Eisenchelation beeinflusst den Erkrankungsverlauf positiv: längere Zeit zur AML-Transformation und Überlebensvorteil
Akute myeloische Leukämie
- Das Auffinden spezifischer früher Mutationen in präleukämischen Stamm – zellen bei AML-Patienten in klinischer Komplettremission legt die Vermutung nahe, dass eine dauerhafte Remission die Eradikation dieser Stammzellen voraussetzt (die andernfalls durch klonale Evolution und Akquirierung neuer Mutationen ein Rezidiv bilden)
Chronische myeloische Leukämie
- Erste Ergebnisse der PACE-Zulassungsstudie mit Ponatinib zeigen, dass konventionell therapieresistente Patienten (z. B. infolge einer T315I-Mu – tation) von dem neuen Tyrosinkinasehemmer profitieren
Philadelphia-Chromosom-negative myeloproliferative Neoplasien
- Eine kontinuierliche Therapie und ein Rückgang der Splenomegalie sind entscheidende Kriterien für das Überleben von Patienten mit myeloproliferativen Erkrankungen, die mit dem JAK-Hemmer Ruxolitinib behandelt werden
Lymphome
- Bei Patienten mit lymphoproliferativen Erkrankungen nach einer Organtransplantation („Post-Transplantation-Lymphom“) wurde mit der sequenziellen Therapie aus 4-mal Rituximab → 4-mal CHOP + GCSF ein Überlebensvorteil von 3 Jahren erzielt
Stammzelltransplantation
- Abstract #1: Weniger extensive chronische Graft-versus-Host-Erkrankungen, wenn für allogene Stammzelltransplantationen (nach myeloablativer Konditionierung) das Knochenmark als Stammzellquelle verwendet wird (und nicht, wie gängige Praxis, das periphere Blut)