Chemotherapie und Nanopartikel-Technologie – Hochselektive Applikation aus dem Labor
Liposomen und Nanopartikel
Aufgrund ihrer spezifischen physikochemischen Charakteristika und der daraus resultierenden Verteilung im Körper erreichen pharmazeutische Wirkstoffe nur zum Teil den Zielort. Bei Chemotherapien hat dieser Effekt – abgesehen von der Schmälerung des therapeutischen Benefits – die Entstehung von teils erheblichen Toxizitäten durch das unerwünschte Einwirken auf andere Organe und Gewebe zur Folge.
Aufgrund dessen konzentrieren sich Forschungen schon lange auf die Entwicklung von Transportsystemen, die eine gezielte Applikation von Chemotherapeutika ermöglichen. In diesem Zusammenhang spielt die Nanotechnologie eine gewichtige Rolle. Nanotechnologisch hergestellte Trägersysteme bewegen sich in der Größenordnung von unter einem Mikrometer; durch die Kopplung an diese Systeme sollen schwer lösliche Wirkstoffe im Idealfall auch ohne die gängigen Solventien transportfähig gemacht und besser an den Tumor herangeführt werden. In klinischer Verwendung befinden sich bereits Lipidvesikel (z. B. liposomales Doxorubicin/Daunorubicin). Seit fast 40 Jahren werden Nanopartikel erforscht, d. h. feste Partikel im Größenbereich zwischen 10 und 1.000 nm, in die der Wirkstoff eingeschlossen wird.
Auswahl des Vehikels
Nanopartikel-Systeme sollten in der Lage sein, die aktiven Substanzen in langsamer und nachhaltiger Form abzugeben, sodass therapeutische Konzentrationen über längere Zeit hinweg erreicht werden1. Dadurch lässt sich nicht nur die Verabreichungshäufigkeit verringern, sondern auch die Wahrscheinlichkeit für das Auftreten von Toxizitäten senken. Eine weitere gewünschte Eigenschaft des Trägersystems besteht naturgemäß in der Bioabbaubarkeit, die einer Akkumulation mit toxischen Effekten vorbeugt. Als Vehikel wurde im Rahmen der Herstellung von Nanopartikeln bereits eine Reihe von Materialien getestet, z. B. Polyalkylcyanoacrylate, Poly-ε-Caprolacton, Polysorbat 80, Gelatine und Albumin. Prinzipiell können sowohl synthetische, gewebeverträgliche Polymere als auch natürliche Makromoleküle wie Proteine zur Anwendung kommen.
Albumin eignet sich aufgrund einer Reihe an günstigen Eigenschaften besonders gut für diese Aufgabe. Als körpereigener Träger hydrophober Moleküle und Transportmittel für Fettsäuren, Hormone und fettlösliche Vitamine ist es biokompatibel und bioabbaubar. In Albumin- Nanopartikeln enthaltene Wirkstoffe können durch Proteasen freigesetzt werden. Die Herstellung von Albumin-Nanopartikeln ist weit verbreitet, einfach und standardisiert.
EPR-Effekt
Eine passive Anreicherung der Nano – partikel wird durch den EPR-Effekt (Enhanced Permeability and Retention) begünstigt, der auf den pathophysiologischen Merkmalen der meisten soliden Tumoren beruht2. Es findet sich eine umfangreiche Angiogenese mit abnormaler Gefäßarchitektur, der lymphatische Abfluss ist gestört, und verschiedene Permeabilitätsmediatoren werden verstärkt produziert. Die gesteigerte Gefäßdurchlässigkeit gewährleistet die für das rasche Tumorwachstum erforderliche Sauerstoff- und Nährstoffversorgung. Dieser EPR-Effekt wurde für Lipide und Makromoleküle universell in soliden Tumoren dokumentiert. Aus therapeutischer Sicht ermöglicht er die gezielte Anwendung von lipid- oder polymerkonjugierten Antikrebstherapien, da sich die Partikel, die für die Passage durch das normale Endothel gesunder Zellen zu groß sind, selektiv im Tumor anreichern können.
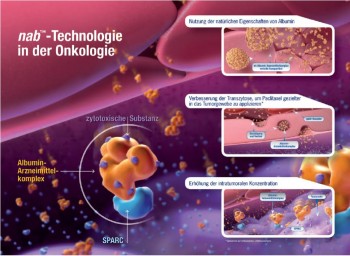
Albumin statt Cremophor: Mit Albumin- Paclitaxel liegt nun die erste erfolgreich in klinischen Studien getestete Nanopartikel- Applikation vor (s. Kommentar). Paclitaxel ist aufgrund seiner komplexen Struktur aus Hydrocarbon-Radikalen hydrophob und wird daher bei der traditionellen Herstellung an Lösungsvermittler wie Cremophor EL gebunden3. Diese Substanzen sind allerdings ihrerseits mit Toxizitäten behaftet, die sich vor allem in Form von Hypersensitivitätsreaktionen niederschlagen können. Dagegen erlaubt die Kopplung an humanes Albumin die Herstellung einer kolloidalen Suspension aus stabilen Partikeln, ohne dass weitere Toxizitäten in Kauf genommen werden müssen. Dank des EPR-Effekts findet eine Anreicherung von Albumin-Paclitaxel im Tumor statt, wobei ein aktiver Transportmechanismus zusätzlich unterstützend wirkt. Somit können die Benefits der Chemotherapie unter Ausnutzung des natürlichen Albumintransports in die Zelle mit der derzeit größtmöglichen Punktgenauigkeit ausgeschöpft werden.
1 Das S et al., Trends Biomater Artif Organs 2005; 18:203–212
2 Maeda H et al., J Control Release 2000; 65:271–284
3 Cortes J et al., EJC Supplements 2010; 8(1):1–10