Effektive adjuvante Therapie bei GIST
Bereits in der Phase-II-Studie (ACOSOG Z9000; n = 107) erzielte eine 1-jährige Therapie mit Imatinib 400 mg/d im Anschluss an die komplette Tumor – resektion bei Hochrisikopatienten mit primärem GIST hohe Überlebensraten. Das rezidivfreie Überleben lag nach einem Follow-up von 1, 2 und 3 Jahren bei 94 %, 73 % und 61 % (De Matteo et al., 2008).
ACOSOG Z9001
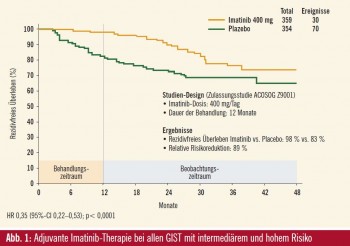
In der ersten doppelblinden, multizentrische Phase-III-Zulassungsstudie ACOSOG Z9001 konnte unter Imatinib im Vergleich zu Placebo das rezidivfreie Überleben nach der Resektion eines c- Kit-positiven, lokalisierten primären GIST von mindestens 3 cm Größe ebenfalls signifikant verlängert werden (De Matteo et al., 2009). 713 Patienten aus den USA und Kanada erhielten im Anschluss an die Operation ein Jahr lang randomisiert entweder Imatinib 400 mg/d (n = 359) oder Placebo (n = 354). Primärer Endpunkt war die Verbesserung des rezidivfreien Überlebens nach einem Jahr. Patienten aus dem Placebo-Arm konnten bei Auftreten eines Rezidivs in den Imatinib- Arm wechseln. Da der primäre Endpunkt bereits zum Zeitpunkt einer geplanten Interimsanalyse erreicht war, wurde die Studie entblindet, und Patienten aus dem Placebo-Arm konnten in den Imatinib-Arm wechseln. Nach einem medianen Follow-up von 19,7 Monaten wurde unter Imatinib ein signifikant verbessertes rezidivfreies Überleben von 98 % vs. 83 % erzielt (HR: 0,35; p < 0,0001), dies entspricht einer relativen Risikoreduktion von 89 % (Abb. 1). Unter Placebo erlitten 41 Patienten ein Rezidiv, während unter Imatinib nur ein einziges Rezidiv dokumentiert wurde.
Stratifikation nach Tumorgröße: Für die Analyse wurden die Patienten auch in Hinblick auf die Tumorgröße stratifiziert (≥ 3 bis < 6; ≥ 6 bis < 10; ≥ 10 cm). In allen drei Gruppen war das rezidivfreie Überleben unter Imatinib verlängert. Dies ist vor allem für Patienten mit größeren Tumoren von besonderer Bedeutung, da sie ohne adjuvante Therapie eine mehr als 50%ige Wahrscheinlichkeit aufweisen, nach zwei Jahren ein Rezidiv zu erleiden. Die Tatsache, dass die Rezidivrate rund 18 Monate nach der Operation und somit 6 Monate nach Beendigung der Studie im Imatinib-Arm anstieg, ist konsistent mit Ergebnissen einer französischen Studie mit metastasierten GIST-Patienten, in der gezeigt werden konnte, dass der Behandlungsstopp nach 1, 3 oder 5 Jahren obligat in Rezidiven mündete (Ray-Coquard et al., 2010).
Patientenselektion durch Risikostratifizierung
Für die Entscheidung, ob eine adjuvante Therapie infrage kommt, ist die Evaluierung der Rezidivwahrscheinlichkeit von grundlegender Bedeutung. Prinzipiell sind alle GIST mit einem hohen malignen Potenzial behaftet, außer Tumoren von unter einem Zentimeter Durchmesser. Als wichtigste Prädiktoren für das klinische Verhalten wurden Tumorgröße, Mitoseindex und Tumorlokalisation identifiziert (Miettinen et al., 2006).
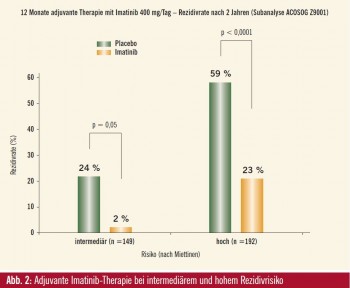
Dementsprechend ergab die Analyse der pathologischen Daten der ACOSOGZ9001- Studie, dass ein hoher Mitoseindex, Tumorgröße und Lokalisation im Dünndarm Prädiktoren für das rezidivfreie Überleben unter einer Imatinib-Therapie darstellen (Blackstein et al., 2010). Nach Risikostratifizierung anhand oben genannter Prädiktoren (Miettinen et al., 2006) lag die Rezidivrate nach 2 Jahren für Patienten mit niedrigem Risiko unter Imatinib und Placebo gleichermaßen bei 2 % (p = 0,92), für Patienten mit intermediärem Risiko unter Imatinib bei 2 % vs. 24 % unter Placebo (p = 0,05) und für Hochrisiko-Patienten bei 23 % vs. 59 % (p < 0,0001) (Abb. 2). Eine zusätzliche Analyse von Corless et al. zeigte, dass auch der Mutationsstatuts der Erkrankung eine prädiktive Rolle spielt. Patienten mit c-Kit-Exon-11-Mutation oder PDGFR-A-Mutation zeigten ein sehr gutes Ansprechen und eine signifikant niedrigere Rezidivrate auf die adjuvante Therapie mit Imatinib.
Therapiedauer bei adjuvanten GIST-Patienten
Zur optimalen Dauer der Behandlung mit Imatinib bei Hochrisiko-GIST-Patienten gibt es noch keine Daten aus randomisierten Studien. Untersucht wird derzeit eine 1- versus 3-Jahres-Behandlung mit Imatinib in einer deutsch-skandinavischen randomisierten Phase-III-Studie (SSG Trial XVIII). Im Anschluss an die Operation erhalten Patienten mit hohem Rezidivrisiko randomisiert 1 oder 3 Jahre lang Imatinib. Der primäre Endpunkt wurde auch in dieser Studie mit rezidivfreiem Überleben definiert.
Im Rahmen des 2. Meetings des GIST Panels Austria im Jänner 2011 in Loipersdorf wurde u.a. auch darüber diskutiert, wie lange derzeit die adjuvante Imatinib-Therapie verabreicht werden soll: Ich persönlich diskutiere mit Hochrisikopatienten mit Imatinib-sensitiven Mutationen individuell, ob eine adjuvante Therapie mit Imatinib für länger als ein Jahr Sinn macht. Dies ist aus meiner Sicht relevant, da die Wahrscheinlichkeit eines Rezidivs bei diesen Patienten gegeben ist. Die mit Spannung erwarteten Daten der 3-jährigen adjuvanten Therapie mit Imatinib werden höchstwahrscheinlich am diesjährigen ASCO – sprich: im Juni 2011 – präsentiert werden. Demzufolge geht es um eine zusätzliche Therapiedauer von 3–4 Monaten.
Literatur:
– Ray Coquard et al., J Clin Oncol 2010; 28:15s (suppl; abstr 10032)
– DeMatteo et al., The Lancet 2009; 373(9669):1097–1104
– Miettinen & Lasota., Seminars in Diagnostic Pathology 2006; 23:91–102
– DeMatteo et al., ASCO 2008, abstr 8
– Blackstein et al., ASCO-GI 2010, abstr 6
– Corless et al., J Clin Oncol 2010; 28:15s, 2010 (suppl; abstr 10006)